硫酸铜晶体含水量的测定
教学内容
测定硫酸铜晶体的含水量
基本概念
CuSO4·5H2O 在常温和通常湿度下既不易风化,也不易潮解,是一种比较稳定的结晶水合物。CuSO4·5H2O受热时逐步失去结晶水的过程可表示如下:
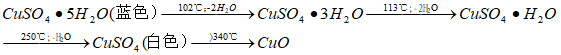
加热一定质量的硫酸铜晶体 m(CuSO4·5H2O),使其全部结晶水失去,得到CuSO4和结晶水的质量数据m(CuSO4)和m(H2O),计算1mol硫酸铜晶体中含有结晶水的物质的量,以确定硫酸铜晶体的化学式,可按下式计算:

式中:m、M、x分别为质量、摩尔质量、水的物质的量。
结晶水的质量分数(ω)为:
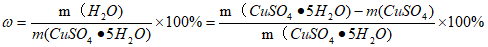
要使实验获得较准确的结果,操作的关键是加热要保证晶体全部失水,但又不能造成CuSO4的分解,判断的标准是粉末全白、无蓝色或黑色。另外,冷却后的称量应准确,且两次称量的质量差不超过0.1g。
标准操作
加热
加热是使物质升高温度的操作。加热为了增大反应速度、加热固体溶解、蒸发浓缩、熔融、升华、加热保温,或者杀菌消毒和凝固、沉淀蛋白质等。
加热方法分火焰直接加热法和间接加热法两种。
直接加热法
物质盛放在试管、蒸发皿、坩埚等容器内,用火焰直接加热。给试管中的液体加热时,试管应夹在近管口处,试管跟桌面成45度角,管口不可对着自己和别人,加热时还应先把试管放在外焰的上部来回移动,使试管受热均匀。然后把试管放在外焰的中部,从试管里的液面开始逐渐下移到试管底部,并不时上下移动试管。
给试管中的固体加热时,试管内的固体要铺平,试管口要略向下倾斜,以防冷凝水流到管底而使试管破裂。铁夹夹在近试管口处,待试管固定在铁架台上后,手持灯具,用外焰的上部来回使试管受热均匀,然后用外焰几种加热近试管口的固体部分,等该处固体反应完毕,再把火焰逐步移向试管底部。
用蒸发皿蒸发液体的操作,要用氧化焰加热,如果还原焰接触蒸发皿底部,会出现炭黑。
需要高温加热的固体,通常放在瓷坩埚内,瓷坩埚放在铁圈或铁三脚架的泥三角上加热,夹取高温下的坩埚,应该用干净的坩埚钳。坩埚钳不用时,应尖端朝上平放,以保持尖端洁净。
间接加热法
给烧杯或烧瓶里的液体加热时,所盛液体的量一般是本身容积的1/3,最多不超过1/2,以防止沸腾时液体溢出或向外冲出。加热时,火焰不能接触烧杯或烧瓶,而要隔着石棉网加热,防止受热不均匀而使仪器破裂,或液体局部过热分解。把受热容器放在水浴、蒸汽浴、油浴、砂浴、石蜡浴、盐浴以及易熔金属浴里加热,也都属于间接加热。中学化学实验室里常用的是水浴,其次是砂浴。这种加热方法的优点是温度容易控制和容器内的物质受热均匀。
水浴加热加热温度不超过100℃时(如测定硝酸钾的溶解度、测定四氯化碳的分子量、制取硝基苯、制取酚醛树脂等),可以用水浴加热。水浴加热一般在水浴锅中进行,也可用盛水的烧杯代替水浴锅。被加热的物质连同盛器浸入水中,使受热物质全部浸没在水里,且盛器不能跟烧杯底相碰。
砂浴加热砂浴可以加热到350~400℃。作砂浴用的黄砂要粒细而均匀,不含有机物。
加热的注意事项:
(1)加热前一般要擦干受热仪器外壁上的水(水浴加热除外)。加热时先用小火均匀加热,然后用大火加热。直接在火焰上加热的仪器不能碰到灯芯。加热后仪器不能立刻接触冷水或冷物体,可以放在干的试管架或石棉网上,让它自然冷却,防止仪器突然遇冷而破裂。
(2)水浴锅盛水为本身容积的1/2~2/3.加热时要随时添加热水,以防烧干。被加热的容器可以搁在大小适当的圆盖上或浸没在水中。浸在水中时容器不要碰倒水浴锅底,防止容器受热不均匀而破裂。加热类似酒精、乙醚等易燃烧、易挥发的有机溶剂时,应先把水浴锅中的水加热到一定的温度后熄灭灯焰,再把盛有易燃烧、易挥发物质的容器放在水浴中加热,且不能接近明火,以防蒸汽燃烧。
(3)用砂浴加热时,先把干净的黄砂放在铁盘中,再把盛加热物质的容器埋在黄砂中,黄砂传热慢,容器底部的黄砂层要薄些,便于容器受热。容器周围的黄砂层要厚些,以便保暖。
(4)加热温度在室温~600℃之间,可以用酒精灯和水浴、砂浴、烘箱加热;在600~1000℃时,宜用煤气灯或酒精喷灯;1000℃以上,用电炉或高频电路。
干燥器
干燥器是一种具有磨口盖子的厚质玻璃器皿,磨口上涂着一薄层凡士林,使其更好地密合,底部放适当的干燥剂,其上架有洁净的的带孔瓷板,以便放置坩埚和称量瓶等。
干燥器使用注意事项
(1)干燥剂不可放得太多,以免沾污坩埚底部。
(2)搬移干燥器时,要用双手拿着,用大拇指紧紧按住盖子。
(3)打开干燥器时,不能往上掀盖,应用左手按住干燥器,右手小心地把盖子稍微推开,等冷空气徐徐进入后,才能完全推开,盖子必须仰放在桌子上。
(4)不可将太热的物体放入干燥器中。
(5)有时较热的物体放入干燥器中后,空气受热膨胀会把盖子顶起来,为了防止盖子被打翻,应当用手按住,不时把盖子稍微推开(不到1s),以放出热空气。
(6)燃烧或烘干后的坩埚和沉淀,在干燥器内不宜放置过久,否则会因吸收一些水分而使质量略有增加。
(7)变色硅胶干燥时为蓝色,受潮后变粉红色.可以在120度烘受潮的硅胶待其变蓝后反复使用,直至破碎不能用为止。
实验步骤
实验装置图如图所示,实验步骤简述如下:
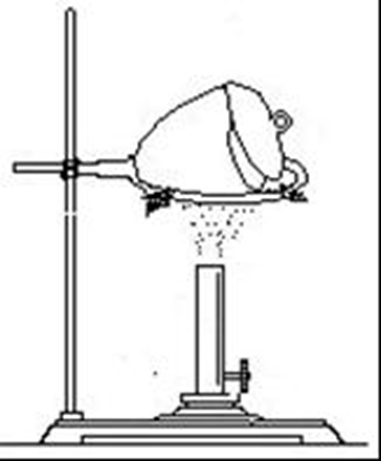
研磨在研钵中将硫酸铜晶体研碎
称量准确称量清洁干燥(包括内外壁)瓷坩埚的质量(设为m1),并用该坩埚称取约2g(准确到0.1g)已经研碎的硫酸铜晶体(设坩埚和硫酸铜晶体总质量为m2)。
加热将盛有硫酸铜晶体的坩埚放在三脚架上面的泥三角上,缓慢加热坩埚,直至其中的硫酸铜晶体由蓝色晶体变白色粉末,且不再有水蒸气逸出。然后将坩埚放入干燥器内冷却。
称量坩埚冷却后,把坩埚放在台秤上称量(记下总质量)。
再加热称量把盛有无水硫酸铜的坩埚再加热数分钟,然后再放在干燥器里冷却后再称量(记下总质量),至两次称量的质量相差不超过0.1g为止(设最后恒定总质量为m3)。
数据处理和计算。
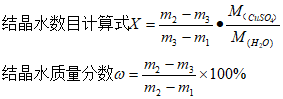
内容拓展
水合晶体失水后的固体粉末是否是晶体呢?
晶体是具有空间格子结构的固体,即组成晶体的分子、原子或离子在空间中呈有规则的排列,晶体的规则的几何外形是它内部(空间格子)结构有规则的反映。在良好的生长条件下,晶体外形的规则性可以完美地反映出来,如食盐和明矾都是具有完美地晶型。有时,外界生长条件不利于规则外形的生长,就成细小微晶粉末(如溶液中发生化学反应析出的沉淀)和多晶聚集体(如金属铸锭),它们无规则的几何外形,却具有空间格子结构,它们都是晶体。失水的硫酸铜仍是晶体,这种粉末虽无肉眼可见的规则的几何外形,但实际上它还是晶体。
硫酸铜晶体结晶水含量测定实验误差分析表。
| 能引起误差的一些操作 | 因变量 | ω或x值 | |
| m (CuSO4) | m (H2O) | ||
| 称量的坩埚不干燥 | — | 增大 | 偏大 |
| 晶体表面有水 | — | 增大 | 偏大 |
| 晶体不纯,含有不挥发杂质 | 增大 | — | 偏小 |
| 晶体未研成细粉末 | — | 减小 | 偏小 |
| 粉末未完全变白就停止加热 | — | 减小 | 偏小 |
| 加热时间过长,部分变黑 | 减小 | — | 偏大 |
| 加热后在空气中冷却称量 | — | 减小 | 偏大 |
| 加热过程中有少量晶体溅出 | 减小 | — | 偏大 |
| 两次称量相差大于0.1g | — | 减小 | 偏小 |


