酸碱平衡紊乱
体液环境适宜的酸碱度,是机体维持正常的生理功能和代谢的必要条件之一。正常生命活动过程中,机体不断生成酸性和碱性物质,也经常摄取一些酸性和碱性食物,但是体液酸碱度总能保持相对稳定,用动脉血 pH表示是7.35~7. 45,平均值为7.40,呈弱碱性。体液的酸碱度在这样范围很窄的环境内变动,是依靠体内各种缓冲系统以及肺和肾的调节功能来实现的。机体这种处理酸碱物质的含量和比例、以维持 pH值在恒定范围内的过程称为酸碱平衡( acid-base balance)。健康机体如是,疾病过程中,机体仍要极力维持血液的pH在正常范围内。
在病理条件下,许多因素引起酸碱负荷过度、严重不足或调节机制障碍,则导致体液酸碱度稳定性破坏,称为酸碱平衡紊乱( acid-base disturbance)。在临床上许多原因可以直接导致酸碱平衡紊乱,但很多情况下,酸碱平衡紊乱是某些疾病或病理过程的继发性变化。病情一旦伴发酸碱平衡紊乱,则会更加严重和复杂,甚至严重威胁患者的生命。及时发现和正确处理酸碱平衡紊乱常常是治疗成败的关键。随着对酸碱平衡理论认识的不断深入,血气分析等诊疗技术的不断提高,酸碱平衡的判断和处理已成为临床日常诊疗的常用手段,血气检测已成为临床护理工作非常重要的一部分。
第一节 正常的酸碱平衡
一、体内酸碱的来源
在化学反应中,凡能释放出 H+的化学物质称为酸,例如 HC1、H2SO4、NH4+和 H2CO3等;凡能接受 H+的化学物质称为碱,如 OH-、SO42-、NH3、HCO3- 等。酸释放出 H+的同时,必然形成一种碱性物质;而碱接受 H+的同时,也必然形成一种酸性物质。因此,酸与其相应的碱形成一个共扼体系。例如:
H2CO3→H++HCO3-
NH4+→H++NH3
H2PO4- →H++HPO42-
HPr-H++Pr-
蛋白质( Pr - )在体液中可与H+结合成为蛋白酸( HPr) ,而且结合较牢固,所以 Pr -也是一种碱。
体内酸性或碱性物质可以来自细胞物质代谢,也可以来自外界摄入。酸性物质主要由机体代谢产生,碱性物质主要来自食物。在普通膳食条件下,酸性物质产生量远远多于碱性物质。
1.酸的来源
(1) 挥发酸(volatileacid) :机体分解代谢过程中,产生最多的酸性物质是H2CO3。体内糖、脂肪和蛋白质氧化分解的产生的CO2与水结合生成H2CO3。H2CO3可释出 H+ ,也可形成气体CO2 ,CO2从肺排出体外,所以H2CO3被称之为挥发酸。
CO2十H2O →H2CO3→H++HCO3-
CO2和 H2O结合为H2CO3的可逆反应可以自发进行,但在碳酸酐酶( carbonic anhydrase, CA)的催化作用下反应进行更迅速。CA主要存在于肾小管上皮细胞、红细胞、肺泡上皮细胞及胃黏膜上皮细胞等细胞中。静息状态下正常成人每天可产生300~400L CO2,如果这些CO2全部与 H2O结合生成H2CO3,可释出15mol左右 H+,成为体内酸性物质的主要来源。通常将肺对H2CO3(CO2)排出量的调节,称为酸碱平衡的呼吸性调节。
(2) 固定酸(fixedacid) :不能由肺呼出只能通过肾由尿排出的酸性物质,称为固定酸,又称非挥发酸(unvolatile acid) 。固定酸主要包括三大营养物质糖、脂肪和蛋白质氧化分解过程中产生的酸性物质。如蛋白质分解代谢产生的硫酸、磷酸和尿酸;无氧糖酵解产生的甘油酸、丙酮酸和乳酸;糖有氧氧化产生的三羧酸;脂肪代谢产生的β-羟丁酸和乙酰乙酸等。机体酸性物质的另一来源包括酸性食物和一些酸性药物摄取,如服用氯化铵、水杨酸等,但数量较少。一般情况下,固定酸主要来源于蛋白质的分解代谢。因此,固定酸的生成与蛋白质的摄入量成正比。正常成人每日由固定酸释出的 H+为50~ 100mmol,相比每天产生的挥发酸少很多。固定酸主要通过肾进行调节,称为酸碱平衡的肾性调节。
2. 碱的来源
体内碱性物质主要来源是食物,特别是蔬菜、瓜果中所含的有机酸盐,如柠檬酸盐、苹果酸盐和草酸盐,在代谢过程中与H+结合生成有机酸,经过三羧酸循环生成碱性盐。体内物质代谢过程中也可产生碱性物质,如氨基酸脱氨基所产生的NH3,这种氨经肝代谢后生成尿素,血中氨含量极低,对体液的酸碱度影响不大。人体在生理情况下生成碱的量与酸相比少得多(图4-1)。另外,服用一些碱性药物,如NaHCO3等也是体内碱性物质的来源之一。
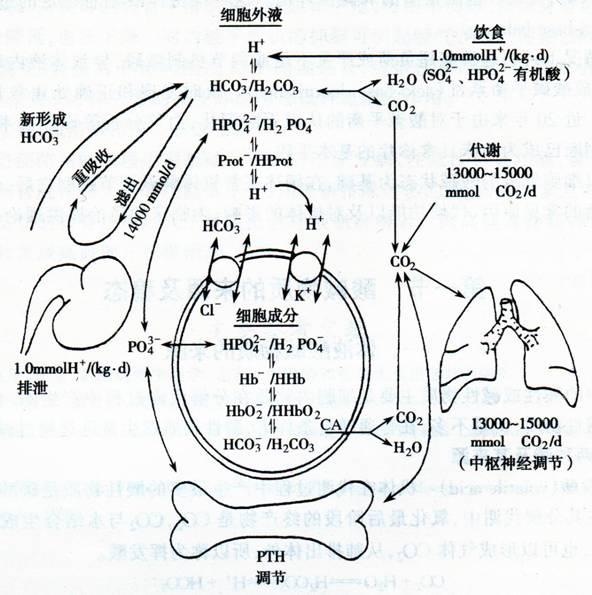
图4-1 酸碱的生成、缓冲和调节
二、酸碱平衡的调节
正常情况下机体生成酸性物质远多于碱性物质,也可因摄取碱性物质而改变二者的比例,但血液 pH却能保持在正常较窄的范围内变化。这是由于机体可以通过体液的缓冲、肺、肾和组织细胞等对酸碱负荷进行缓冲和有效调节。
(一)血液的缓冲作用
缓冲系统由弱酸(缓冲酸)及其共轭的缓冲碱组成。血液缓冲系统主要有碳酸氢盐缓冲系统、磷酸盐缓冲系统、血浆蛋白缓冲系统、血红蛋白和氧合血红蛋白缓冲系统五种。这些缓冲对的缓冲能力不同,可分为血浆缓冲系统和红细胞内缓冲系统。此外,在某些特殊情况下,其他组织也可发挥一定的缓冲作用,如骨骼对慢性代谢性酸中毒的缓冲作用。
表4-1 全血的五种缓冲系统 表4-2 全血各缓冲体系的合量与分布

当血中 H+过多时,反应向左移动,使H+的浓度不至于发生大幅度的增高,同时缓冲碱的浓度降低;当H+减少时,反应则向右移动(表4-1 ) ,使H+的浓度得到部分的恢复,同时缓冲碱的浓度增加。
例如:碳酸氢盐缓冲系统由 HCO3-/H2CO3组成,当强酸(如HCl)或强碱(如NaOH)进入血液时,可发生如下的缓冲反应:
HCl+HCO3-→Cl-+H2CO3 H2CO3→CO2十H2O
NaOH+H2CO3→NaHCO3十H2O
碳酸氢盐缓冲系统是最重要的体液缓冲系统,其特点如下:①含量最多。(表4-2 )。可以缓冲所有的固定酸,不能缓冲挥发酸;②开放性调节。能通过肺和肾对 H2CO3(CO2)和
NaHCO3进行调节。
血红蛋白和氧合血红蛋白缓冲系统主要缓冲挥发酸。
磷酸盐缓冲系统存在于细胞内外液中,主要在细胞内液(K2HPO4/KH2PO4)中发挥缓冲作用;蛋白质缓冲系统存在于血浆及细胞内,在其他缓冲对都被调动后,其作用才显示出来,平时缓冲作用不大。
(二) 组织组胞的调节作用
机体大量的组织细胞对酸碱平衡起到非常重要的调节作用。其缓冲作用主要是通过细胞内外的离子交换进行的。红细胞、肌细胞和骨细胞均能发挥这种作用。如H+-K+、H+-Na+、Na+-K+交换等。细胞外液 H+浓度过高时,H+可顺浓度梯度差弥散入细胞内,而 K+从细胞内移出,以维持细胞电中性;反之,当细胞外液 H+浓度降低时,H+从细胞内移出,K+从细胞外进入细胞内。因此酸中毒往往伴有高血钾,碱中毒时则伴有低血钾。此外,Cl--HCO3-的交换也很重要,因为 Cl-是可以自由通过细胞膜的的阴离子,当HCO3-增高时,它的排出可由 Cl--HCO3-交换来完成。
(三)肺的调节作用
肺是通过改变呼吸运动的频率和幅度,调节CO2的排出量,从而改变血浆挥发酸(H2CO3)浓度,使血浆中HC03-与 H2CO3比值接近20:1,来保持pH相对恒定,在酸碱平衡的调节中发挥作用的。
呼吸运动的调节分为中枢调节和外周调节两方面。①呼吸运动的中枢调节:延髓呼吸中枢可以调控肺泡通气量。呼吸中枢可接受来自中枢化学感受器和外周化学感受器的刺激。呼吸中枢化学感受器可感受脑脊液和局部细胞外液中H+浓度变化,H+浓度升高可刺激呼吸中枢兴奋,使呼吸运动加深加快,增加CO2的排出量。但是,血液中的 H+不易通过血脑屏障对中枢化学感受器发挥直接作用,而血液中CO2作为脂溶性物质能迅速通过血脑屏障,使化学感受器周围H+浓度升高,pH降低,从而使呼吸中枢兴奋,反射性地使呼吸加深、加快,增加肺泡通气量,使CO2排出增多,从而降低 PaCO2和血浆中 H2CO3浓度。反之,当 PaCO2降低时,中枢化学感受器的兴奋性降低,出现呼吸变浅、变慢甚至出现呼吸暂停,CO2排出减少,则使 PaCO2和血浆中 H2CO3浓度出现一定程度的增高。中枢化学感受器对不同 PaCO2的反应性是不同的。PaCO2的正常值为40mmHg,PaCO2只需升高2mmHg,就可刺激中枢化学感受器,出现肺通气增强,从而降低血中H2CO3浓度,实现反馈调节。但如果 PaCO2过高超过80mmHg以上时,呼吸中枢反而受到抑制,产生 CO2麻醉(carbon dioxide narcosis)。②呼吸运动的外周调节:呼吸中枢还能接受外周化学感受器的刺激而兴奋,外周化学感受器包括主动脉体和颈动脉体感受器,尤其是颈动脉体对缺氧、pH和PaCO2的改变敏感。当 PaO2降低、pH降低或 PaCO2升高时,可以刺激外周化学感受器使呼吸中枢兴奋,引起呼吸加深、加快,使CO2排出增多,血浆 H2CO3 浓度降低。PaO2降低对呼吸中枢的直接作用是抑制效应,外周化学感受器对PaO2的改变较为敏感,缺氧能够刺激外周化学感受器,间接引起呼吸中枢兴奋,使通气量增加,增加 CO2排出量。当 PaO2<60mmHg时可反射性兴奋呼吸中枢,使呼吸加深加快;但PaO2过低对呼吸中枢的直接效应则是抑制,从而使PaCO2和血浆中H2CO3浓度增高。
(四)肾的调节作用
肾主要通过排出机体代谢过程中产生的酸性或碱性物质,来调节血浆中NaHCO3含量,使血浆pH保持在正常范围内。普通膳食条件下机体代谢产生酸的量远多于碱的量,因此肾脏主要通过调节固定酸发挥调节酸碱平衡的作用。机体代谢过程中产生的大量酸性物质不断消耗NaHCO3和其他碱性物质,如果不能及时补充碱性物质和排出多余的H+,血液 pH值就会发生变动。NaHCO3可自由通过肾小球,因此肾小球滤液中NaHCO3含量与血浆相等,其中85%~90%的NaHCO3在近曲小管被重吸收,剩余部分在远曲小管和集合管被重吸收(图4-2) 。正常情况下,随尿液排出体外的NaHCO3仅为滤出的0.1%,几乎无NaHCO3的丢失。所以,尿液常呈酸性,pH一般在6.0左右,但在酸碱失衡时,pH可在4.4~8.0之间波动,其间H+浓度相差有1000倍。由此可见,肾脏对酸碱的调节能力非常强大,主要机制如下:
1. 近曲小管泌H+和对HCO3-的重吸收 近曲小管上皮细胞泌H+和重吸收HCO3- 的方式是H+-Na+交换。机制:①近曲小管上皮细胞内含有大量的CA,能催化 CO2与 H2O结合生成H2CO3 ,而H2CO3可解离出 H+和HCO3-;②肾小球滤液中的 NaHCO3在近曲小管管腔内解离为 Na+和HCO3- ,Na+可顺电化学梯度被重吸收进入肾小管上皮细胞内,同时通过 H+-Na+交換体将细胞内H2CO3解离产生的 H+分泌到管腔中,其能量来源于基侧膜的 Na+-K+-ATP酶;③H+分泌入肾小管管腔后,与管腔内的 HCO3-结合生成H2CO3。H2CO3在刷状缘 CA的作用下被分解为 CO2和H2O。H2O随尿液排出,CO2由于其脂溶性,可迅速通过细胞膜弥散进人肾小管上皮细胞内,在细胞内CA的作用下再与 H2O结合生成H2CO3;④经 H+-Na+交换进入小管上皮细胞内的 Na+在小管上皮细胞内与细胞内重吸收的 HCO3-同向转运进入血液循环,实现 NaHCO3的重吸收(图4-2左)。以上4个步骤是一个连续的过程,完成了一次近曲小管上皮细胞泌 H+和重吸收 HCO3-的循环。酸中毒越严重,CA的活性越强,H+-Na+交换也增强,肾的泌氢保碱作用也越强。
2. 远曲小管及集合管泌 H+和对HCO3-的重吸收 远曲小管和集合管泌氢是小管上皮闰细胞内H+-ATP酶主动泌氢的过程。该闰细胞又称为泌氢细胞,它不能转运 Na+,是一种非Na+依赖性的泌氢。在远曲小管和集合管部位借助于 H+-ATP酶的作用向管腔泌氢,同时在基侧膜以 Cl--HCO3-交换的方式重吸收HCO3-使尿液酸化,称为远端酸化作用(distal acidification)(图4-2右)。当肾小球滤液中NaHCO3重吸收后,仍不能满足细胞外液NaHCO3浓度,就要增加尿中可滴定酸的生成。刚从肾小球滤出的滤液中可滴定酸Na2HPO4与NaH2PO4的比例为4:1,原尿的pH为7.4,与血浆相同。管腔滤液流经远曲小管和集合管时,不断接受泌氢细胞的泌 H+,碱性盐 Na2HPO4结合H+形成酸性盐NaH2PO4,使尿液不断酸化。但是通过磷酸盐缓冲增强泌酸是有限的,当尿液 pH降至4. 8左右时,两者比值由原来的4 : 1变为1 :99 ,几乎尿液中所有碱性盐都已转变为酸性盐,已不能进一步发挥缓冲作用了。

图4-2 近曲小管和集合管泌H+、重吸收 HCO3-过程示意图
O:表示主动转运; ●:表示继发性主动转运
3. 产NH3和铵盐(NH4+)的排出 正常情况下,NH4+的排泄速率为20~40mmol/d,当尿液pH稍有下降,肾小管上皮细胞则分泌NH3来阻止尿液pH的下降,因此NH4+的生成和排出是pH依赖性的,且机体酸中毒程度越严重,尿NH4+排出量越多,甚至能增加到10倍以上。近曲小管上皮细胞是产 NH3的主要场所,主要由谷氨酰胺酶水解谷氨酰胺产生,酸中毒时,谷氨酰胺酶活性增强,以下反应加速进行。谷氨酰胺在谷氨酰胺酶作用下水解产生氨(NH3)和谷氨酸,谷氨酸脱NH3生成α-酮成二酸,后者进一步代谢生成HCO3-。酸中毒越严重,谷氨酰胺酶活性越高,产生NH3和HCO3- 越多。HCO3-与Na+同向转运进入血循环。在近曲小管NH3与细胞内碳酸解离的H+结合成NH4+,通过NH4+-Na+交换进入肾小管管腔,随尿排出。NH3是脂溶性,远曲小管和集合管泌NH3,可通过小管上皮细胞膜自由扩散进入小管腔,和尿液中H+结合成NH4+,从尿中排泄(图4-3) ;也可通过基侧膜进入细胞间隙。酸中毒严重时,远曲小管和集合管磷酸盐缓冲系统不能缓冲时,不仅近曲小管泌NH4+增加,远曲小管和集合管泌NH3也增加,弥散至管腔与H+结合成NH4+,随尿排出体外。管腔中NH4+的不断形成维持了管腔内外H+的浓度梯度,促进H+的持续分泌,是机体在严重酸中毒情况下排H+的补充过程。
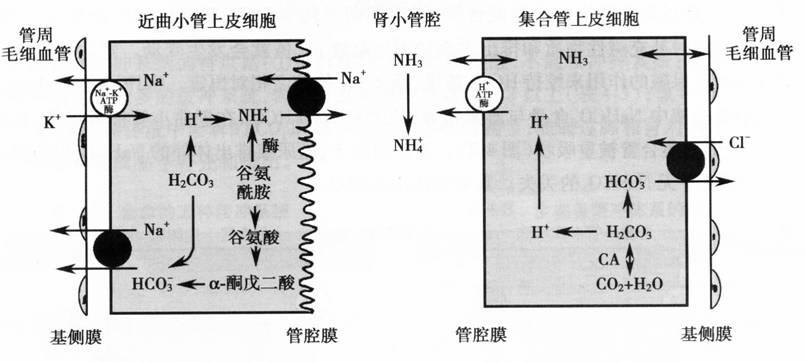
图4-3 尿中铵盐(NH4+)的排出
综上所述,肾对酸碱平衡的调节主要是通过肾小管上皮细胞的活动来实现的。肾小管上皮细胞在不断分泌 H+的同时,将HCO3-重吸收入血,维持机体NaHCO3浓度的稳定。
此外,肝可以通过合成尿素清除 NH3调节酸碱平衡;慢性酸中毒时,骨骼的钙盐溶解有利于对H+的缓冲,如: Ca3 ( PO4) 2 +4 H+→3Ca2++2H2PO4-。
机体通过以上四方面因素共同调节维持酸碱平衡状态,但各因素在作用时间和作用强度上是有差别的。血液缓冲系统反应最为迅速,一旦有酸性或碱性物质入血,缓冲物质就立即与其反应,将强酸或强碱中和转变成弱酸或弱碱,缓冲系统自身被消耗,故缓冲作用不能持久;肺的调节作用效能最大,也很迅速,在几分钟内开始,30分钟时达最高峰,通过改变肺泡通气来控制血浆H2CO3浓度的高低。但呼吸过深过快会增加耗氧,过浅过慢又会导致缺氧,因此肺的呼吸调节难以持久,仅在急性酸碱平衡紊乱时起呼吸代偿作用,且肺仅对挥发酸有调节作用,不能缓冲固定酸;细胞的缓冲作用也较强,但约3~4小时后才发挥调节作用,酸碱平衡调节是通过细胞内外离子的转移来维持,可引起血钾浓度的改变;肾的调节作用发挥较慢,常在数小时后起效,3~5天达高峰,肾的调节作用持久,通过排出固定酸及保留NaH CO3起重要作用。机体对酸碱度的调节是有限度的,如果机体的酸碱变化超过了机体的调节能力,或者调节机制某一方面出现了问题,机体的酸碱平衡状态就会改变。
第二节反映酸碱平衡的常用指标及意义
一、pH
pH是表示溶液酸碱度的指标。由于血液中 H+很少,因此常用 H+浓度的负对数即 pH 来表示,动脉血pH受血液缓冲对的影响,特别是H2CO3及 HCO3- 的影响。根据 Henderson-Hasselbalch 方程式:pH= pKa+log [HCO3-]/[ H2CO3 ]
H2CO3由 CO2溶解量(d CO2 )决定,而 dCO2=溶解度(α)×PaCO2 (Henry定律)
所以上述公式可改写为:
pH = pKa+log[HCO3- ]/α×Pa CO2 (α为溶解度=0.03 )
=6. 1+log24/0.03×40=6. 1+log24/1.2 =7.4
以上公式反映了pH、HCO3-和PaCO2三者的相互关系。可以看出,血液pH的变化取决于血液中[HCO3-]/[H2CO3 ]比值。
血气分析仪可直接用 pH和CO2电极测出pH或[H+]及PaCO2,并根据Henderson_ Hasselbalch方程式计算出HCO3-的量。
通常将[HCO3- ]看成是代谢性的,将[H2CO3]看成是呼吸性的。血液pH的变化可以由代谢性因素引起也可以由呼吸性因素引起。正常人动脉血 pH范围为7.35~7. 45,平均值是7. 40 。当测得患者血液pH值降低或增高时,可以判断是酸中毒或是碱中毒,凡 pH低于7. 35为酸中毒,凡 pH高于7. 45为碱中毒。但并不能区别是呼吸因素还是代谢因素所致。如果pH值在正常范围内,机体可能处于酸碱平衡状态,也可能处于代偿性酸中毒或碱中毒状态,或同时存在程度相近的混合型酸、碱中毒,使 pH变动相互抵消,因此pH值在判断酸碱平衡紊乱上有局限性,必须借助其他一些指标来区分酸碱平衡紊乱及其类型,是呼吸性的还是代谢性的。

图4-4 Henderson-Hasselbalch方程式与 pH值的关系
二、动脉血二氧化碳分压
动脉血二氧化碳分压 (arterial partial pressureof CO2, PaCO2)是指动脉血中呈物理溶解状态的CO2分子产生的张力。由于 CO2通过呼吸膜弥散快,动脉血 CO2分压相当于肺泡气 CO2分压( PACO2) ,因此测定PaCO2可反应肺泡通气量的情况。PaCO2与肺泡通气量成反比,通气不足,PaCO2升高,通气过度,PaCO2降低,所以 PaCO2是反映呼吸性酸碱平衡紊乱的重要指标,其变动直接影响着血浆呼吸性因素[H2CO3]浓度的高低。根据Henderson-Hasselbalch 方程式,原发性的PaCO2升高引起的pH降低称为呼吸性酸中毒;原发性的PaCO2降低引起的pH升高称为呼吸性碱中毒。PaCO2正常值为33 ~ 46mmHg,平均值为40mmHg。 PaCO2 <33mmHg,表示肺通气过度,CO2排出过多,见于呼吸性碱中毒或代偿后的代谢性酸中毒;PaCO2>46mmHg,表示肺通气不足,有CO2在体内潴留,见于呼吸性酸中毒或代偿后代谢性碱中毒。
三、实际碳酸氢盐和标准碳酸氢盐
标准碳酸氢盐(standard bicarbonate,SB)是指全血在标准条件下,即 PaCO2为40mmHg、温度38℃、血红蛋白氧饱和度为100%测得的血浆中HCO3-的含量。由于标准化后HCO3-不受呼吸因素的影响,因此是判断代谢因素的指标。SB正常范围是22 ~27mmoL/L,平均为24mmol/L。SB在代谢性酸中毒时降低,在代谢性碱中毒时升高。
实际碳酸氢盐( actual bicarbonate,AB)是指隔绝空气的血液标本,在实际 PaCO2、实际体温和血氧饱和度条件下测得的血浆HCO3-浓度。因此AB受呼吸和代谢两方面因素的影响。正常人AB与 SB相等。两者数值均低表明有代谢性酸中毒;两者数值均高表明有代谢性碱中毒;AB与 SB不相等时表明呼吸因素对酸碱平衡有影响。若 SB正常,而 AB>SB时,表明有CO2滞留,可见于呼吸性酸中毒;反之AB< SB,则表明CO2排出过多,见于呼吸性碱中毒。SB在慢性呼吸性酸碱中毒时,由于有肾脏代偿, 也可发生继发性升高或降低。
四、缓冲碱
缓冲碱(buffer base,BB)是指血液中一切具有缓冲作用的负离子碱的总和。包括血浆和红细胞中碳酸氢盐和非碳酸氢盐缓冲系统中的负离子,如HCO3-、Hb-、HbO2- 、Pr-和 HPO42- 等。通常以氧饱和的全血在标准状态下即 PaCO2为40mmHg、温度38℃、血红蛋白氧饱和度为100%时测定。正常值为45 ~ 51mmol/L (平均值48 mmol/L)。虽然缓冲碱中HCO3-受PaCO2影响,但负离子总和基本不受呼吸性因素的影响,因此也是反映代谢因素的指标。BB减少常见于代谢性酸中毒,BB升高常见于代谢性碱中毒。
五、碱剩余
碱剩余( base excess,BE)是指标准条件下即PaCO2为40mmHg、温度38℃、血红蛋白氧饱和度为100%,在体外用酸或碱滴定全血标本至pH7.40时所需的酸或碱的量(mmol/L) 。此指标排除了呼吸因素的影响,是反映代谢因素的指标,既包括了HCO3-,也包括了非碳酸氢盐缓冲碱。
全血 BE正常值范围为-3.0~+3.0mmoL/L,常用正值增大或负值增大来表示。若用酸滴定,使血液 pH达7.40,表明患者血液中碱剩余高于正常,BE正值增大;如需用碱滴定,才使血液 pH达7.40,表明患者血液中碱剩余低于正常,被测血液的碱缺失,BE用负值来表示。
BE负值增大见于代谢性酸中毒;BE正值增大见于代谢性碱中毒。
BE也可由全血 BB和 BB正常值(NBB)算出:BE=BB-NBB=BB-48。
以上各指标均可通过血气分析仪测得。
六、阴离子间隙
阴离子间隙( anion gap,AG)是指血浆中未测定的阴离子( undetermined anion, UA)与未测定的阳离子( undetermined cation, UC)的差值,即AG=UA-UC。正常机体血浆中的阳离子与阴离子总量相等,从而维持电中性。临床实际测定时,常规测定的阳离子Na+占血浆阳离子总量的90%,称为可测定阳离子。常规测定的阴离子HCO3- 和 Cl-占血浆阴离子总量的85% ,称为可测定阴离子。血浆中未测定的阳离子UC包括 K+、Ca2+和 Mg2+。血浆中未测定的阴离子UA包括 Pr-、HPO4-、SO42-和有机酸阴离子等。
AG可用血浆中常规测定的阳离子与常规测定的阴离子的差算出,即:
Na++UC= HCO3-+C1-+UA
AG=UA-UC=Na+-(HCO3-+Cl-)=140-(24+104)=12mmoL/L,正常范围是10~14mmoL/L(图4-5)

图4-5血浆阴离子间隙图解(单位mmol/L)
AG不是血气分析仪测出的指标,但它在区分代谢性酸中毒的类型和诊断混合型酸碱平衡紊乱中具有非常重要的作用。AG可增高也可降低,但增高的意义较大。
通常AG>16mmol/L,结合病因作为判断是否有 AG增高代谢性酸中毒的界限。AG增高多见于固定酸增多:如乳酸堆积、酮体增多及水杨酸中毒、甲醇中毒等。AG增高还可见于混合性酸碱失衡,如:代谢性酸中毒合并代谢性碱中毒,三重酸碱失衡以及与代谢性酸中毒无关的情况,如脱水、钠盐药物摄入过多和骨髓瘤病人释出本周氏蛋白过多等情况。
AG降低在诊断酸碱失衡方面意义不大,仅见于未测定阴离子减少或未测定阳离子增多,如低蛋白血症等。
第三节单纯型酸碱平衡紊乱
单纯型酸碱平衡紊乱分为四种类型:代谢性酸中毒、代谢性碱中毒、呼吸性酸中毒和呼吸性碱中毒。
一、代谢性酸中毒
代谢性酸中毒( metabolic acidosis)是指血浆HCO3- 原发性减少引起pH下降的酸碱平衡紊乱。是临床上最常见的酸碱平衡紊乱类型。
(一)原因和机制
1.酸负荷增多 主要见于固定酸过多。
(1)外源性固定酸摄入过多,HCO3-缓冲消耗。①水杨酸中毒:大量摄入阿司匹林(乙酰水杨酸)可引起酸中毒,经缓冲HCO3-浓度下降,水杨酸根潴留;②含氯酸性药物摄入过多:长期或大量服用含氯的盐类药物,如氯化铵、盐酸精氨酸等,在体内易解离出HCl。如氯化铵,经肝合成尿素,并释放出HCl,反应式如下:2NH4Cl+CO2→ (NH2)2CO+2HCl+H2O。引起血氯增高型代谢性酸中毒。
(2)体内固定酸产生过多 ①乳酸酸中毒( lactic acidosis):任何原因引起的缺氧都可以使细胞内糖的无氧酵解增强而引起乳酸生成增加,产生乳酸性酸中毒。常见于休克、心搏骤停、低氧血症、严重贫血、肺水肿、一氧化碳中毒和心力衰竭等。乳酸代谢在肝脏中进行,严重肝病使乳酸利用障碍也可引起血浆乳酸过高。②酮症酸中毒( keto-acidosis):见于体内脂肪被大量动员的情况下,多发生于糖尿病、严重饥饿和酒精中毒。糖尿病时由于胰岛素不足,葡萄糖利用减少,脂肪分解加速,使大量脂肪酸进入肝,形成过多的酮体(其中β-羟丁酸和乙酰乙酸为酸性物质),超过了外周组织的氧化能力及肾排出能力时可发生酮症酸中毒。在严重饥饿或禁食情况下,当体内糖原消耗后,大量动用脂肪供能,也可出现酮症酸中毒。
(3)酸性物质排出过少 ①肾衰竭:在严重肾功能衰竭患者,GFR严重降低,体内固定酸不能由尿中排泄,特别是硫酸和磷酸在体内积蓄,H+浓度增加导致HCO3-浓度降低,硫酸根和磷酸根浓度在血中增加,引起AG增高型代谢性酸中毒;②肾小管功能障碍:I型肾小管性酸中毒(renal tubular acidosis-I,RTA-I)的发病环节是由于远曲小管集合管的泌H+功能障碍,H+在体内蓄积,导致血浆HCO3- 浓度进行性下降。肾小管酸中毒常引起AG正常(血氯增高型)代谢性酸中毒。
2. HCO3-丢失过多 主要见于碱性消化液丢失及肾脏重吸收HCO3-减少。
(1)HCO3-经消化道直接丢失。胰液、肠液和胆液中碳酸氢盐含量均高于血浆,严重腹泻、肠道瘘管或肠道引流等均可引起HCO3-大量丢失。
(2)肾脏重吸收HCO3-减少 ①II型肾小管性酸中毒( renal tubular acidosis-II, RTA-II ):由于近曲小管 Na+-H+转运体功能障碍,导致近曲小管泌H+障碍和HCO3-在近曲小管重吸收减少,血浆HCO3-浓度降低,尿中排出较多的HCO3-,引起“反常性碱性尿”。 由于HCO3-的重吸收减少出现Cl-重吸收增加,血Cl-增高,因此RTA-II常引起AG正常(血氯增高型)代谢性酸中毒;②应用碳酸酐酶抑制剂:大量使用碳酸酐酶抑制剂如乙酰唑胺可抑制肾小管上皮细胞内CA活性,使H2CO3生成减少,泌H+和重吸收HCO3-减少。
肾功能障碍是导致代谢性酸中毒非常重要的原因,既可以影响到固定酸的排出,导致血浆酸负荷增多而消耗HCO3-,也可直接影响到HCO3-重吸收,导致血浆HCO3-浓度降低。一般的代谢性酸中毒,肾脏功能正常时可通过增强泌H+泌NH4+使尿液酸化,保持血液的pH正常。但是肾小管性酸中毒时HCO3-生成和重吸收障碍,导致HCO3-从尿中排出增多,尿液呈中性或碱性。
3.高K+血症 各种原因引起细胞外液 K+增多时,K+与细胞内 H+交换,引起细胞外 H+增加,导致代谢性酸中毒。这种酸中毒时体内 H+总量并未增加,仅有H+从细胞内逸出,造成细胞内 H+下降,故细胞内呈碱中毒。在远曲小管处由于小管细胞内H+下降,小管细胞泌H+减少,也可引起“反常性碱性尿”。
4. 血液稀释 见于快速输入大量无HCO3-的液体如葡萄糖或生理盐水,使血液中HCO3-稀释,HCO3-浓度下降,造成稀释性代谢性酸中毒。
(二)分类
根据 AG 值的不同,将代谢性酸中毒分为两类: AG増高型代谢性酸中毒和AG正常血Cl-增高型代谢性酸中毒。
1. AG正常型代谢性酸中毒 其特点是AG正常,血Cl-升高。这类酸中毒发生主要由各种原因导致的HCO3-丢失及肾脏重吸收HCO3-减少。其特点为血浆HCO3-浓度降低,细胞内Cl-移出细胞,血Cl-代偿性升高,呈血氯增高型代谢性酸中毒(图4-6B) 。常见于消化道直接丢失HCO3-,轻度或中度肾功能衰竭泌 H+减少,RTA时HCO3-重吸收减少或泌 H+障碍,使用碳酸酐酶抑制剂,高钾血症、含氯的酸性盐摄入过多和稀释性代谢性酸中毒等。
2. AG増高型代谢性酸中毒 其特点是AG增高,血Cl-正常。除了含Cl-以外的其它任何固定酸的血浆浓度增高的代谢性酸中毒都属于AG増高型代谢性酸中毒。这类酸中毒发生机制主要由固定酸产生或摄入过多、排出障碍造成。这部分固定酸根属于未测定阴离子,所以 AG值增大,而Cl-值正常,故又称血氯正常型代谢性酸中毒(图4-6C) 。如水杨酸中毒、乳酸酸中毒、酮症酸中毒、磷酸和硫酸排泄障碍等。其固定酸的H+被HCO3-缓冲,其酸根(水杨酸根、乳酸根、β-羟丁酸根、乙酰乙酸根、H2PO4-、SO42-)增高。

图4-6 正常和代谢性酸中毒时阴离子间隙
A.正常情况下AG; B.AG正常型(血氯增高)代谢性酸中毒; C. AG增高型(血氯正常)代谢性酸中毒
(三)机体的代偿调节
1.血液的缓冲 代谢性酸中毒时,血液中增多的H+立即被血浆缓冲系统进行缓冲,结果HCO3-及其他缓冲碱不断被消耗。
2.细胞内缓冲 细胞内的缓冲多在酸中毒2~4小时后,约1/2的 H+通过离子交换方式进入细胞内,被细胞内液缓冲系统缓冲。为维持细胞内外电荷平衡K+移向细胞外液,结果造成血K+增高。
3.肺的代偿调节 代谢性酸中毒时血液H+浓度增加可通过剌激颈动脉体和主动脉体外周化学感受器,反射性地引起呼吸中枢兴奋,使呼吸加深加快,增加肺的通气量。肺的代偿意义是使CO2排出增多,降低血浆H2CO3浓度,有利于维持 [HCO3- ]/[ H2CO3 ]的比值,使血液 pH趋向正常。代谢性酸中毒当pH由7.4降到7.0时,肺泡通气量可由正常的4L/min增加到30L/min以上。呼吸加深加快是代谢性酸中毒的主要临床表现。肺的代偿调节非常迅速,一般在酸中毒数分钟后就出现呼吸加深加快,30分钟后即达代偿,12 ~24小时达代偿高峰,代偿最大极限时,Pa CO2可降到10mmHg。
4.肾的代偿调节 除肾功能障碍引起的代谢性酸中毒外,其他原因引起的代谢性酸中毒可以通过肾的排酸保碱能力加强来发挥代偿作用。代谢性酸中毒时,肾脏通过增强其泌H+、产NH3、泌NH4+及重吸收HCO3-,使HCO3-在细胞外液的浓度有所恢复,pH得到一定代偿。且代谢性酸中毒时肾小管上皮细胞中的碳酸酐酶和谷氨酰胺酶活性增强,使HCO3-生成和谷氨酰胺的分解增强,尿中可滴定酸和NH4+排出增加。严重代谢性酸中毒时肾小管产NH3增加是最主要的代偿机制,因为H+-Na+交换增加,肾小管腔内H+浓度增加,降低了肾小管上皮细胞与管腔液H+的浓度差,使肾小管上皮细胞继续排H+受限。但管腔内H+浓度越高,NH3的生成与排出越快,产生的HCO3-越多。通过以上反应,肾脏排酸保碱能力增强,由于从尿中排出的H+和NH4+增多,因此尿液呈酸性。肾的代偿作用较慢,一般要3 ~5天才能达高峰。
血气指标的变化特点如下:
由于HCO3-降低,所以 AB、SB、BB值均降低,BE负值增大,pH值下降,通过呼吸代偿,PaCO2继发性下降,AB<SB。
(四)对机体的影响
代谢性酸中毒主要引起心血管系统、中枢神经系统功能障碍以及呼吸的代偿性增强,慢性代谢性酸中毒还会对骨骼系统产生影响。
1.心血管系统改变 严重的代谢性酸中毒能导致心肌收缩力降低、产生致死性室性心律失常、使血管对儿茶酚胺的反应性降低。
(1)心肌收缩力降低:轻度酸中毒可引起肾上腺髓质释放肾上腺素,发挥其对心脏的正性肌力作用, 但严重酸中毒pH小于7. 2时,肾上腺素的正性肌力作用被阻断,出现心肌收缩力减弱,心输出量减少。Ca2+是心肌的兴奋-收缩耦联因子,酸中毒引起心肌收缩力降低的机制主要与H+和Ca2+竞争有关,相关机制如下:①H+影响Ca2+内流;②H+影响心肌细胞肌浆网释放Ca2+;③H+增多可竞争性抑制 Ca2+与心肌肌钙蛋白亚单位结合,从而抑制心肌的兴奋-收缩耦联,降低心肌收缩性。
(2)心律失常:代谢性酸中毒时出现的心律失常与血钾升高密切相关。酸中毒时细胞外 H+进入细胞内与 K+交換,K+逸出细胞,另外酸中毒时肾小管上皮细胞泌 H+增加,而排K+减少,这两方面因素共同导致血钾升高。重度高血钾可导致严重的传导阻滞和心室纤颤,心肌兴奋性消失,可造成致死性心律失常和心跳停止。
(3)血管系统对儿茶酚胺的反应性降低:酸中毒时H+增多,可降低外周血管对儿茶酚胺的反应性,使血管扩张,血压下降。尤其是毛细血管前括约肌最为明显,血管扩张使血管床容积不断扩大,回心血量减少,甚至发生休克。因此休克时首先需要纠正酸中毒,才能减轻血流动力学的障碍,不然会导致休克加重。
2. 中枢神经系统改变:中枢神经系统的代谢障碍主要表现为意识障碍、乏力、知觉迟钝,甚至嗜睡或昏迷,最后可因呼吸中枢和血管运动中枢麻痹而死亡。其发生机制有:
(1)酸中毒时生物氧化酶类的活性受到抑制,氧化磷酸化过程减弱,致使ATP生成减少,因而脑组织能量供应不足。
(2)pH值降低时,脑组织内谷氨酸脱羧酶活性增强,使γ-氨基丁酸增多,后者对中枢神经系统具有抑制作用。
3. 呼吸的代偿 代谢性酸中毒时由于血浆HCO3-浓度下降,机体通过呼吸加深加快增加CO2的排出量,降低血浆H2CO3浓度,保持pH相对恒定。
4. 骨骼系统改变 慢性肾功能衰竭出现酸中毒时,骨骼释放钙盐以进行缓冲,造成骨质脱钙,在小儿可表现为骨骼发育、生长延迟,严重者表现为肾性佝偻病。在成人则可导致骨软化症和纤维性骨炎。
(五)防治与护理的病理生理学基础
1.预防和治疗原发病 去除引起代谢性酸中毒的发病原因、治疗原发病,是治疗代谢性酸中毒的病因学防治原则。要结合患者的临床表现和血气分析的结果及时分析处理。
2. 碱性药物的应用 对代谢性酸中毒患者主要的处理措施是补充碱性药物。补碱的剂量和方法应根据酸中毒的严重程度区别对待。一般轻度代谢性酸中毒HCO3- >16mmol/L时,可以少补,甚至不补,因为肾有排酸保碱的能力,约有50%的酸要靠非碳酸氢盐缓冲系统来调节。严重的代谢性酸中毒病人需静脉滴注碱性药物治疗,一般主张在血气监护下分次补碱,补碱量宜小不宜大。如果病人的原发病因是由于HCO3- 减少,首选的碱性药物是碳酸氢钠,因其可直接补充血浆缓冲碱,作用迅速,为临床治疗所常用。其他碱性药物如乳酸钠等也是常用来治疗代谢性酸中毒的药物,通过肝可转化为HCO3-。但乳酸钠与H+结合变为乳酸,所以肝功能不全或乳酸酸中毒时不宜使用。三羟甲基氨基甲烷(tromethamine,THAM)是不含钠的有机胺碱性药,可避免NaHCO3和乳酸钠使用导致的血钠升高。在体内的作用是 THAM+H2CO3→THAM·H++ HCO3- ,由上式可见 THAM不仅可缓冲挥发酸,而且在中和H2CO3后可产生HCO3-。所以此药既可以治疗呼吸性酸中毒又可以治疗代谢性酸中毒。缺点是对呼吸中枢有抑制作用,故治疗时要注意输入的速度。
3. 防止药物外渗 碱性药物外渗,可引起剧烈疼痛,严重时可致组织坏死。
4. 纠正水和电解质紊乱 代谢性酸中毒患者容易出现K+和Ca2+代谢障碍。如严重腹泻造成的酸中毒时由于细胞内 K+外流,往往掩盖了低血钾,补碱纠正酸中毒后,K+又返回细胞内,可明显地出现低血钾。血钾异常常影响心律失常的发生,因此要密切注意心电监护;酸中毒时游离钙增多,酸中毒纠正后,游离钙明显减少,有时可出现手足搐搦,因为 Ca2+与血浆蛋白在碱性条件下可生成结合钙,使游离钙减少,而在酸性条件下,结合钙又可离解为 Ca2+与血浆蛋白,使游离钙增多。因此代谢性酸中毒患者在及时纠酸的同时也要纠正水和电解质紊乱,恢复有效循环血量以及改善肾功能。
5. 注意观察中枢神经系统等功能障碍 代谢性酸中毒易引起中枢神经抑制,进而影响呼吸和血管运动中枢,故应密切注意患者的神志、呼吸及血压变化,及时使用床栏或加强陪护,避免意外伤害发生。


