物质的量及其计算
-
1 物质的量及其计算
-
2
上一节
下一节
物质的量
 物质的量是表示物质所含微粒多少的物理量。
物质的量是表示物质所含微粒多少的物理量。
【注意】
①物质的量是专用名词,四个字是一个整体,不能分割,也不可加字、减字。
②物质的量实际上表示含有一定数目的集体。用n表示物质的量。
有关物质的量的计算
(1)n=(m/M)=(V/Vm)=(N/NA)=(c×V)
(2)有关物理量之间的相互关系建立物质的量的好处在于: ① 它反映了化学反应的实质; 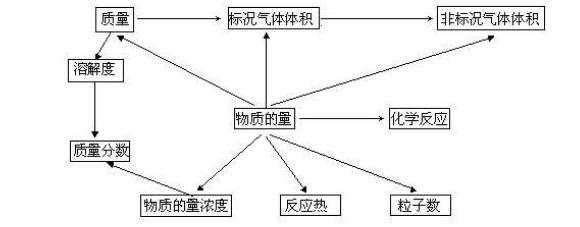
② 它把看不见的、不可量度的粒子数(微观量)和看得见的、可量度的质量或体积(宏观量)联系起来了;
③ 它把气体的体积和分子数联系起来了;
④ 可以建立以物质的量为中心的,联系其它各种物理量的一个完整的化学计算体系;
⑤ 由于化学方程式中各物质的化学计量数之比既是粒子数比,又是物质的量之比,也是相同条件下气体的体积比。这种比值较相应的质量比简单,因此,用物质的量的关系进行计算就比较简捷。



