中和热的测定实验
-
1 中和热的测定实验
-
2
上一节
下一节
测定实验
原理:
在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O的反应热。
装置:
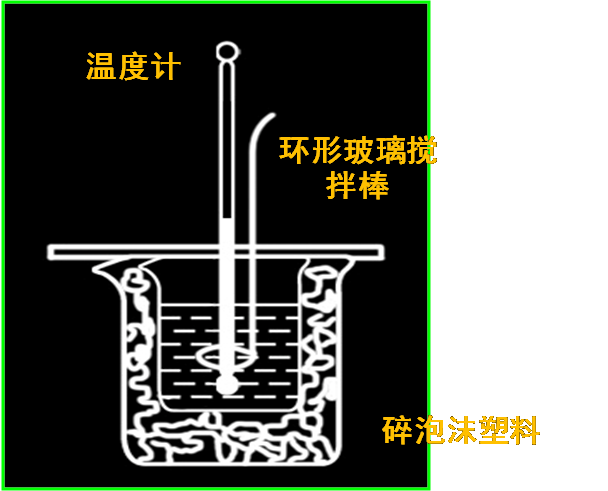
步骤:
在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,如下图所示。
2.用一个量筒量取50 mL 0.50 mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。
用另一个量筒量取50 mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
重复实验两次,取测量所得数据的平均值作为计算依据。
计算
中和热测定重要说明
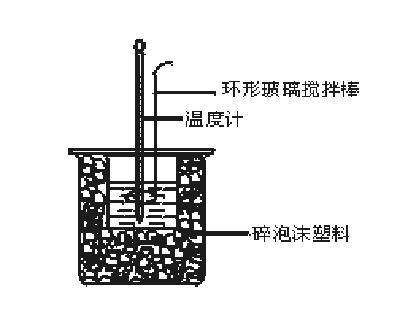 (1)大小烧杯间填满碎泡沫塑料,大烧杯上盖泡沫塑料板,目的是达到保温、隔热、减少实验过程中热量损失。
(1)大小烧杯间填满碎泡沫塑料,大烧杯上盖泡沫塑料板,目的是达到保温、隔热、减少实验过程中热量损失。
(2)环形玻璃搅拌棒使用方法:上下或轻轻搅动。
(3)酸溶液或碱溶液有一种要稍过量,以便反应更充分。
(4)初温度为两溶液混合前温度的平均值,终止温度为混合后的最高温度。
(5)实验共三次取平均值作为计算依据。
(6)Q=mc△t



