请你思考
从氮的原子结构和在周期表中的位置看,氮元素应具有较强的氧化性,氮单质也应是较活泼的非金属单质,为什么空气中的氮气却如此稳定?
1、氮原子结构

结论:氮较易得到3e-达到8e-稳定结构,显示出较强的氧化性。
![]()
由于N≡N键很牢固、分子结构稳定,性质稳定
自然界里氮主要以游离态存在于大气中,
其体积分数为78%,质量分数为75%,通常情况下氮气不与其它物质反应,有时还能替代稀有气体,作保护剂。
请你思考
农业生产中有这样一句谚语:“雷雨发庄稼”,你知道它的科学道理吗?
2、氮及氧化物的重要转化关系
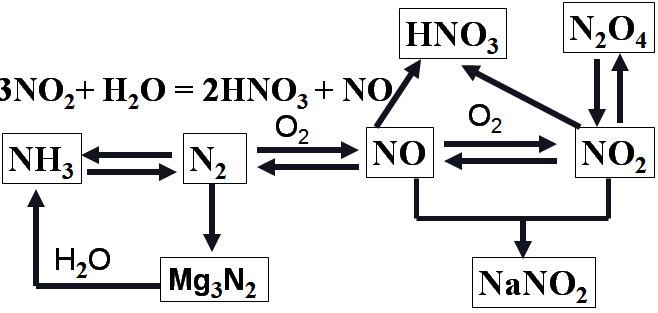
3、O2及NOx的混合物溶于水的计算
(1)NO2(NO2+N2、NO2+NO)溶于水
3NO2+H2O = 2HNO3+NO 常用方法:差量法
讨论1:标况下,一充满NO2的试管倒立水中,液面上升,假设试管中溶液不扩散,求试管中硝酸溶液的物质的量浓度。(1/22.4mol•L-1)
(2) NO和O2的混合物溶于水 2NO+O2=2NO2 ……① 3NO2+H2O = 2HNO3+NO ……②
①×3+ ② ×2得到总的反应方程式为:总式: 4NO+3O2+2H2O=4HNO3
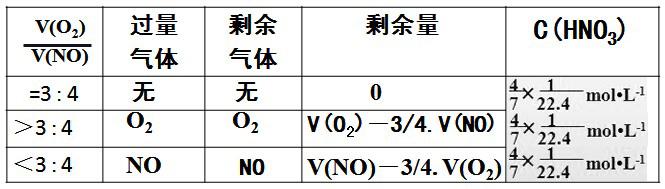
讨论2: 如图,容积为50mL的容器充满O2和NO,倒置于水槽中,打开开关阀K,让NO和O2相通,充分反应后,试管内剩余气体体积为8mL,求原O2和NO的体积。(4NO+3O2+2H2O=4HNO3)
若剩余气体为O2,NO为24mL,O2为26mL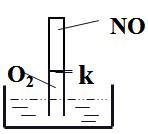
若剩余气体为NO,NO为32mL,O2为18mL
(3)NO2和O2的混合物溶于水
3NO2+H2O = 2HNO3+NO ……①×2+) 2NO+O2=2NO2 …… ②×3
总式:4NO2+O2+2H2O=4HNO3
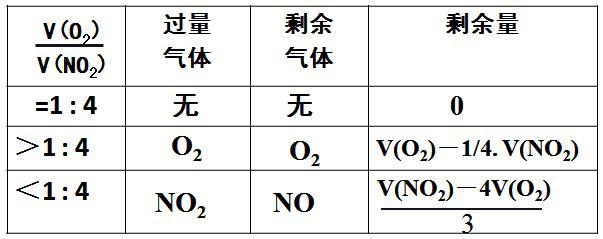
讨论3:将容积为50mL的量筒内充满NO2与O2的混合气体,倒置在盛满水的水槽中,充分反应后,剩余5ml气体,则混合气体中NO2与O2的体积比可能是多少?
4NO2+O2+2H2O=4HNO3 当氧气剩余时,体积比为 18 :7
当二氧化氮剩余时(由于二氧化氮与水反应,最终剩余的为NO,要注意转化),体积比为 43 :7
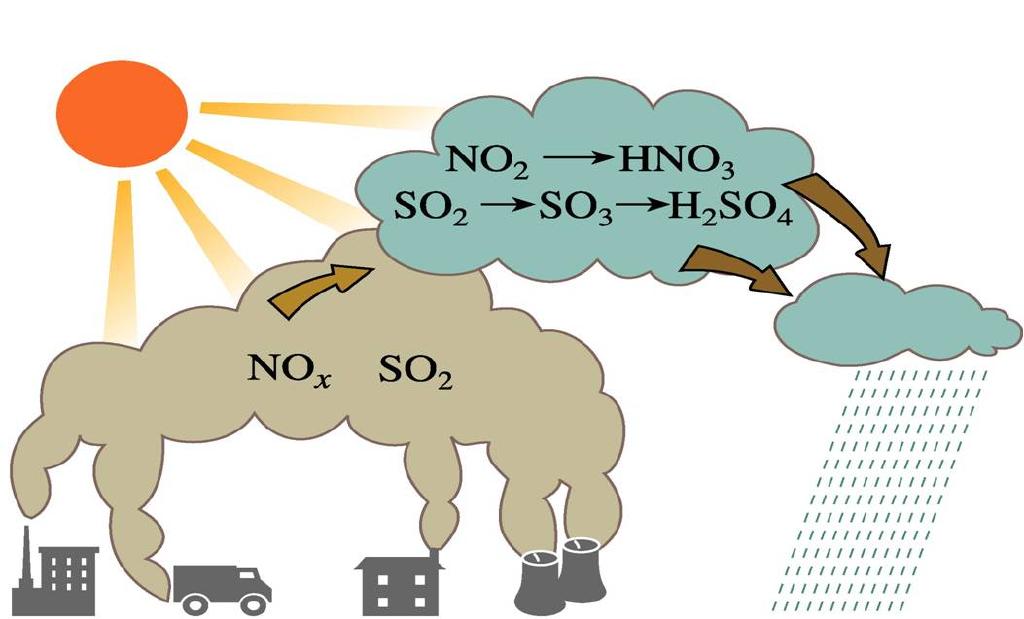
4、氮的氧化物对环境的危害
(1)在紫外线的照射下产生光化学烟雾


(2)与二氧化硫等有害气体共同形成酸雨