氯单质及其重要化合物
上一节
下一节
考点精讲
一、氯气:
1、氯气的物理性质
| 颜色 | 状态 | 气味 | 密度 | 毒性 | 溶解性 |
|---|---|---|---|---|---|
| 黄绿色 | 气体 | 强烈刺激性 | 比空气大 | 有毒 | 可溶于水 |
注意:实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,仅使极少量气体飘进鼻孔。
2、氯原子结构
Cl基态核外电子排布式:
![]()
Cl的原子结构简图:

结论:氯较易得到e-达到8e-稳定结构,显示出较强的氧化性。
3、氯气的重要化学性质
(1)与金属反应
A.与Na反应,现象:剧烈燃烧,产生大量白烟。

B.与Fe反应,现象:剧烈燃烧,产生棕褐色的烟。
![]()
C.与Cu反应,现象:剧烈燃烧,产生棕黄色的烟。
![]()
注意:氯气与变价金属反应时,生成高价态氯化物。
(2)与非金属反应
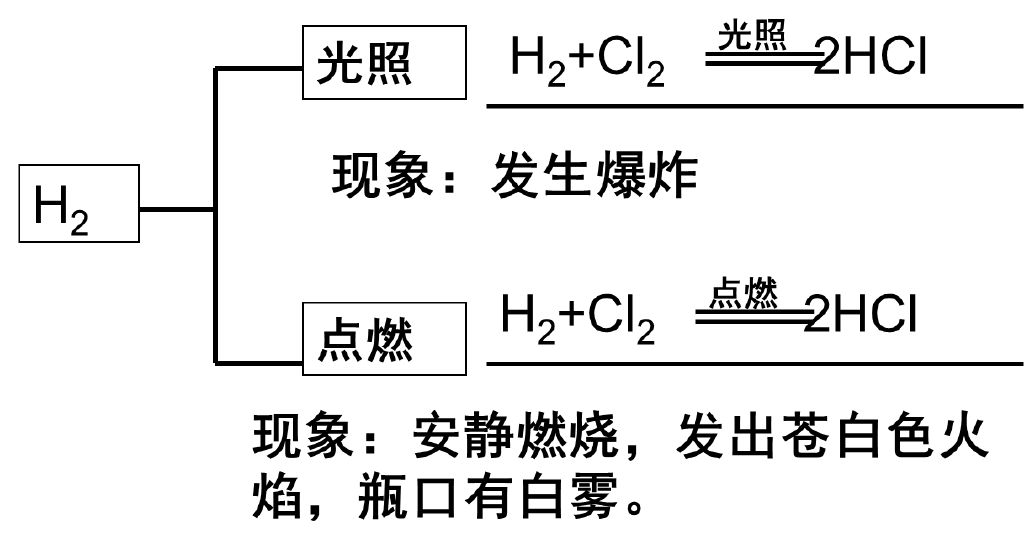
(3)与水反应:
![]()
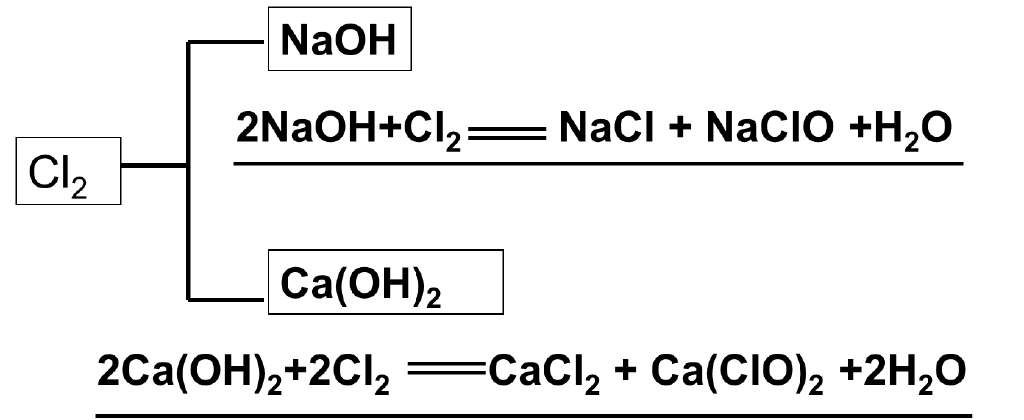
(4)与碱反应
(5)与还原性物质反应
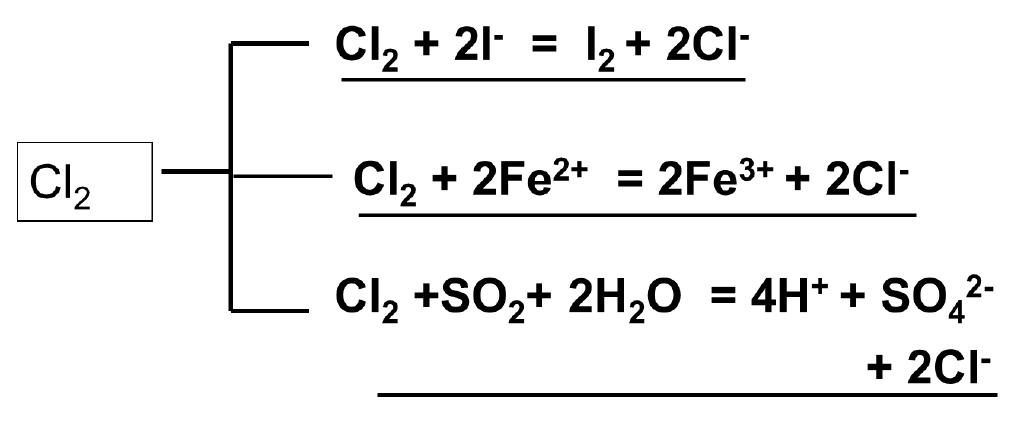
(6)与有机物反应
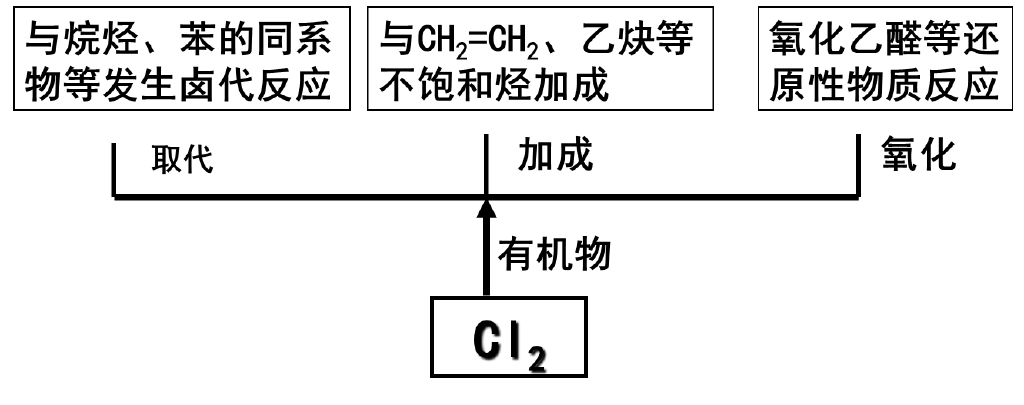
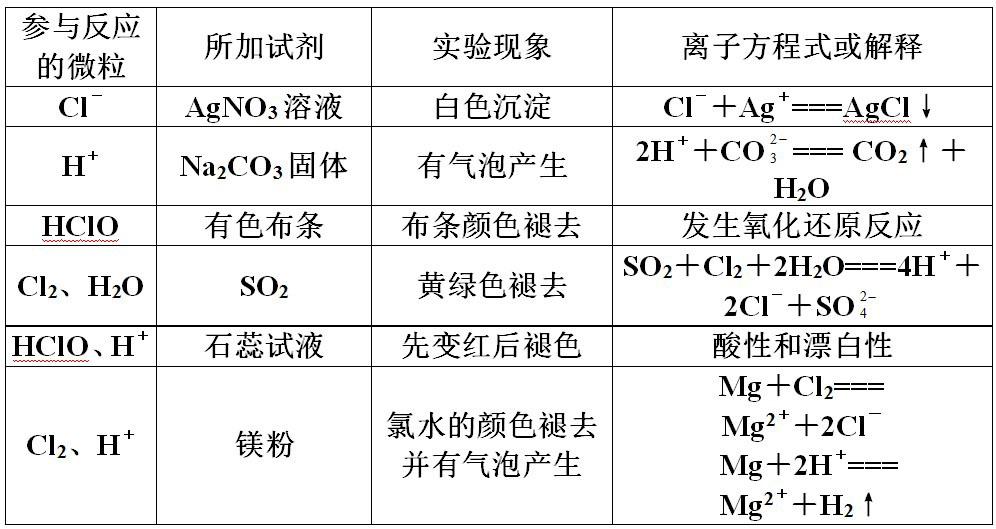
4、氯水的成分及性质
(1)、氯水中的微粒
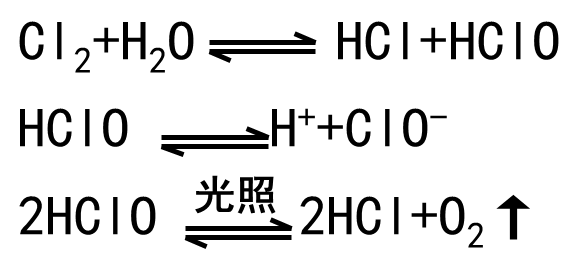
新制氯水中,所含的分子有Cl2、H2O、HClO;离子有H+、Cl-、ClO- 3OH-(少量)。
(2)氯水的性质:氯水组成的多样性,决定了它性质的多重性
① Cl-的性质;
② HCl的强酸性;
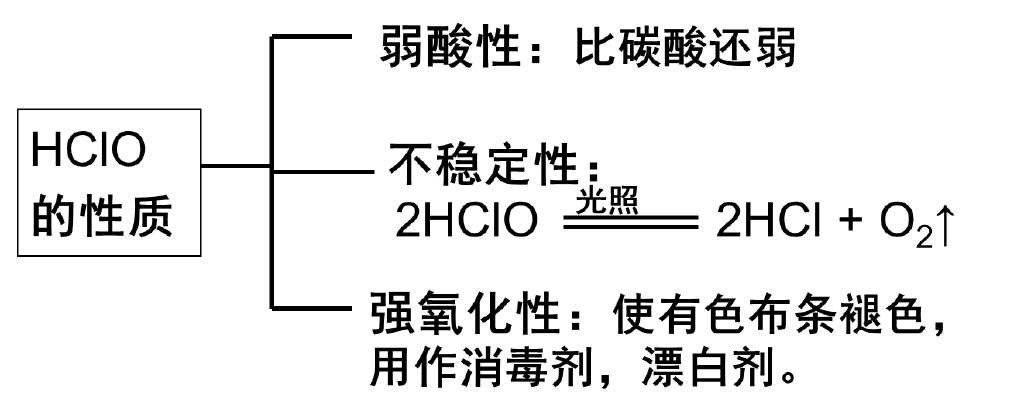
③ HClO的强氧化性、弱酸性;
④ Cl2的强氧化性。