-
1
-
2
4.3 气固相催化反应本征动力学
本征:完全没有扩散影响的,单纯的反应物及产物在催化剂表面吸附脱附反应过程。其动力学表达为本征动力学。
物理吸附和化学吸附
• 物理吸附-吸附剂与被吸附物靠范德华力结合
• 化学吸附-吸附剂与被吸附物之间可视为发生化学反应
其特点和异同点:
一、化学吸附与脱附
1、化学吸附速率的表达
活性中心:固体催化剂表面能够与气相分子发生反应的原子。以符号σ表示。
吸附式可以表示为如下型式:A+ σ→A σ
A-反应物, σ-活性中心, A σ-吸附了反应物的活性中心
既然吸附过程可以视为化学反应(基元反应),吸附速率式就可以写成:
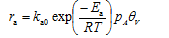
达到平衡时,吸附与脱附速率相等:
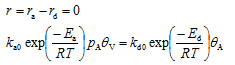
θ难于测量,不便应用。可利用吸附模型求得θ。
2、Langmuir 吸附模型
基本假定:
• 催化剂表面活性中心的分布是均匀的;
• 吸、脱附活化能与表面覆盖率无关;
• 每个活性中心只能吸附一个分子;
• 吸附的分子之间互不影响。
称为理想吸附模型。
基于以上假定,有:
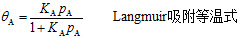
2、焦姆金(ТЕМКИН)吸附模型
与Langmuir吸附模型不同, ТЕМКИН模型认为吸附及脱附活化能与表面覆盖率呈线性关系。即:
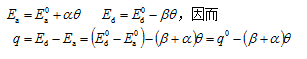
3、弗鲁德里希(Freundlich)吸附模型
比焦姆金吸附模型更进一步, Freundlich模型认为吸附及脱附活化能与表面覆盖率并非呈线性关系,而是对数关系。即:
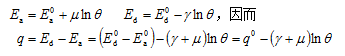
二、表面化学反应
目的:定义被吸附在催化剂活性中心上的反应物之间的反应速率。
将被催化剂活性中心吸附的反应物之间进行的化学反应通常被认为是基元反应,其速率表达符合质量作用定律。
1、反应本征动力学
基于理想吸附假定,得到双曲型(Hougen-Watson)型方程。
基本假定:
• 在吸附、反应、脱附三个过程中必有一个最慢,这个最慢的步骤被称为控制步骤,代表了本征反应速率;
• 除控制步骤外的其它步骤均处于平衡状态;
• 吸附和脱附都可以用Langmuir吸附模型描述。
对于一个反应过程有不同的控制步骤
(1)吸附、脱附过程为控制步骤
(2)表面化学反应为控制步骤
模型方法:
• 将吸附、反应、脱附各步骤写清楚;
• 依质量作用定律写出反应、吸附、解吸速率式;
• 令所有非控制步骤达到平衡,设平衡常数;
• 从平衡的各式中解出θ,代入到非平衡式中;
• 最后的结果中,只出现非平衡式(控制步骤)的速率常数、各平衡式的平衡常数及各组份的分压。各常数可以合并。
用途:
• 建立动力学方程的骨架,确立动力学方程的基本型式,为在实验上得到动力学参数做准备。
• 方程中的各K为待定参数。通过实验筛选合适的模型(模型识别),模型识别后通过进一步的实验确定模型参数(参数估值)得到满意的动力学模型。
如果存在两种活性中心,分别仅吸附A和B,此时对某反应
利用与前面完全相同的技巧,可以推导出各种不同控制步骤时的动力学表达。
如当化学反应为控制步骤时有一结果:
由动力学方程的型式判断反应历程:
动力学方程的基本型式: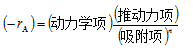
教学后记:


