4.1气固相催化过程
对于气固相催化反应,由于反应在异相进行,存在本征动力学和宏观动力学之分,其区别在于有无传递过程的影响。
气固相:反应物和产物均为气相,催化剂为固相。
催化剂参与反应,但在反应过程中不消耗。
催化剂的加入可以改变反应速率。
催化剂的加入,不能改变反应的平衡。催化剂以同样的比例同时改变正逆反应的速率。
催化剂可以在复杂的反应系统,有选择地加速某些反应。
同样的反应物在不同催化剂的作用下可以生成不同的产品。
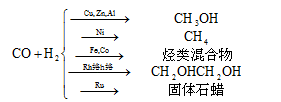
如果希望催化剂充分发挥作用,应当尽可能增加反应物与催化剂的接触。
一、非均相催化反应速率表达
对于均相反应,已经定义速率
由于气固相催化反应发生在催化剂表面,而且催化剂的量对于反应的速率起着关键的作用,因此,反应速率不再由反应体积来定义,而改由催化剂体积来定义。
1、以催化剂体积定义反应速率:
2、以催化剂质量定义反应速率:
3、以催化剂内表面积定义反应速率:
固体催化剂的特殊结构,造成化学反应主要在催化剂的内表面进行。
催化剂的表面积绝大多数是内表面积。
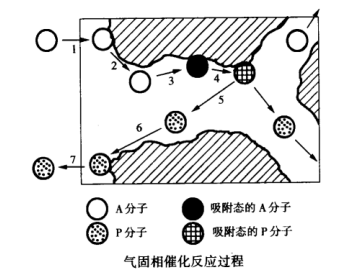
气固相催化反应的7个步骤、3个过程:
1反应物由气流主体扩散到催化剂外表面;2反应物由催化剂外表面扩散到内表面; 3反应物在催化剂表面活性中心上吸附; 4吸附在活性中心的反应物进行化学反应;5产物在催化剂表面活性中心上脱附; 6产物由催化剂内表面扩散到外表面;7产物由催化剂外表面扩散到气流主体。
• 1,7为外扩散过程
• 2,6为内扩散过程
• 3,4,5为化学动力学过程
针对不同具体情况,三个过程进行的速率各不相同,其中进行最慢的称为控制步骤,控制步骤进行的速率决定了整个宏观反应的速率。


