一、可逆反应过程特点
1、在温度恒定时,随关键组分转化率xA的增加,正反应速率k1f(xA)将随之下降;逆反应速率k2g(xA)将随之上升;总反应速率-rA=ak1f(xA)-ak2g(xA)将随之下降。
2、温度对反应速率的影响 在一定转化率下,可逆吸热反应的速率总是随着温度的升高而增加。
可逆放热反应的速率随温度的变化规律如图所示,当温度较低时,反应净速率随温度升高而加快,到达某一极大值后,随着温度的继续升高,净反应速率反而下降。
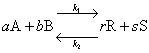
设可逆反应: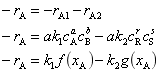
总反应速率(-rA)为正逆反应速率之差:![]()
当正逆反应速率相等时,总反应速率为零,反应达到平衡(-rA)=0。
此时:![]()
式中:KC为此反应在当前反应温度下以浓度表示的平衡常数,因次为浓度单位的Δn次方;xAe为平衡转化率。
平衡常数K为热力学参数,无因次,与反应速率及其表达式无关,可以通过参与此反应的各组分的标准生成自由焓求得。
平衡常数与温度的关系:
如果忽略反应热效应随温度的变化,可以通过下式由已知的一个温度下的平衡常数求得另一个温度下的平衡常数: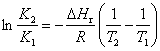
可以推导出平衡转化率与平衡温度之间的关系: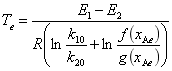
一、可逆反应过程特点
1、在温度恒定时,随关键组分转化率xA的增加,正反应速率k1f(xA)将随之下降;逆反应速率k2g(xA)将随之上升;总反应速率-rA=ak1f(xA)-ak2g(xA)将随之下降。
2、温度对反应速率的影响 在一定转化率下,可逆吸热反应的速率总是随着温度的升高而增加。
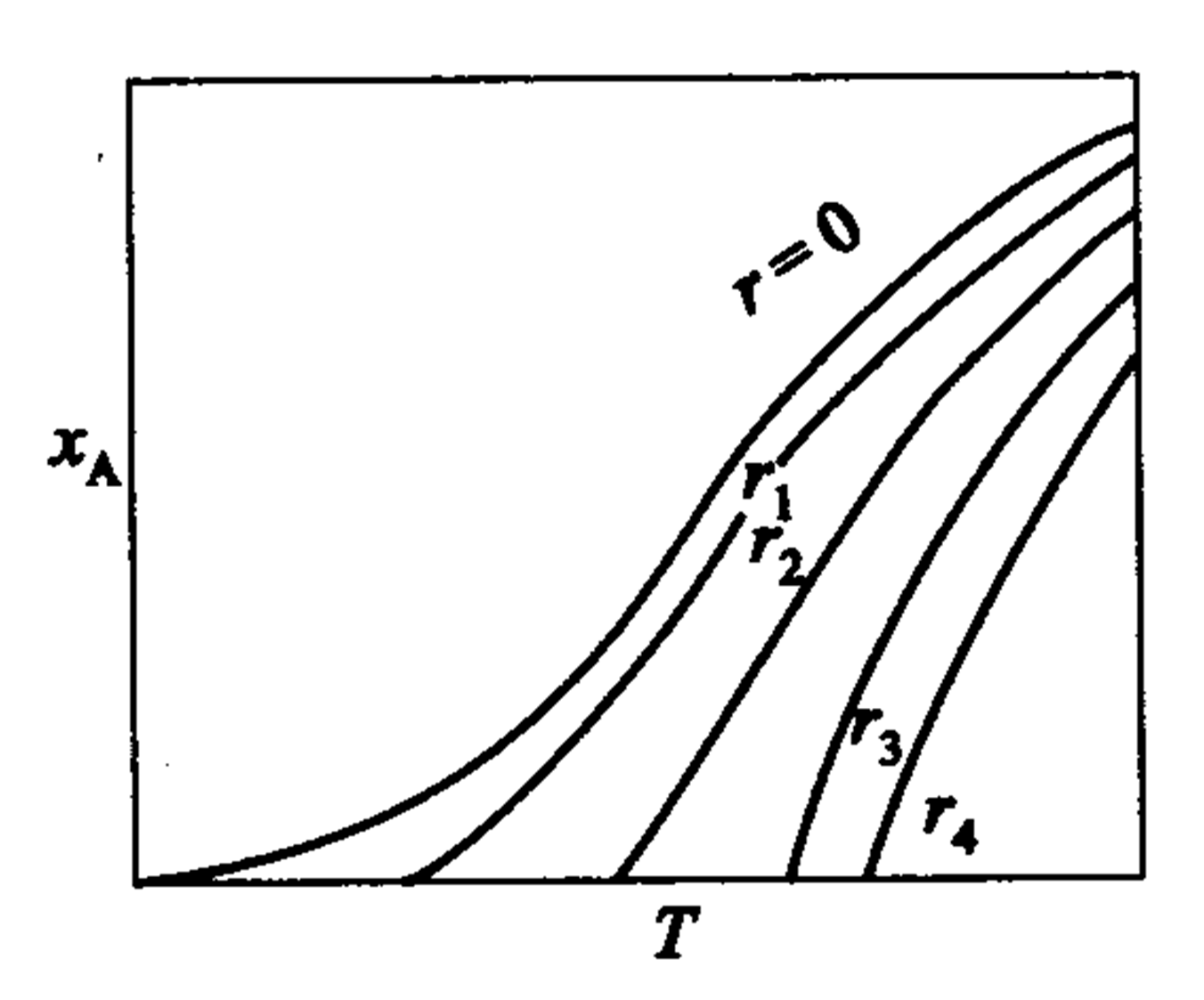
可逆放热反应的速率随温度的变化规律如图所示,当温度较低时,反应净速率随温度升高而加快,到达某一极大值后,随着温度的继续升高,净反应速率反而下降。
教学后记:


