13.3萃取分离法
11.3.1液-液萃取分离
2 分配定律、分配系数和分配比
分配定律:有机溶剂从水相中萃取溶质A,若A在两相中的存在形态相同,平衡时,在有机相的浓度为[A]o, 水相的浓度为[A]w之比,用KD表示。
分配系数:
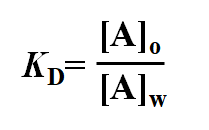
注意:1.溶质浓度低;
2.两相存在形式相同(无副反应)
2分配定律、分配系数和分配比
n分配比: 物质A在两相中可能存在多种形态,在两相中的各形态浓度总和(c)之比,用D表示。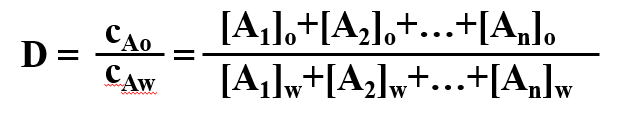
如果用Vo (mL) 溶剂萃取含有mo (g) 溶质A的Vw(mL)试液,一次萃取后,水相中剩余m1(g)的溶质A,进入有机相的溶质A为(mo-m1) (g), 此时分配比为:
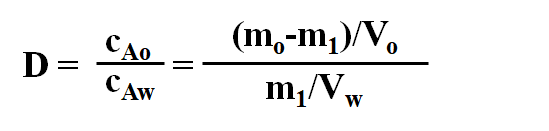
m1=mo[Vw/(DVo + Vw)]
萃取两次后,水相中剩余物质A为m2(g)
m2=mo[Vw/(DVo + Vw)]2
…
萃取n次后,水相中剩余物质A为mn(g)
mn=mo[Vw/(DVo + Vw)]n
3 萃取率
萃取率用于衡量萃取的总效果,用E表示

例,用乙醚萃取从一肉样品中除去脂,脂的D=2,现有乙醚90ml,有人介绍分三次每次30ml对分散在30ml水中的含有0.1g脂的1.0g肉制品进行萃取,那么一次90ml和三次30ml分别萃取,哪一个好?
计算:
一次90ml,x=0.1(30/[(2×90)+30]1=0.014g
三次30ml,x=0.1(30/[(2×30)+30]3=0.0037g
例题:今有一0.0500mol/L西药25.0mL,在某一有机溶剂和水中分配比为9.6,若要使水相中的西药浓度小于1.0×10-4mol/L,计算:(1)若一次萃取需有机溶剂多少毫升?;(2)若每次10mL萃取,共需多少毫升?
4萃取体系和萃取平衡
萃取平衡
萃取剂多为有机弱酸碱, 中性形式易疏水而溶于有机溶剂,一元弱酸(HL)在两相中平衡有:

a 螯合萃取体系
螯合物萃取是金属离子萃取的主要方式,萃取剂是螯合剂,形成的螯合物为中性,溶于有机溶剂被萃取。
如双硫腙与Hg2+的络合物,8-羟基喹啉与La3+的络合物等属螯合物萃取体系。
螯合物萃取体系存在的几个平衡关系如下图:
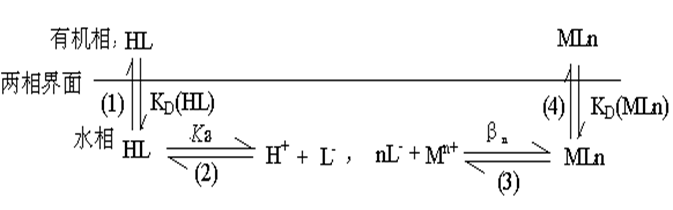
总的萃取平衡方程式为:M(w)+nHL(o) =MLn(o)+nH+(w)
萃取平衡常数Kex
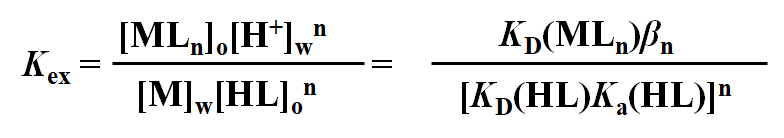

b离子缔合物萃取体系
阳离子和阴离子通过静电引力相结合而形成电中性的化合物称为离子缔合物。该物具有疏水性,能被被有机溶剂萃取。
碱性阳离子染料与络阴离子形成的缔合物,如次甲基蓝与[BF4]-、罗丹明B与[AuCl4] -,四苯胂[(C6H5)4As]+与WO42-;
金属大络阳离子(Cu+-新亚铜灵络阳离子与Cl-)及季铵盐与阴离子或金属络阴离子形成的缔合物。
c溶剂化合物萃取体系
中性有机溶剂分子通过配位原子与金属离子键合,而溶于该有机溶剂中,从而实现萃取。
如,磷酸三丁酯(TPB) 在盐酸介质中萃取Fe3+, FeCl33TPB
杂多酸萃取体系
在HCl溶液中乙醚萃取FeCl4-,乙醚与H+形成[(CH3CH2)2OH]+,它与FeCl4-形成缔合物[(CH3CH2)2OH]+·[FeCl4]-。在这里乙醚既是萃取剂又是萃取溶剂。如此的还有甲基异丁基酮,乙酸乙酯等。含氧有机溶剂化合物成盐的能力大小为:
R2O>ROH>RCOOH>RCOOR'>RCOR'>RCHO
也有把该体系列入离子缔合萃取体系。
d 共价化合物萃取体系
也叫简单分子萃取体系,如I2,Br2,GeCl4,OsO4等不带电荷,在水溶液中以分子形式存在,可为CCl4,C6H6等萃取
5 萃取条件的选择
a 萃取剂的选择
螯合物稳定,疏水性强,萃取率高
b 溶液的酸度
酸度影响萃取剂的离解,络合物的稳定性,金属离子的水解
c 萃取溶剂的选择
l金属络合物在溶剂中有较大的溶解度,尽量采用结构与络合物结构相似的溶剂,
l萃取溶剂的密度与水溶液的密度差别要大,粘度要小,易分层。
l毒性小,最好无毒,并且挥发性小。
6萃取方法及分析化学中的应用
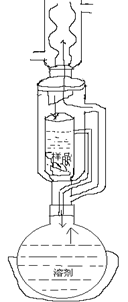
萃取方法
•单级萃取
•连续萃取
•多级萃取