9.5 沉淀溶解平衡及其应用
•9.5.1 影响沉淀纯度的因素
•9.5.2 沉淀的形成和沉淀条件
•9.5.3 重量分析法
•9.5.4 沉淀滴定法
9.5.1影响沉淀纯度的因素
一、共沉淀 (coprecipitation)
沉淀析出时,溶液中的某些可溶性杂质会被沉淀带下来而混杂于沉淀中,这种现象称为共沉淀。如,BaSO4沉淀中常含有Fe2(SO4)3
重量分析中最重要的误差来源之一。
产生共沉淀的原因是表面吸附,形成混晶,吸留和包藏等,其中主要的是表面吸附。
1. 表面吸附
沉淀表面离子电荷的作用力未完全平衡,形成自由力场,溶液中带相反电荷的离子被吸引到沉淀表面上,形成第一吸附层。
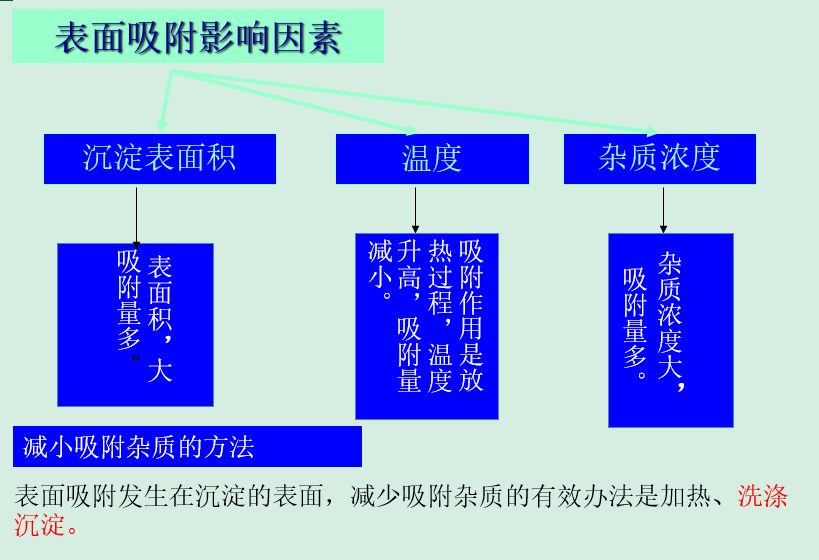
沉淀吸附杂质的量与下列因素有关:
(1)沉淀的总表面积:总表面积↑,吸附杂质↑;
(2)杂质离子的浓度:浓度↑,吸附现象↑;
(3)温度:吸附是放热过程,溶液温度↑,沉淀吸附杂质的量就减少。
2. 混晶
杂质与沉淀具有相同的晶格,或杂质离子与构晶离子具有相同的电荷和相近的离子半径,杂质将进入晶格排列中形成混晶。
MgNH4AsO4·6H2O —MgNH4PO4·6H2O ,PbSO4 —BaSO4
洗涤或陈化的方法无法净化沉淀。
如何避免:先分离除去。
3. 吸留和包藏
吸留是被吸附的杂质机械地嵌入沉淀中。
包藏常指母液机械地包藏在沉淀中。
发生的原因:沉淀剂加入太快,使沉淀急速生长,沉淀表面吸附的杂质来不及离开就被随后生成的沉淀所覆盖。
杂质被吸留或包藏在沉淀内部,不能用洗涤的方法将杂质除去,
如何避免:改变沉淀条件、陈化或重结晶。
二、后沉淀 (postprecipitation
由于沉淀速度的差异,在已形成的沉淀上形成第二种不溶物质,多发生在某组分形成的稳定的过饱和溶液中。
例:若把含有Mg2+的母液与草酸钙沉淀一起放置一段时间,则草酸镁的后沉淀量将会增多。
后沉淀所引入的杂质量比共沉淀要多,且随着沉淀放置时间的延长而增多。
某些沉淀的陈化时间不宜过久。
三、获得纯净沉淀的措施(236页)
(1)采用适当的分析程序和沉淀方法;
(2)降低易被吸附离子的浓度;
(3)再沉淀。
9.5.2 沉淀的形成与沉淀条件
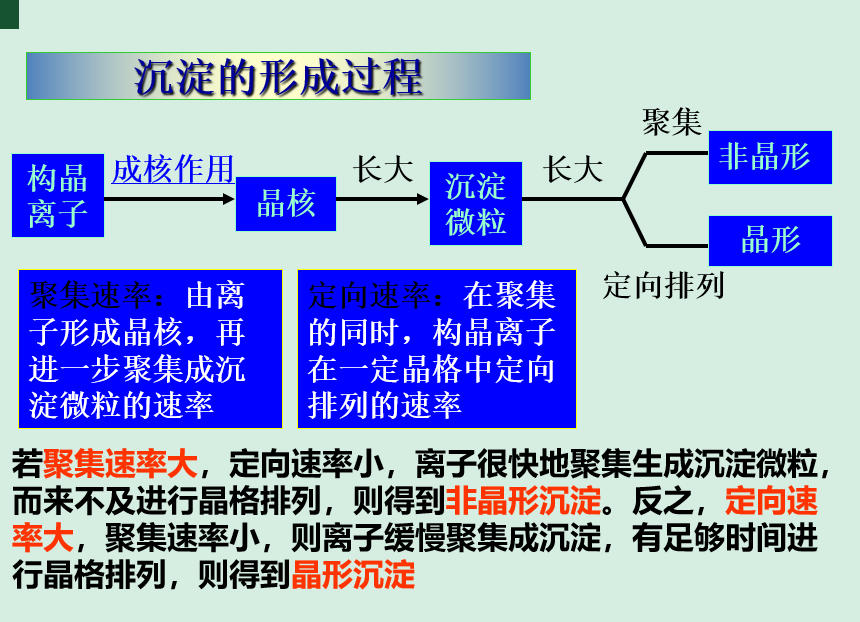
1、 沉淀的形成
晶核形成过程:当形成沉淀离子浓度的乘积>Ksp,离子相互碰撞聚集成微小的晶核。
晶核长大过程:构晶离子向晶核表面扩散,并沉积在晶核上,晶核就逐渐长大成沉淀微粒。
聚集速度:晶核→聚集成沉淀微粒的速度。
定向速度:构晶离子在晶格中定向排列的速度。
非晶形沉淀:聚集速度>定向速度。
晶形沉淀:定向速度>聚集速度。