9.4.5 常用的氧化还原滴定法
1 高锰酸钾法
2 重铬酸钾法
3 碘量法
4 其他氧化还原滴定法
 KMnO4标准溶液的配制与标定(间接法配制
KMnO4标准溶液的配制与标定(间接法配制
KMnO4自行分解反应:
4KMnO4 + 2H2O = 4MnO2↓+ 4KOH + 3O2↑
易受水、空气中还原性物质影响,间接法配置
【配制方法】:
配制时,称取稍多于理论量的KMnO4固体,溶解在规定体积的蒸馏水中,加热煮沸,暗处保存(棕色瓶)7~10d后,用微孔玻璃砂芯漏斗过滤,除去析出的沉淀,以待标定。
【标定方法】:以H2C2O4·2H2O、Na2C2O4、As2O3、纯铁丝、(NH4)2Fe(SO4)2·6H2O等为基准物质标定。其中,最常用的是Na2C2O4,因为它易提纯稳定,不含结晶水,在105~110℃烘干2h,放入干燥器中冷却后,即可使用。
标定反应(用什么酸?)
2MnO4-+ 5C2O42- +16H+ =2Mn2++ 10CO2↑+ 8H2O
5AsO33- + 2MnO4-+ 6H+ = 5AsO43-+ 2Mn2++ 3H2O
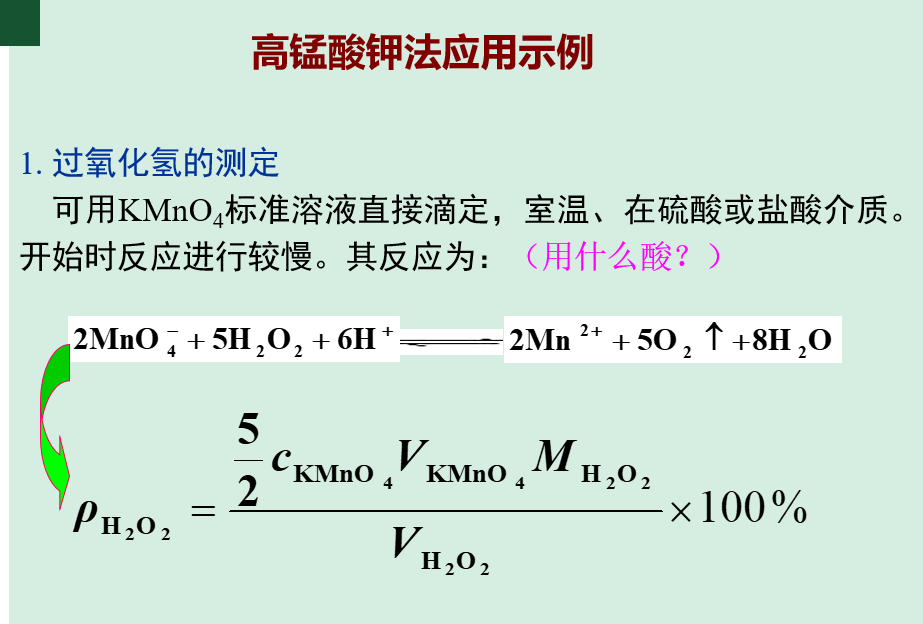
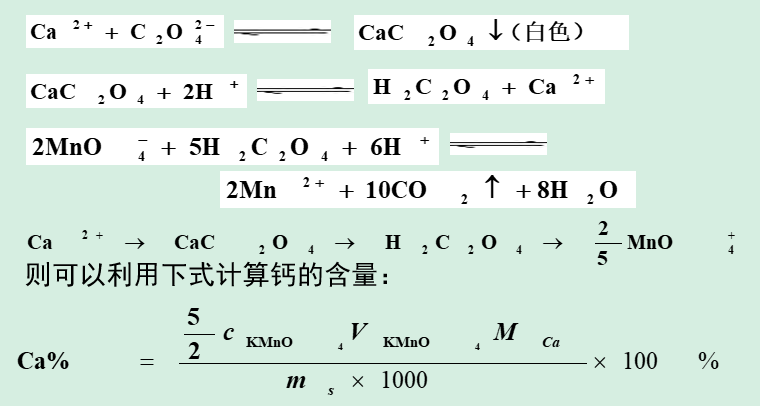
2. 高锰酸钾法测钙(间接测定法)
Ca2++C2O42 - → CaC2O4↓→陈化处理 → 过滤、洗涤 → 酸解(稀硫酸)→ H2C2O4 → 滴定(KMnO4 标液)
采取均相沉淀法:先在酸性溶液中加入过量(NH4)2C2O4,然后滴加稀氨水使pH值逐渐升高至3.5~4.5。
3. 铁的测定
试样→酸解(HCl)→ Fe3+→ SnCl2→ Fe2+→HgCl2(除去多余的SnCl2)→硫磷混酸→滴定(Fe2+)
SnCl2 + 2HgCl2 (剧毒) = SnCl4 + Hg2Cl2↓
5Fe2+ +MnO4- +8H+ = 5Fe3+ + Mn2+ + 4H2O
无汞测定铁法(见重铬酸钾法) 。
加硫磷混酸的作用:
(1) 避免Cl-存在下所发生的诱导反应;
(2) PO43-+Fe3+ (黄色)→Fe(PO4)22-(无色)
消除产物Fe3+黄色的干扰,终点颜色(KMnO4的微红色)易于观察,同时降低铁电对的电位。
9.4.5.2重铬酸钾法
1、概述
K2Cr2O7在酸性条件下与还原剂作用:
Cr2O72- + 14H++ 6e = 2Cr3++ 7H2O jq=1.33 V
(1) 氧化能力比KMnO4稍弱,仍属强氧化剂;
(2) 应用范围比KMnO4 法窄,不受Cl-影响;
(3) 此法只能在酸性条件下使用;
(4) 易提纯,稳定。作为基准试剂直接配置标准溶液。
K2Cr2O7有毒,要建立环保意识。
2、应用(略)
9.4.6.3碘 量 法
1、 概述
(1).碘量法的特点
碘量法是基于I2氧化性及I-的还原性的分析法。
I3-+ 2e = 3I -, jqI2/I-=0.534 V
用 I2标准溶液直接滴定还原剂的方法是直接碘法;
利用I-与强氧化剂作用生成定量的I2, 再用还原剂标准溶液与 I2反应,测定氧化剂的方法称为间接碘法(亦称碘量法)。
(2). 碘量法(间接碘法)的基本反应
I3-+2e = 3I - I2 +2S2O32- = S4O62- + 2 I-
反应在中性或弱酸性中进行,pH过高,I2会发生岐化反应:
3I2+ 6OH - = IO3- + 5I -+3H2O
在强酸性溶液中,Na2S2O3会发生分解,I -容易被氧化。通常pH < 9。
(3)Na2S2O3标准溶液的配制与标定
①含结晶水的Na2S2O3·5H2O容易风化潮解,且含少量杂质,不能直接配制标准溶液。
② Na2S2O3化学稳定性差,能被溶解O2、CO2和微生物所分解析出硫。因此配制Na2S2O3标准溶液时应采用新煮沸(除氧、杀菌)并冷却蒸馏水。
③ 加入少量Na2CO3使溶液呈弱碱性(抑制细菌生长),溶液保存在棕色瓶中,置于暗处放置8~12天后标定。
④ 标定Na2S2O3所用基准物有K2Cr2O7,KIO3等。采用间接碘法标定。在酸性溶液中使K2Cr2O7与KI反应, 以淀粉为指示剂,用Na2S2O3溶液滴定。
⑤ 淀粉指示剂应在近终点时加入,否则吸留I2使终点拖后。
⑥ 滴定终点后,如经过五分钟以上溶液变兰,属于正常,如溶液迅速变兰, 说明反应不完全, 遇到这种情况应重新标定。
氧化-还原滴定课本习题讨论
•2. 为什么银还原器(金属银浸于1 mol•L-1HCl溶液中)只能还原Fe3+而不能还原Ti(IV)?试由条件电极电势的大小加以说明。
•6. 间接法测定铜时,都能氧化而干扰铜的测定。实验说明加入以NH4HF2使溶液pH=3.3,此时的干扰都能消除,为什么?•7. 计算在H2SO4介质中, H+浓度分别为1 mol•L-1和0.1mol•L-1的溶液中VO2+/VO 2+ 电对的条件电极电位(忽略离子强度的影响),已知E(VO2+/VO 2+)=1.00V。
•9. 用30.00 mL KMnO4恰能完全氧化一定质量的KHC2O4·H2O,同样质量的KHC2O4·H2O又恰能被25.20mL0.2000mol·L-1KOH溶液中和。计算KMnO4溶液的浓度。
•10. 用KMnO4法测定硅酸盐样品中的Ca2+含量。称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀。将洗净的CaC2O4溶解于稀H2SO4中,用0.05052 mol×L-1 KMnO4标准溶液滴定,消耗25.64mL。计算硅酸盐中Ca的质量分数。
•13. 某土壤试样1.000g,用重量法测得试样中Al2O3及Fe2O3共0.500 0g,将该混合氧化物用酸溶解并使铁还原为Fe2+后,用0.033 33 mol·L-1K2Cr2O7标准溶液进行滴定,用去25.00mLK2Cr2O7。计算土壤中FeO和Al2O3的质量分数。
•17. 今有25.00mLKI溶液,用0.050 0mol·L-1的KIO3溶液10.00mL处理后,煮沸溶液以除去I2。冷却后,加入过量KI溶液使之与剩余的KIO3反应,然后将溶液调至中性。析出的I2用0.100 8mol·L-1Na2S2O3标准溶液滴定,用去21.14 mL。计算KI溶液的浓度。


