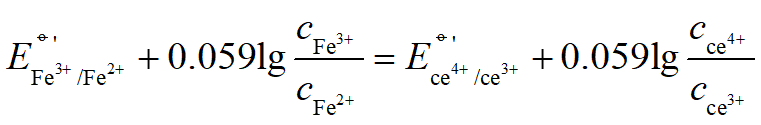9.4.3氧化还原滴定曲线及终点的确定
上一节
下一节
9.4.3氧化还原滴定曲线及终点的确定
9.4.3.1 氧化还原滴定曲线
滴定过程中存在着滴定剂电对和被滴定物电对:
n2 Ox1+ n1Red2 = n2Red1 + n1Ox2
随着滴定剂的加入,两个电对的电极电位不断发生变化,并随时处于动态平衡中。可由任意一个电对计算出溶液的电位值,对应加入的滴定剂体积绘制出滴定曲线。
化学计量点前,常用被滴定物(量大)电对进行计算;
化学计量点后,常用滴定剂(量大)电对进行计算;
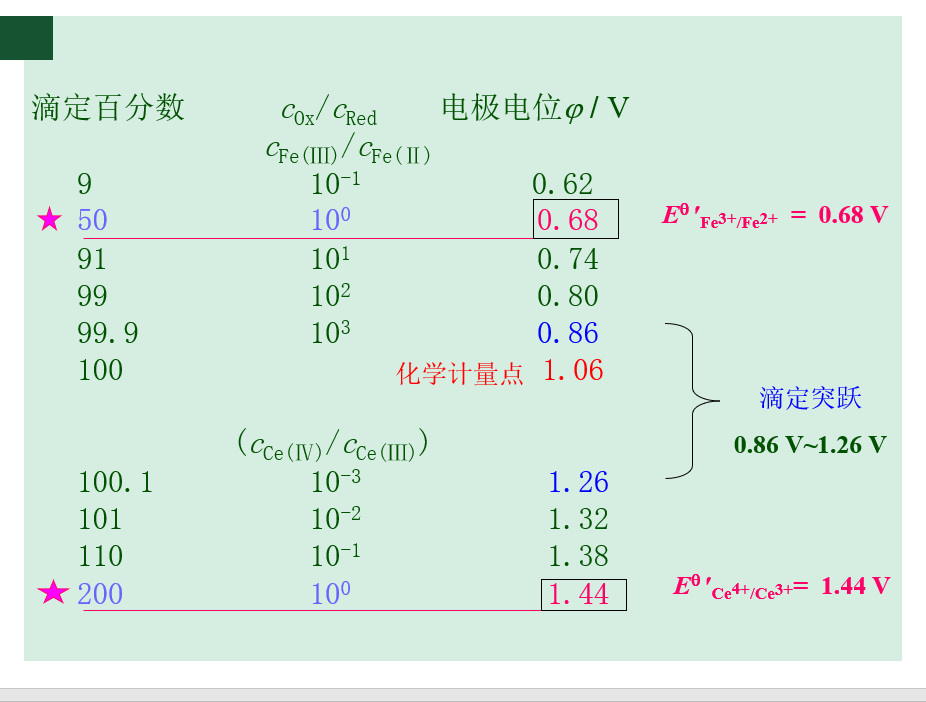
0.1000 mol ·L-1 Ce(SO4)2溶液滴定0.1000 mol ·L-1 Fe2+的酸性溶液(1.0 mol ·L-1硫酸)
滴定反应: Ce4+ + Fe2+ = Ce3+ + Fe3+
Eq′Ce4+/Ce3+= 1.44 V; Eq′Fe3+/Fe2+ = 0.68V
每加入一定量滴定剂,反应达到一个新的平衡,此时两个电对的电极电位相等: