9.4.2 氧化还原准确滴定条件和反应速率
上一节
下一节
9.4.2 氧化还原准确滴定条件和反应速率
1、 条件平衡常数
在氧化还原滴定反应过程中,需要判断:
(1) 反应是否进行完全,即终点误差是否满足要求;
(2)如果两个电对反应完全,应满足什么条件?
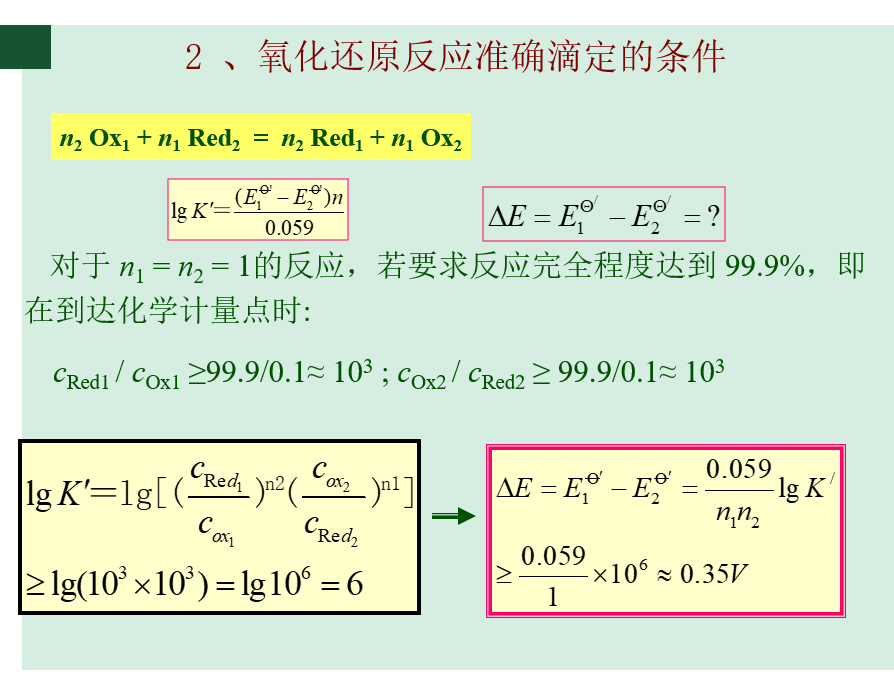
n2Ox1 + n1Red2 = n2Red1 + n1Ox2
氧化还原反应进行的程度可用平衡常数的大小来衡量。
n2Ox1 + n1Red2 = n2Red1 + n1Ox2
两个半电池反应的电极电位为:
Ox1+n1e=Red1
Ox2+n2e=Red2
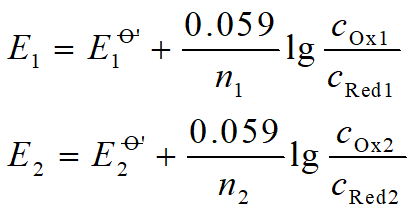
滴定过程中,达到平衡时(E1 =E2):
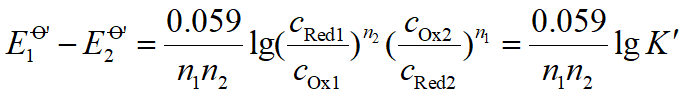
3、影响氧化反应速率的主要因素有:
1. 反应物浓度 质量作用定律,反应物浓度↑,反应
速率↑;K2Cr2O7+6KI+14HCl=8KCl+2CrCl3+7H2O+I2
Na2S2O3 +I2 =2I-+Na2S4O6
KI过量5倍, HCl在0.8至 1mol/L。
2. 温度 温度每升高10℃,反应速率可提高2~3倍。
3. 催化剂 改变反应过程,降低反应的活化能;
4. 诱导作用 由于一种氧化还原反应的发生而促
进另一种氧化还原反应进行的现象。