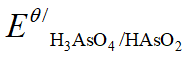9.4.1 条件电极电势及其影响因素
氧化还原半反应(RedoxHalf-Reaction)为:
Ox(氧化态) + n e-= Red(还原态)
可逆电对的电位可用能斯特方程式( NernstEquation)表示:
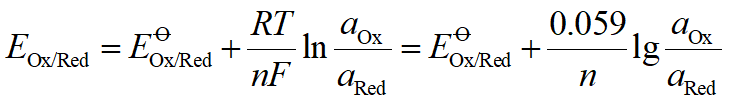
Eq: 电对的标准电极电势(Standard Electrode Potential)
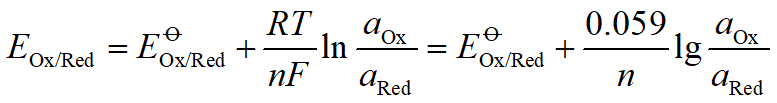
但在实际应用时,存在着两个问题:
(1) 不知道活度 a(或活度系数g): a= g c
(2) 离子在溶液中可能发生: 络合、沉淀等副反应。
( 副反应系数:αM=[M'] / [M] ;
[M' ]总浓度, [M]有效浓度 )
考虑到这两个因素(离子强度、氧化还原态的存在形式) ,需要引入条件电极电势!
9.4.1.1条件电极电势: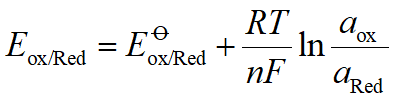
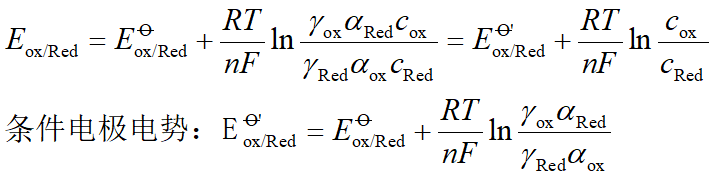 在特定条件下,氧化态与还原态的总浓度均为1mol.L-1(即cox/cRed = 1)时的实际电极电势叫条件电极电势。条件电极电势能更准确判断氧化还原反应进行的方向、次序及反应完成的程度。
在特定条件下,氧化态与还原态的总浓度均为1mol.L-1(即cox/cRed = 1)时的实际电极电势叫条件电极电势。条件电极电势能更准确判断氧化还原反应进行的方向、次序及反应完成的程度。
9.4.1.2外界条件对电极电的影响
1).离子强度的影响 离子强度较大时,活度系数远小于1,活度与浓度有较大差异。但与副反应对电极电势的影响相比一般忽略不计。
(2). 副反应的影响 主要影响因素
电对的氧化态(cOX)生成沉淀(或配合物)时,电极电势降低;
还原态(cRed)生成沉淀(或配合物)时,电极电势增加。
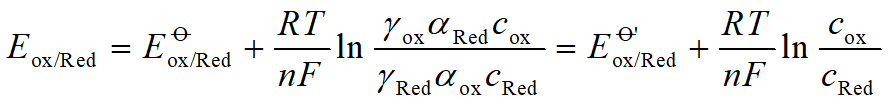
电对的氧化态(cOX)生成沉淀(或配合物)时,电极电势降低;
还原态(cRed)生成沉淀(或配合物)时,电极电势增加。
例:判断二价铜离子能否与碘离子反应
2Cu2+ + 4I- = 2CuI + I2
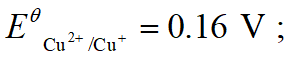
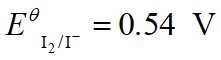
从数据看,不能反应,但实际上反应完全。
原因:反应生成了难溶物CuI,改变了反应的方向。
Ksp(CuI) = [Cu+][I-]= 1.1 ´10-12
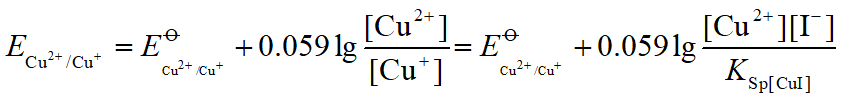 若控制[Cu2+] = [I-] = 1.0 mol ·L-1则:
若控制[Cu2+] = [I-] = 1.0 mol ·L-1则: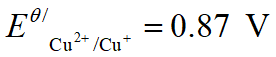
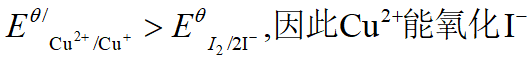
(3).酸度的影响
若有H+或OH-参加氧化还原半反应,则酸度变化直接影响电对的电极电势。
例:课本219页:例9.21pH=8.0时,忽略离子强度影响,计算: