10.2 光吸收的基本定律
1.朗伯—比耳定律
• 布格(Bouguer)和朗伯(Lambert)先后于1729年和1760年阐明了光的吸收程度和吸收层厚度的关系。A∝b 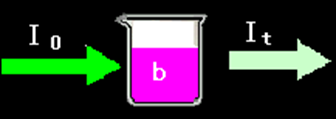 1852年比耳(Beer)又提出了光的吸收程度和吸收物浓度之间也具有类似的关系。A∝ c 二者的结合称为朗伯—比耳定律,其数学表达式为:
1852年比耳(Beer)又提出了光的吸收程度和吸收物浓度之间也具有类似的关系。A∝ c 二者的结合称为朗伯—比耳定律,其数学表达式为:
朗伯—比耳定律数学表达式
A=lg(I0/It)=εb c
式中A:吸光度;描述溶液对光的吸收程度;
b:液层厚度(光程长度),通常以cm为单位;
c:溶液的摩尔浓度,单位mol·L-1;
ε:摩尔吸光系数,单位L·mol-1·cm-1;
或: A=lg(I0/It)=a b c
c:溶液的浓度,单位g·L-1
a:吸光系数,单位L·g-1·cm-1
a与ε的关系为:
a =ε/M (M为摩尔质量)
透光度(透光率)T
透光度T : 描述入射光透过溶液的程度:
T = It / I0
吸光度A与透光度T的关系:
A= -lg T
© 朗伯—比耳定律是吸光光度法的理论基础和定量测定的依据。应用于各种光度法的吸收测量;© 摩尔吸光系数ε在数值上等于浓度为1 mol/L、液层厚度为25px时该溶液在某一波长下的吸光度(却不能这样测定,为什么?);© 吸光系数a(L·g-1·cm-1)相当于浓度为1 g/L、液层厚度为25px时该溶液在某一波长下的吸光度。
2.摩尔吸光系数ε的讨论
(1)吸收物质在一定波长和溶剂条件下的特征常数;
(2)不随浓度c和光程长度b的改变而改变。在温度和波长等条件一定时,ε仅与吸收物质本身的性质有关,与待测物浓度无关;
(3)可作为定性鉴定的参数;
(4)同一吸收物质在不同波长下的ε值是不同的。在最大吸收波长λmax处的摩尔吸光系数,常以εmax表示。εmax表明了该吸收物质最大限度的吸光能力,也反映了光度法测定该物质可能达到的最大灵敏度。
摩尔吸光系数ε的讨论
(5)εmax越大表明该物质的吸光能力越强,用光度法测定该物质的灵敏度越高。ε>105:超高灵敏;
ε=(6~10)×104 :高灵敏;
ε<104 :不灵敏。
(6)ε在数值上等于浓度为1mol/L、液层厚度为25px时该溶液在某一波长下的吸光度。
3.偏离朗伯—比耳定律的原因(了解)
标准曲线法测定未知溶液的浓
度时,发现:标准曲线常发生弯曲
(尤其当溶液浓度较高时),这种
现象称为对朗伯—比耳定律的偏离。
引起这种偏离的因素(两大类):
(1)物理性因素,即仪器的非理想引起的;
(2)化学性因素。
(1)物理性因素
难以获得真正的纯单色光。
朗—比耳定律的前提条件之一是入射光为单色光。
•
分光光度计只能获得近乎单色的狭窄光带。复合光可导致对朗伯—比耳定律的正或负偏离。
非单色光、杂散光、非平行入射光都会引起对朗伯—比耳定律的偏离,最主要的是非单色光作为入射光引起的偏离。
(2)化学性因素
•朗—比耳定律的假定:所有的吸光质点之间不发生相互作用;假定只有在稀溶液(c<10-2mol/L)时才基本符合。
当溶液浓度c>10 -2 mol/L 时,吸光质点间可能发生缔合等相互作用,直接影响了对光的吸收。
• 故:朗伯—比耳定律只适用于稀溶液。
溶液中存在着离解、聚合、互变异构、配合物的形成等化学平衡时。使吸光质点的浓度发生变化,影响吸光度。
• 例:铬酸盐或重铬酸盐溶液中存在下列平衡:
CrO42- +2H+= Cr2O72-+H2O
溶液中CrO42-、Cr2O72-的颜色不同,吸光性质也不相同。故此时溶液pH对测定有重要影响。
朗伯-比尔定律的适用条件
单色光
应选用lmax处或肩峰处测定
2. 吸光质点形式不变
离解、络合、缔合会破坏线性关系
应控制条件(酸度、浓度、介质等)
3. 稀溶液
浓度增大,分子之间作用增强
吸光度的加和性与吸光度的测量A = A1 + A2 + … +An
用参比溶液调T=100%(A=0),再测样品溶液的吸光度,即消除了吸收池对光的吸收、反射,溶剂、试剂对光的吸收等。


