化学分析:常量组分(>1%), Er0.1%~0.2%
依据化学反应,使用玻璃仪器
仪器分析:微量组分(<1%), Er 1%~5%
依据物理或物理化学性质, 需要特殊的仪器
例: 含Fe约0.05%的样品, 称0.2g, 则m(Fe)≈0.1mg
重量法 m(Fe2O3)≈0.14mg,称不准
容量法 V(K2Cr2O7)≈0.02mL, 测不准
光度法 结果0.048%~0.052%, 满足要求
110.1.1 光的基本性质
1.光的基本性质
光是一种电磁波,具有波粒二象性。光的波动性可用波长l、频率n、光速c、波数(cm-1)等参数来描述:
ln= c ; 波数 =1/ l = n/c
光是由光子流组成,光子的能量:
E = h n = h c / l
(Planck常数:h=6.626× 10 -34 J ·S)
光的波长越短(频率越高),其能量越大。
单色光:单波长的光(由具有相同能量的光子组成)
白光(太阳光):由各种单色光组成的复合光
可见光区:400-760nm
紫外光区:近紫外区200- 400 nm
远紫外区10 - 200 nm(真空紫外区)
| 远紫外 | 近紫外 | 可见 | 近红外 | 中红外 | 远红外 |
| (真空紫外) |
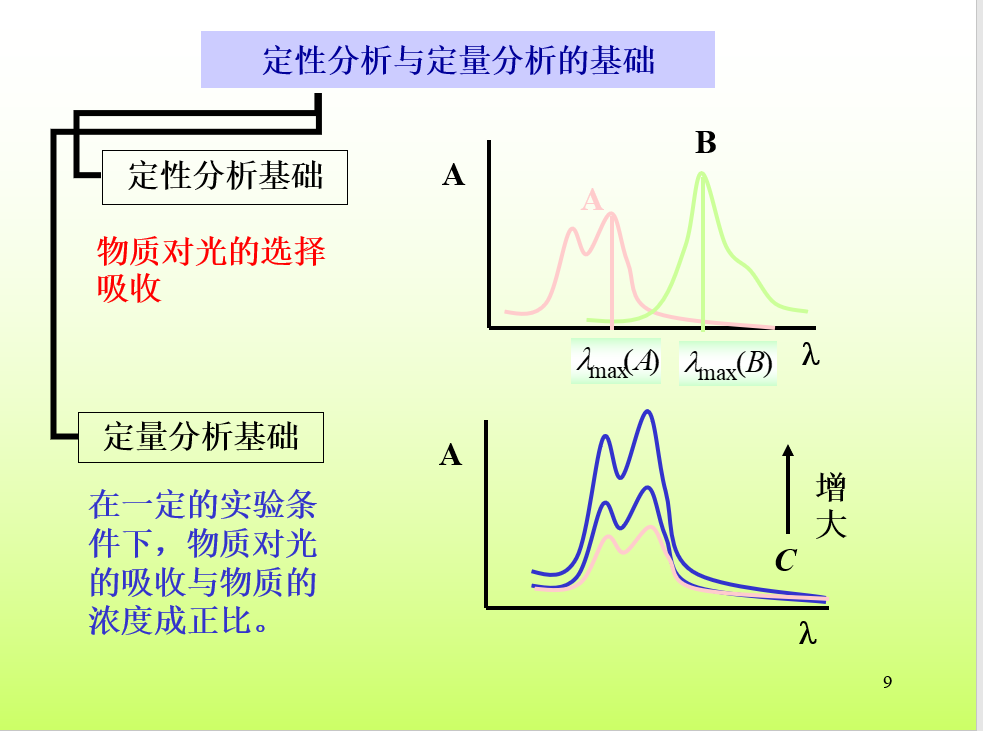
物质对光的选择性吸收及吸收曲线
DE = E2 - E1 = h n
量子化 ;选择性吸收;
分子结构的复杂性使其对不同波长光的吸收程度不同;
用不同波长的单色光照射,测吸光度—吸收曲线与最大吸收波长lmax;
若两种不同颜色的单色光按一定的强度比例混合得到白光,那么就称这两种单色光为互补色光,这种现象称为光的互补。

不同颜色的可见光波长及其互补光
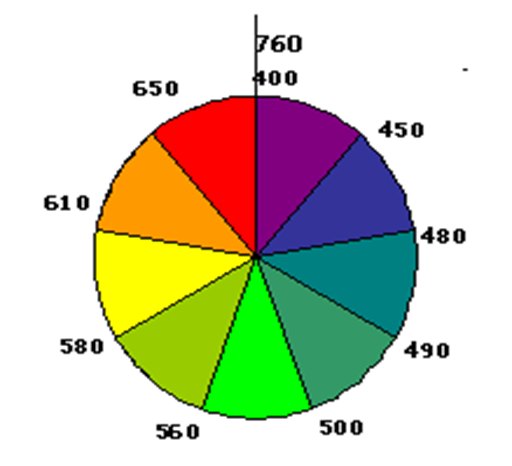
| l/nm | 颜色 | 互补光 |
| 400-450 | 紫 | 黄绿 |
| 450-480 | 蓝 | 黄 |
| 480-490 | 绿蓝 | 橙 |
| 490-500 | 蓝绿 | 红 |
| 500-560 | 绿 | 红紫 |
| 560-580 | 黄绿 | 紫 |
| 580-610 | 黄 | 蓝 |
| 610-650 | 橙 | 绿蓝 |
| 650-760 | 红 | 蓝绿 |
吸收曲线的讨论:
©(1)同一种物质对不同波长光的吸光度不同。吸光度最大处对应的波长称为最大吸收波长λmax©(2)不同浓度的同一种物质,其吸收曲线形状相似,λmax不变。而对于不同物质,它们的吸收曲线形状和λmax则不同。©(3)吸收曲线可以提供物质的结构信息,并作为物质定性分析的依据。©(4)不同浓度的同一种物质,在某一定波长下吸光度A 有差异,在
λmax处吸光度A 的差异最大,此特性可作为物质定量分析的依据。
©(5)在λmax处吸光度随浓度变化的幅度最大,所以测定最灵敏。
吸收曲线是定量分析中选择入射光波长的重要依据。