配位滴定法概述
•1、定义:以配位反应为基础的一类滴定分析方法。利用配位剂与金属离子发生配位反应,以配位剂为标准溶液,测定金属离子含量。
•2、配位剂:(1)无机配位剂,如NH3,CN-,SCN-等,与金属离子形成的配合物的稳定性较差,存在逐级配位现象,所以一般不用。(2)有机配位剂:与金属离子形成的配合物的稳定性好,不存在逐级配位现象。常用的是氨羧配位剂,其中最重要,应用最广泛的是乙二胺四乙酸(EDTA)及其二钠盐。
所以配位滴定法也称为“EDTA”法。

氨羧配位剂广泛用于滴定分析。
胺氮——易与Co2+、Ni2+、Zn2+、Cu2+、Hg2+配位。
羧氧——可与几乎所有的金属离子配位。
氨羧配位剂已发展到几十种,其中广为应用的是乙二胺四乙酸。
ethylenediaminetetraaceticacid
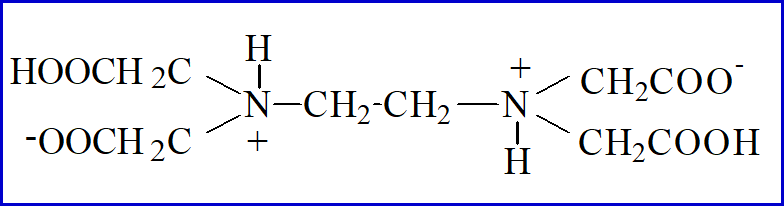
乙二胺(en) 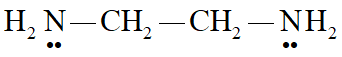
EDTA的性质
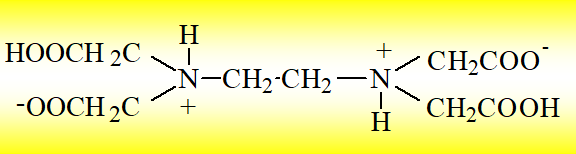
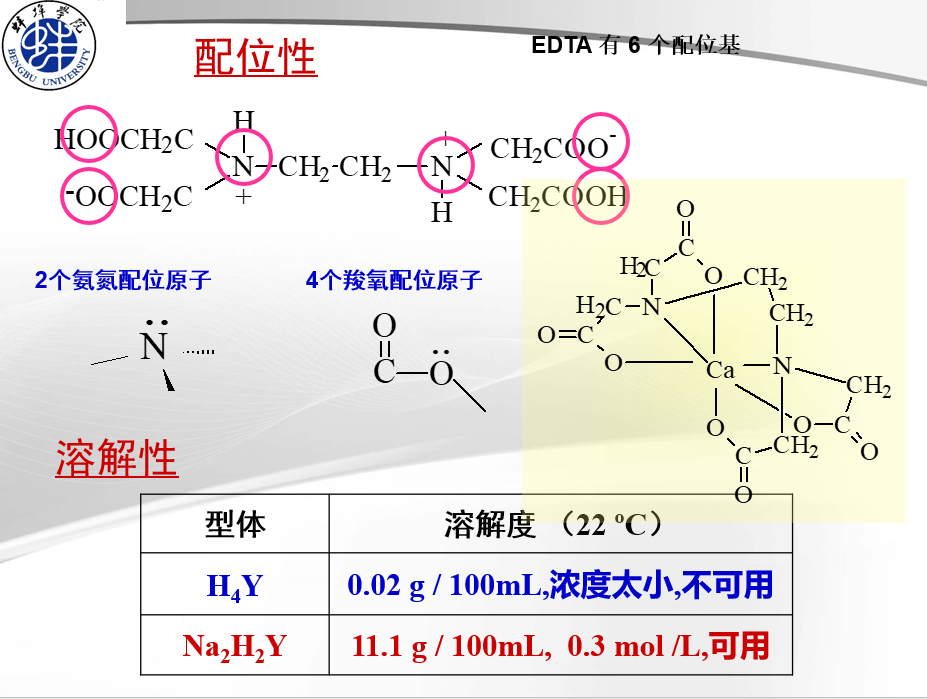


1.配位物的稳定常数(绝对稳定常数KMY)
M + Y MY(主反应,省去电荷)
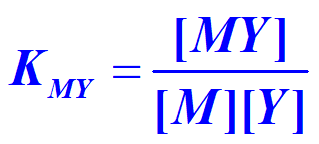
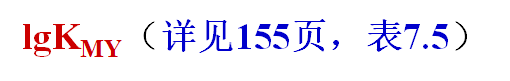
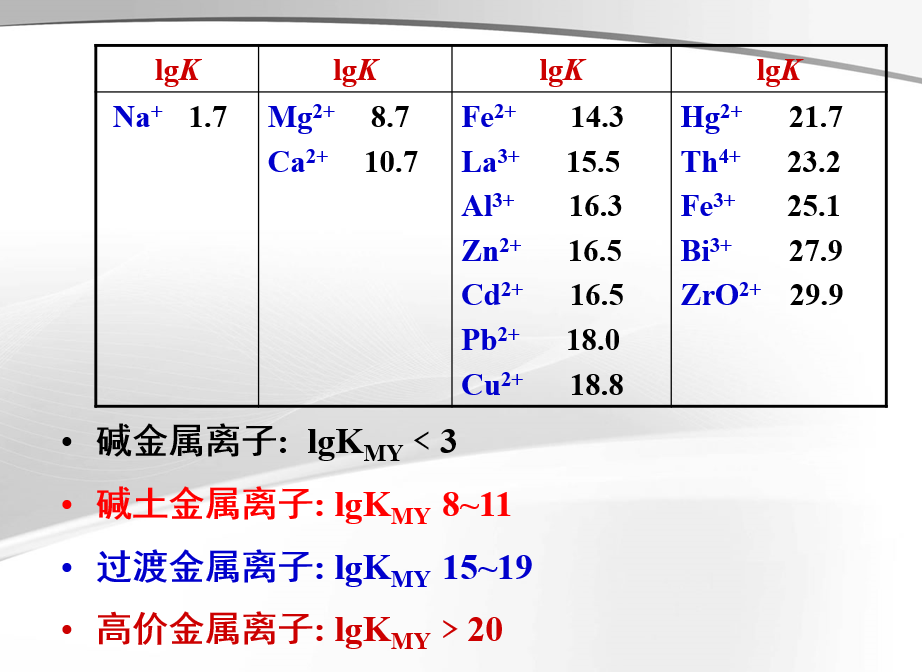
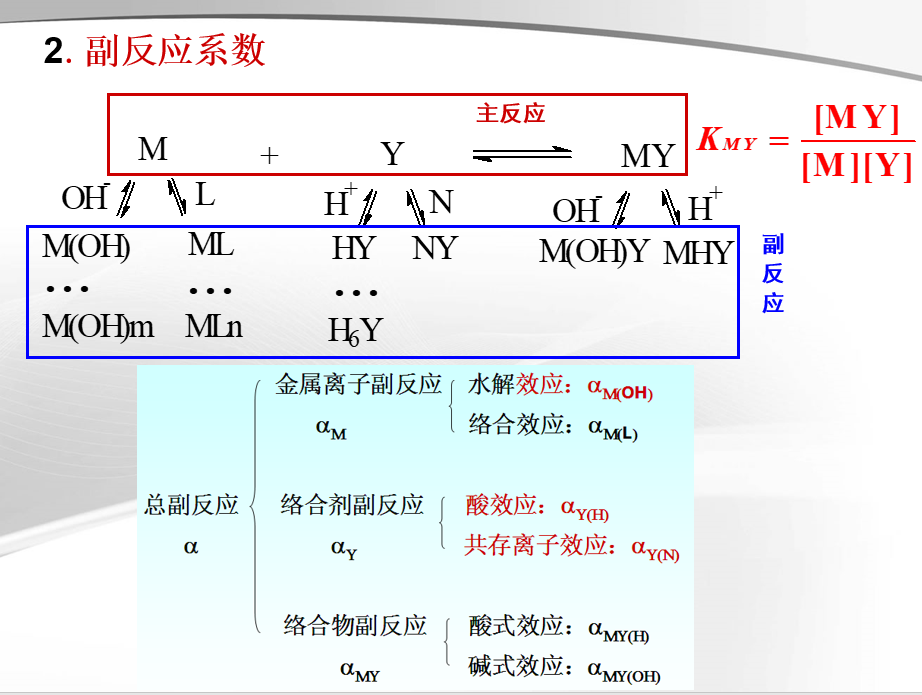
1、EDTA的酸效应及酸效应系数αY(H)
(1)定义:由于溶液中H+使EDTA参加主反应能力下降的现象。
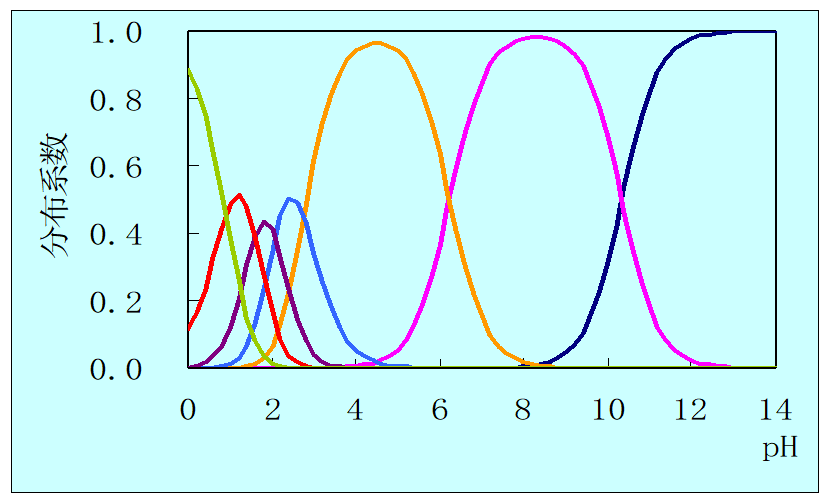
(2)定量衡量:一定pH的溶液中,EDTA各种存在形式的总浓度[Y'],与能参加配位反应的有效存在形式Y4-的平衡浓度[Y]的比值。(注意:酸效应系数与分布系数呈倒数关系)
酸效应系数αY(H) = [Y']/[Y]用来衡量酸效应大小的值。
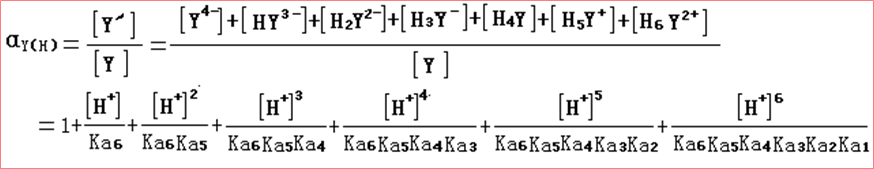
为了方便使用,将一些pH值时EDTA的酸效应系数的对数值lgαY(H)列表(155页表7.5),其他pH值的lgαY(H)值可以采用内插法。
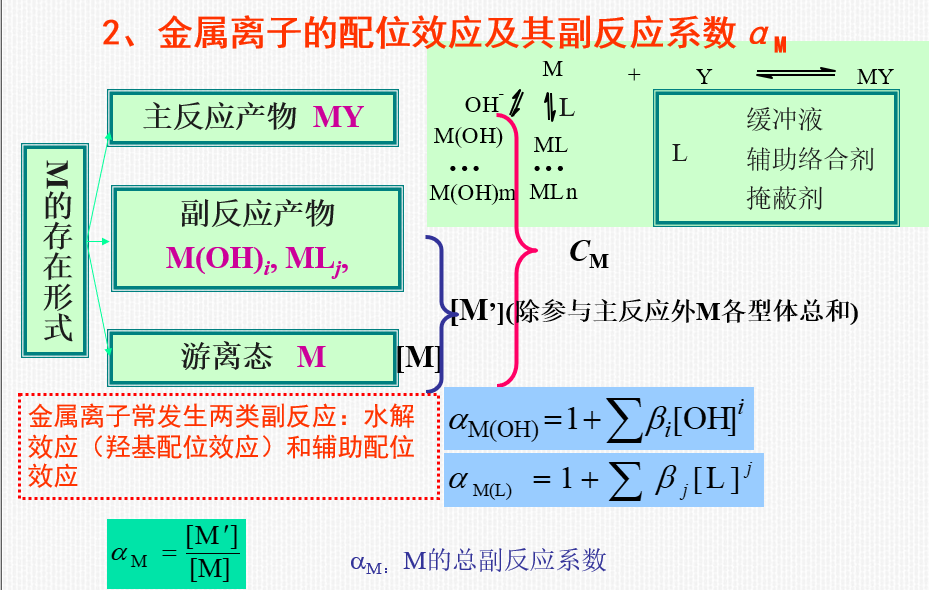


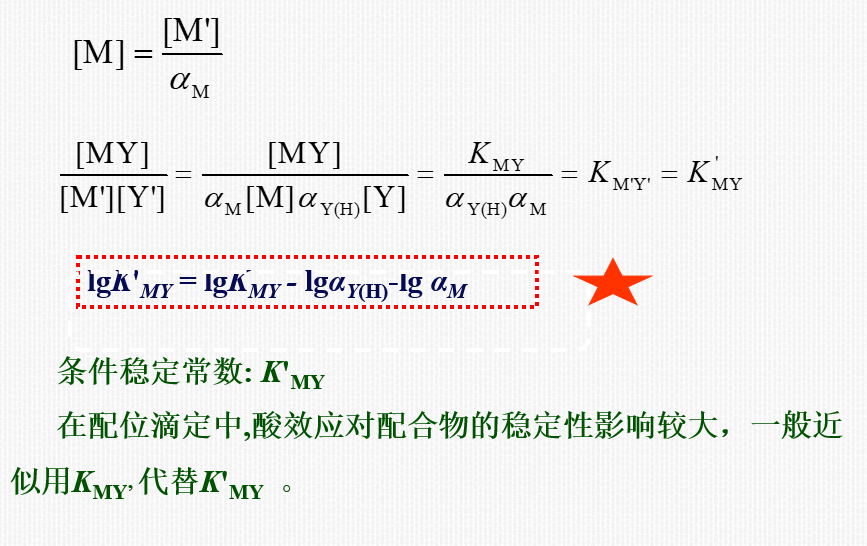

9.3.1 配位滴定曲线
n1、纵坐标为pM,横坐标为滴定分数或VEDTA。绘制pM- VEDTA曲线。
n2、仍然按照2点、2段进行讨论。
3、应使用KMY‘进行计算
以pH=10时,0.01000mol/LEDTA溶液滴定20.00mL0.01000mol/LCa2+为例讨论配位滴定曲线的绘制。
n①未滴前:pCa=2.0,
n②滴至化学计量点前:由剩余Ca2+浓度计算pCa(忽略CaY2-解离)滴定分数99.9%,加入EDTA19.98mL,pCa=5.30。
n③化学计量点:全部生成CaY2-, Ca2+由CaY2-解离产生。
n④化学计量点后:Y2-过量, Ca2+由CaY2-解离产生,过量Y2-将抑制Ca2+的产生,设加入20.02mLEDTA(100.1%)。

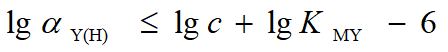
当: c= 10-2 mol/L
lgαY(H)≤ lgKMY - 8
算出lgαY(H),再查表7.5,用内插法可求得配位滴定允许的最低pH (pHmin)。
将各种金属离子的lgKMY与其最小pH绘成曲线,称为EDTA的酸效应曲线或林邦曲线。
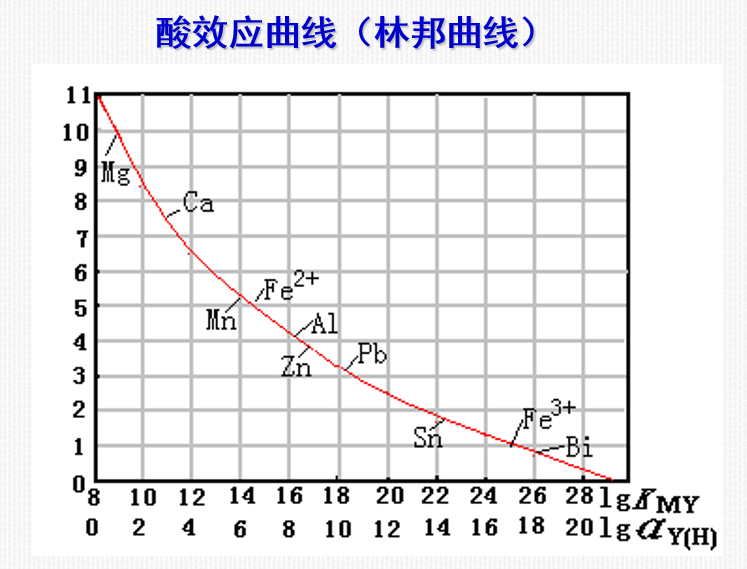
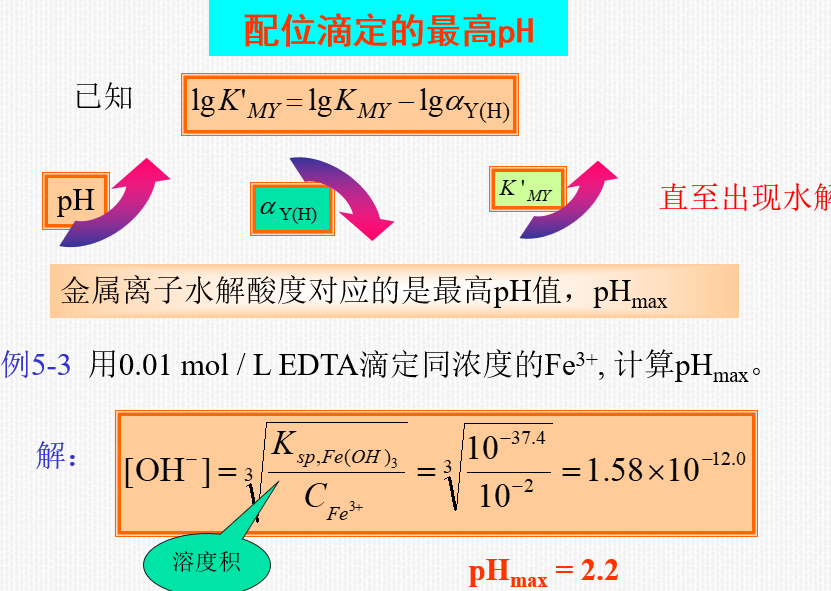
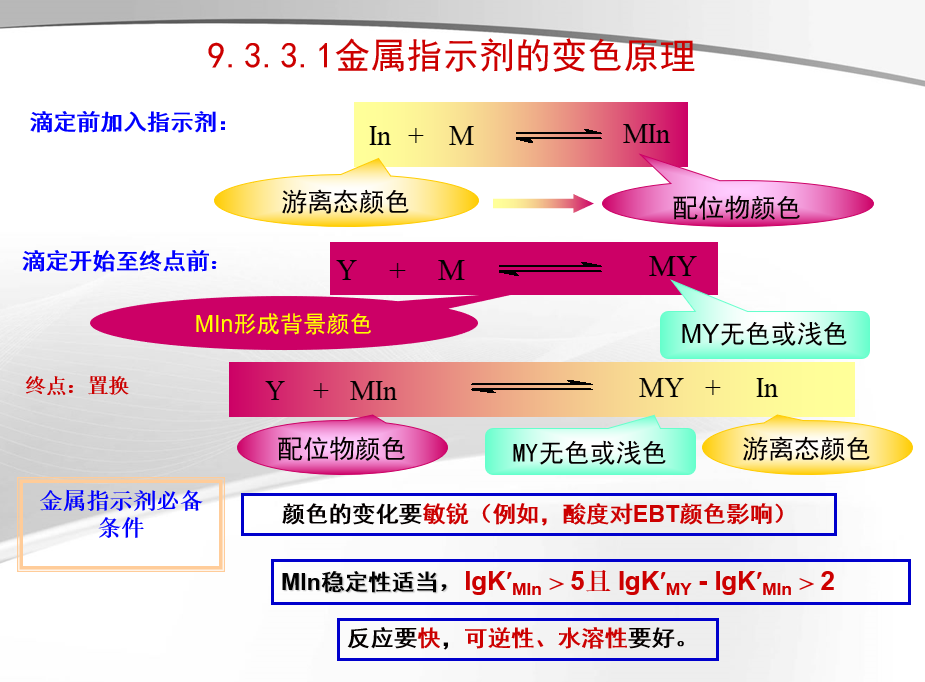
9.3.3 金属指示剂
金属指示剂 (也是配位剂)——具有酸碱性质的有机染料,能与金属离子形成明显不同于其本身颜色的有色配位物,
用以指示滴定过程中金属离子浓度的变化。
例如:铬黑T(EBT)
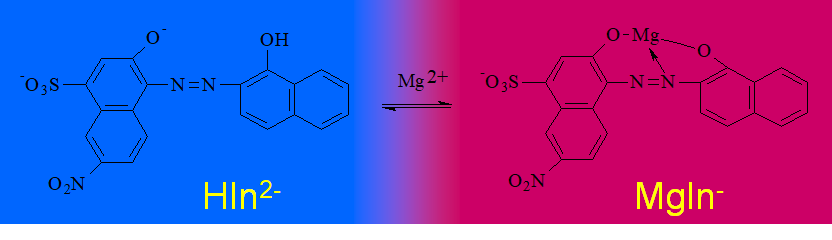
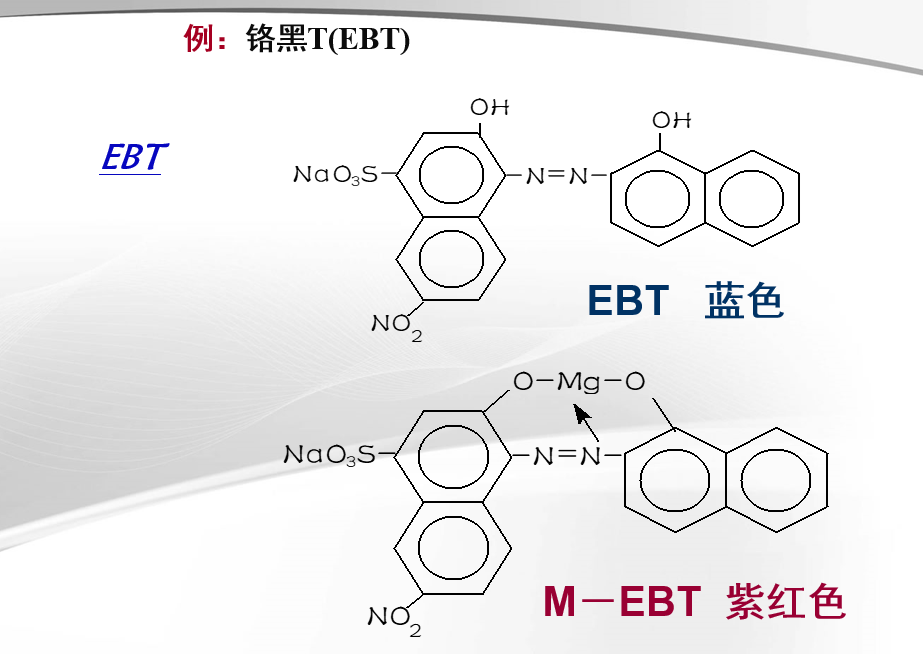
9.3.3.2使用金属指示剂中存在的问题
(1)封闭现象——因K¢MIn>K¢MY,使溶液一直呈MIn色,
无终点变色的现象。
消除方法:使用其它指示剂或掩蔽
(2) 僵化现象——因HIn或MIn溶解度小,变色过程的
反应缓慢,使终点变色不敏锐的现象。
消除方法:加适当有机溶剂或加热
(3) 变质——指示剂在放置过程中因被氧化或聚合等而变质。
解决方法:配成固体混合物。
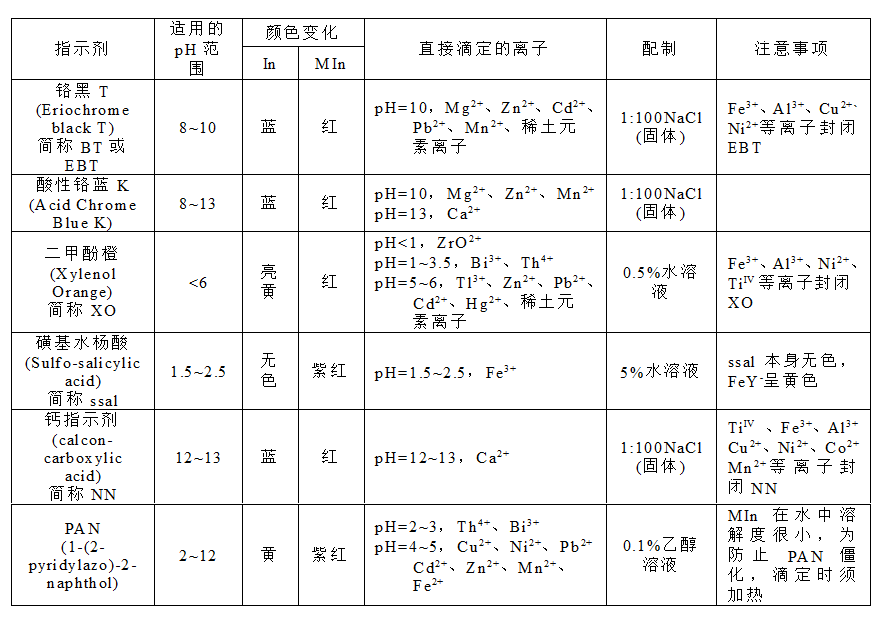
常见的金属指示剂(见附表)
9.3.4 混合离子的分别滴定
混合离子的滴定:
分别滴定其中的多种金属离子,如何进行?
(1)单一金属离子能否被准确滴定?lgCK'≥6
(2)两种金属离子能否被分别滴定?⊿lgK ≥5



