9.2酸碱滴定法
9.2.l 酸碱指示剂
9.2.1.1. 酸碱指示剂的变色原理


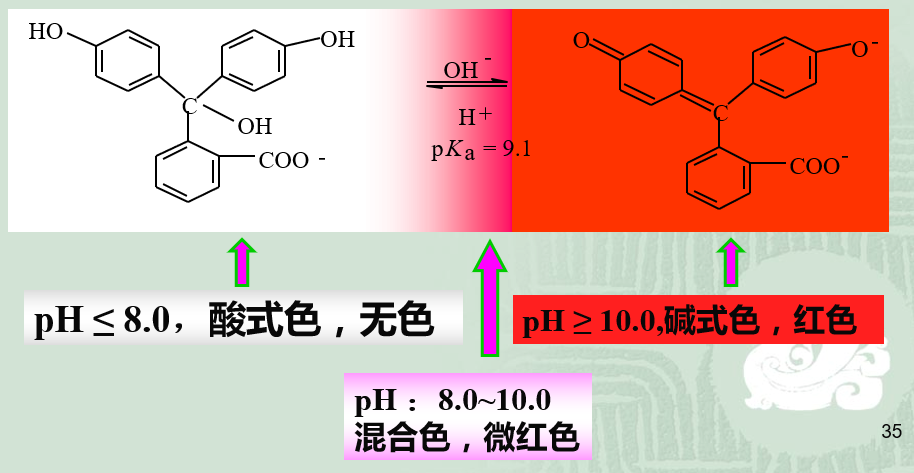
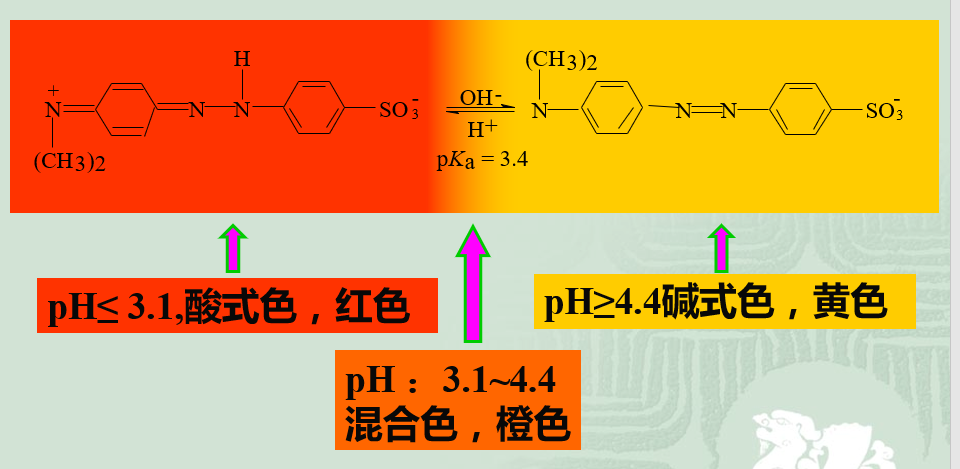
再如,甲基橙指示剂Merhyl Orange(MO)
9.2.1.2.指示剂的变色范围和变色点

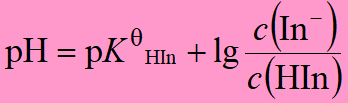
c(In-)=c(HIn)时, pH=pKHIn, 酸色和碱色的等量成分
混合色, 称为指示剂的理论变色点
c(In-)/c(HIn) ≤ 1/10时, 则pH≤ pKHIn–1,酸式色;
c(In-)/c(HIn) ≥ 10时,则pH≥ pKHIn+1,碱式色 ;
1/10< c(In-)/c(HIn) <10时,酸式和碱式的混合色。
指示剂的理论变色范围为:pH = pKHIn±1,2个pH单位
实际变色范围和理论变色范围略有差别:
例如,甲基橙, pKHIn=3.4,理论变色范围为[2.4, 4.4];
实际为[3.1, 4.4]。
原因:人的眼睛对不同颜色的敏感程度不同造成的。通常使用实际变色范围,见322页附录8.1。
9.2.1.3.混合指示剂
第一类:两种或两种以上指示剂混合而成
颜色互补,变色范围变窄,变色敏锐,利于终点判断,减小误差。
例如,溴甲酚绿—甲基红混合指示剂
第二类:指示剂加惰性染料
例如,中性红—亚甲基蓝(惰性染料)混合指示剂

pH试纸 :甲基红,溴百里酚蓝,百里酚蓝,酚酞按一定比例混合,溶于乙醇,浸泡滤纸。
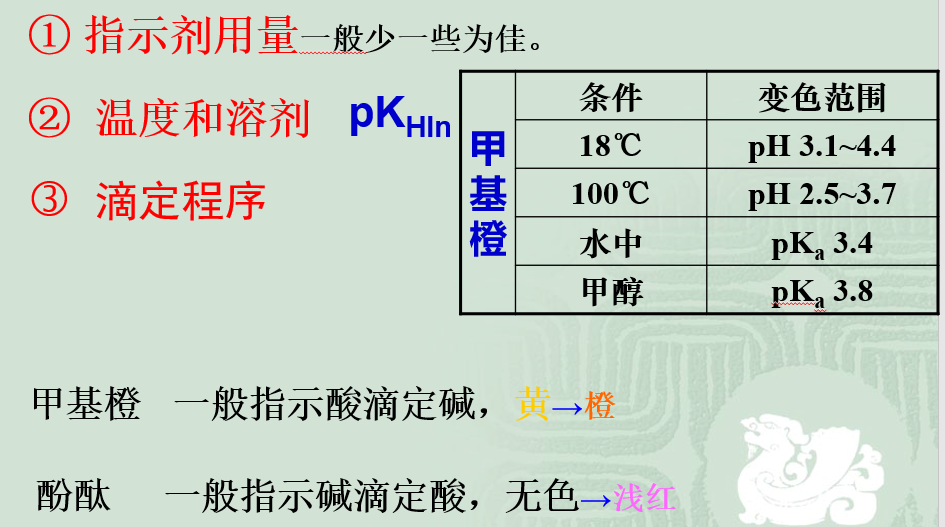
9.2.1.4.影响指示剂变色范围的因素
9.2.2 酸碱溶液中各组分的分布
溶质的总浓度(分析浓度、标签浓度)c表示,单位:mol/L。
平衡浓度,解离达到平衡时,溶质在溶液中各种型体(形式,物种),用[ ]表示,单位也是mol/L。
物料等衡式(MBE),解离达到平衡时,c=[ ]1+[ ]2+[ ]3+…
分布系数δ(distribution coefficient):平衡时溶液中某形式的平衡浓度占总浓度的分数,以δ表示,δi = []i / c。
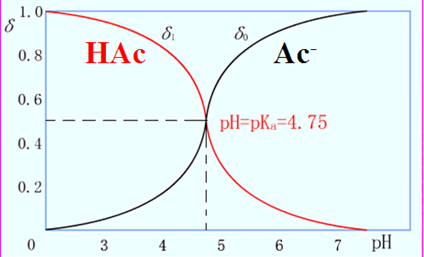
9.2.2.1一元弱酸δ的计算,以醋酸(HAc)为例
溶液中物质存在形式:HAc;Ac-,总浓度为c
设: HAc的分布系数为δ1;
Ac-的分布系数为δ0;
则:δ1=[HAc]/c = [HAc]/ ([HAc]+ [Ac- ] )
= 1 / { 1 + ([Ac- ] / [HAc])}
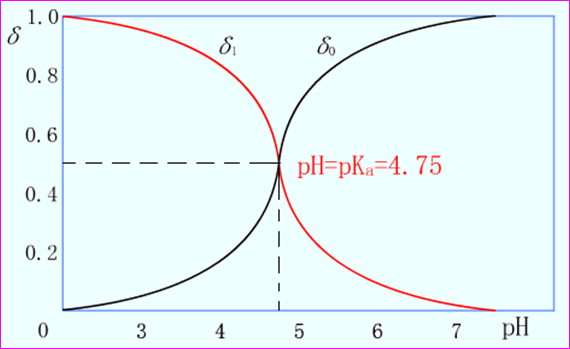
= 1/{ 1 + (Ka/[H+])} =[H+]/ ( [H+] + Ka )
δ0= [Ac-] / c = Ka/ ( [H+] + Ka )

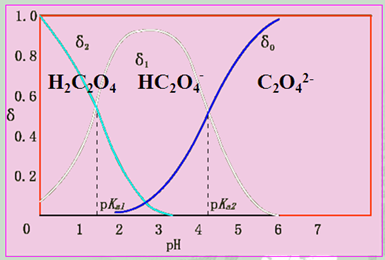
9.2.2.2二元酸δ的计算,以草酸(H2C2O4)为例:
存在形式:H2C2O4 ; HC2O4-; C2O42-;
(δ2) ; (δ1) ; (δ0) ;
总浓度:c= [H2C2O4] +[HC2O4- ] +[C2O42-]
δ2 = [H2C2O4] / c
= [H2C2O4] /[H2C2O4] +[HC2O4- ] +[C2O42-]
= 1 / { 1+[HC2O4- ] /[H2C2O4] +[C2O42-] /[H2C2O4] }
= 1 / { 1+Ka1 / [H+] + Ka1Ka2 / [H+]2 }
= [H+]2/{ [H+]2 +[H+]Ka1 +Ka1Ka2}
δ1= [H+]Ka1/{ [H+]2 +[H+]Ka1 +Ka1Ka2}
δ0= Ka1Ka2 / { [H+]2 +[H+]Ka1 +Ka1Ka2}
H2C2O4分布系数与溶液pH关系曲线的讨论:
(1) pH<pKa1时 H2C2O4为主
(2) pKa1<pH<pKa2时 HC2O4-为主
(3)pH>pKa2时 C2O4 2-为主
(4) pH=2~3时 三者共存。
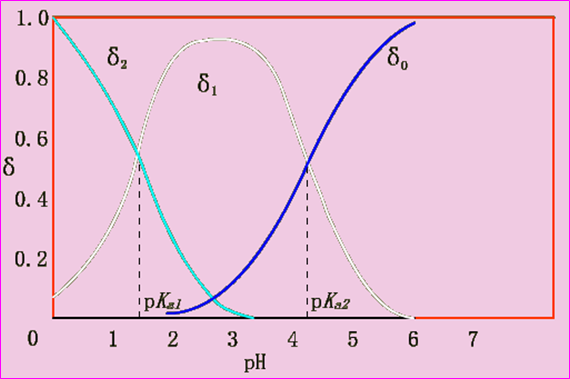
pKa1= 1.23 pKa2=4.19
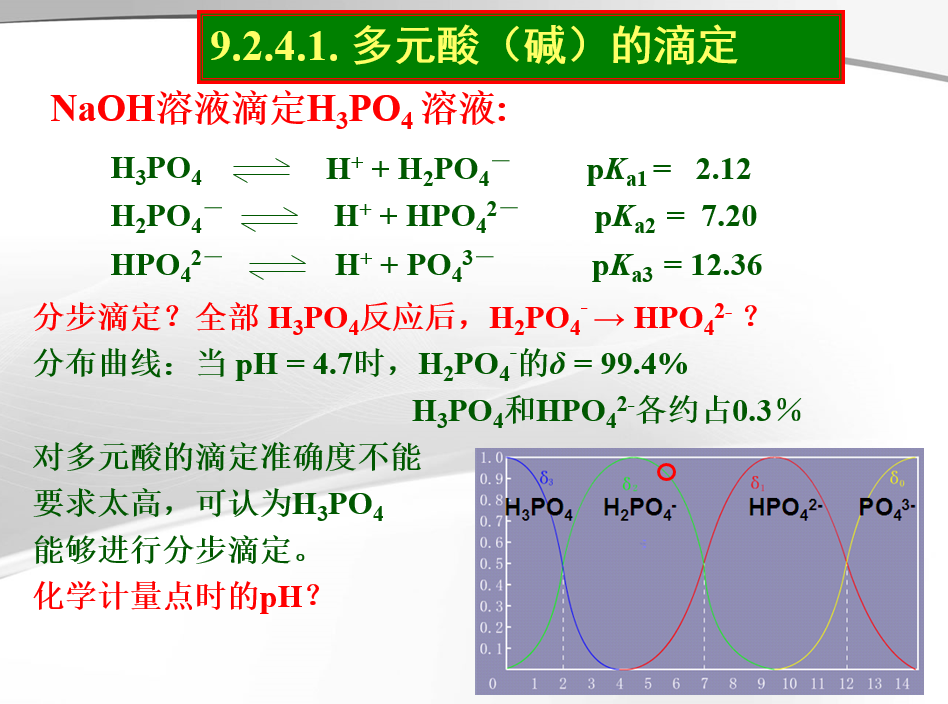
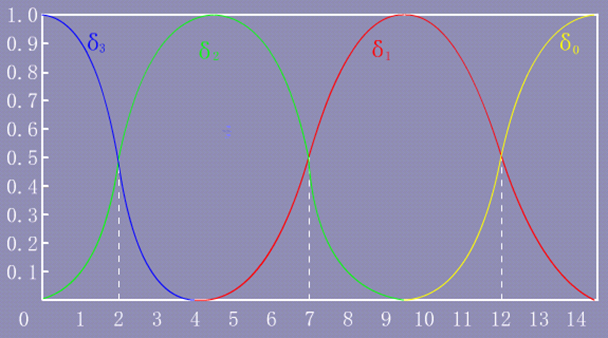
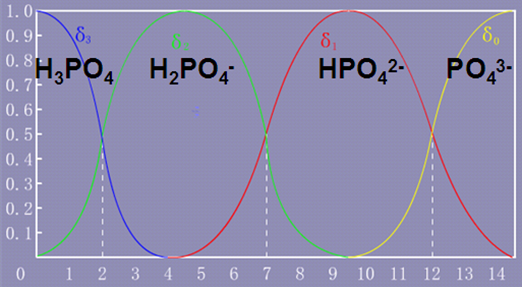
三元酸δ的计算,以H3PO4为例
四种存在形式:H3PO4;H2PO4-;HPO42-;PO43-;
分 布 系 数: δ3 ; δ2 ; δ1 ; δ0
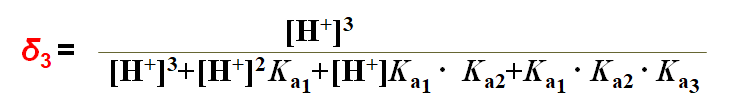
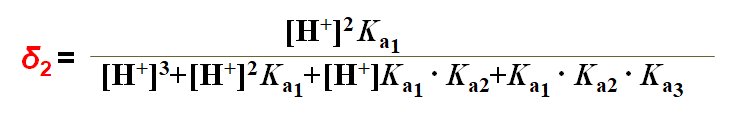
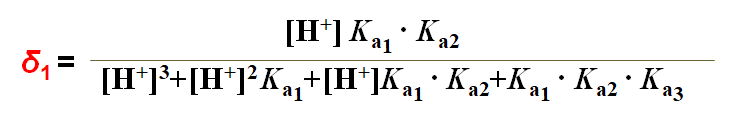
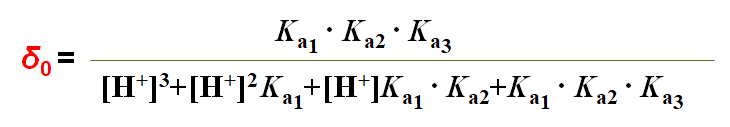
H3PO4分布曲线的讨论:
(1)pH=4.7时, δ2 =0.994 δ3 =δ1 = 0.003
(2)pH=9.8时,δ1=0.994 δ0 =δ2 = 0.003
(3)三个pKa相差较大共存现象不明显;
分布系数δ
平衡时溶液中某物种的浓度占总浓度的百分数
 9.2.3 一元酸碱的滴定
9.2.3 一元酸碱的滴定
9.2.3.1滴定曲线、滴定突跃、指示剂选择
(1)滴定曲线:以滴定剂加入量(体积或滴定百分数)为横坐标,以被滴溶液的pH值变化为综坐标做的图。
2)滴定突跃范围:计量点前后相对误差±0.1%,即滴定百分数99.9%--100.1%时,溶液pH值急剧变化区间。
3)酸碱指示剂选择:指示剂的变色范围全部或部分落在滴定的突跃范围内;指示剂变色点处于突跃范围内;或计量点处于指示剂的变色范围内。
滴定需解决三个问题:
 判断被测物质能否被准确滴定
判断被测物质能否被准确滴定
滴定过程中溶液pH值的变化情况
怎样选择最合适的指示剂
![]()
计算滴定过程中溶液pH值、绘制滴定曲线
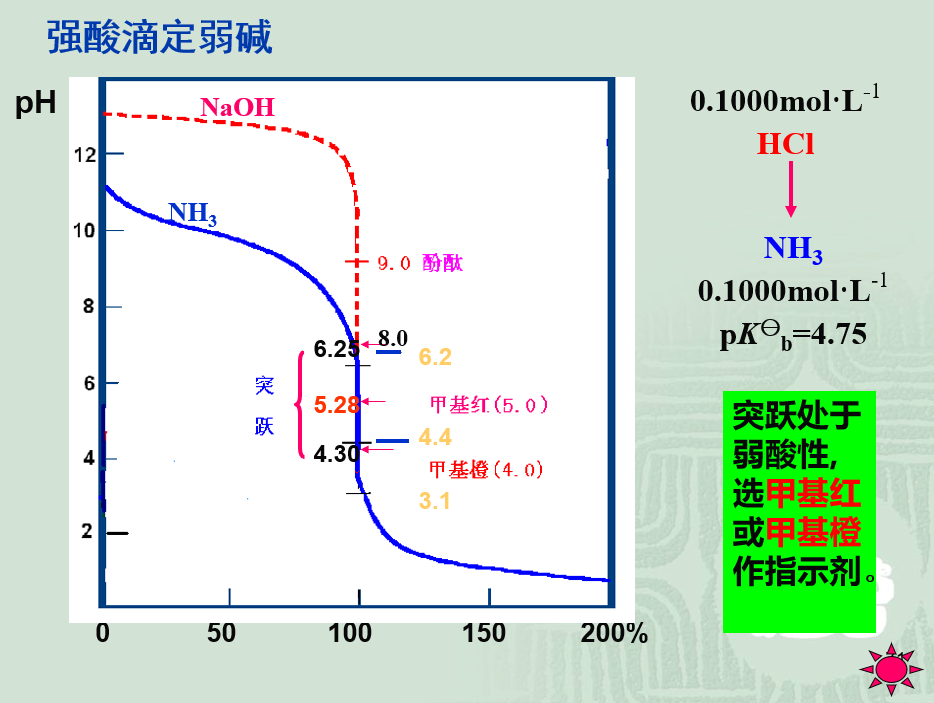
9.2.3.2.强酸强碱之间的滴定
滴定反应及其反应平衡常数
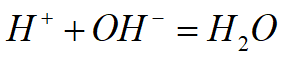
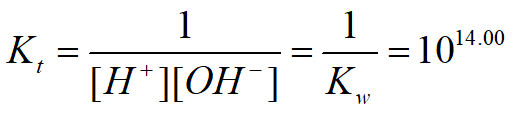
酸碱滴定中完全程度最高的反应。
0.1000mol·L-1 NaOH 滴定 20.00mL 0.1000mol·L-1 HCl
滴定过程
两点(起点、计量点),
两段(化学计量点前、化学计量点后),
滴定情景:谁装滴定管中,谁在锥形瓶中,谁的pH在变?
1. 滴定前(起点)
![]()
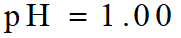
0.1000mol·L-1 NaOH 滴定 20.00mL 0.1000mol·L-1 HCl
2. 至化学计量点前
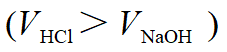
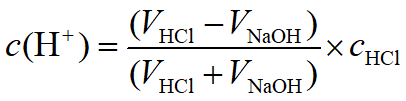
假设滴入19.98mL的NaOH溶液
(相对误差为-0.1%)
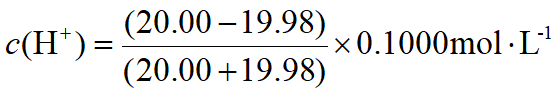
![]()
![]()
0.1000mol·L-1 NaOH 滴定 20.00mL 0.1000mol·L-1 HCl

![]()
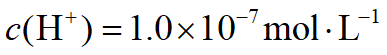
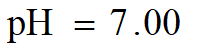
4. 化学计量点后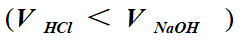
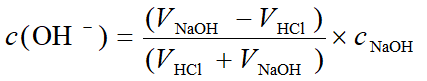
假设滴入20.02mL的NaOH溶液
(相对误差为+0.1%)
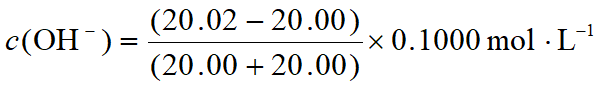
![]()
![]()
![]()
0.1000mol·L-1 NaOH 滴定 20.00mL 0.1000mol·L-1 HCl
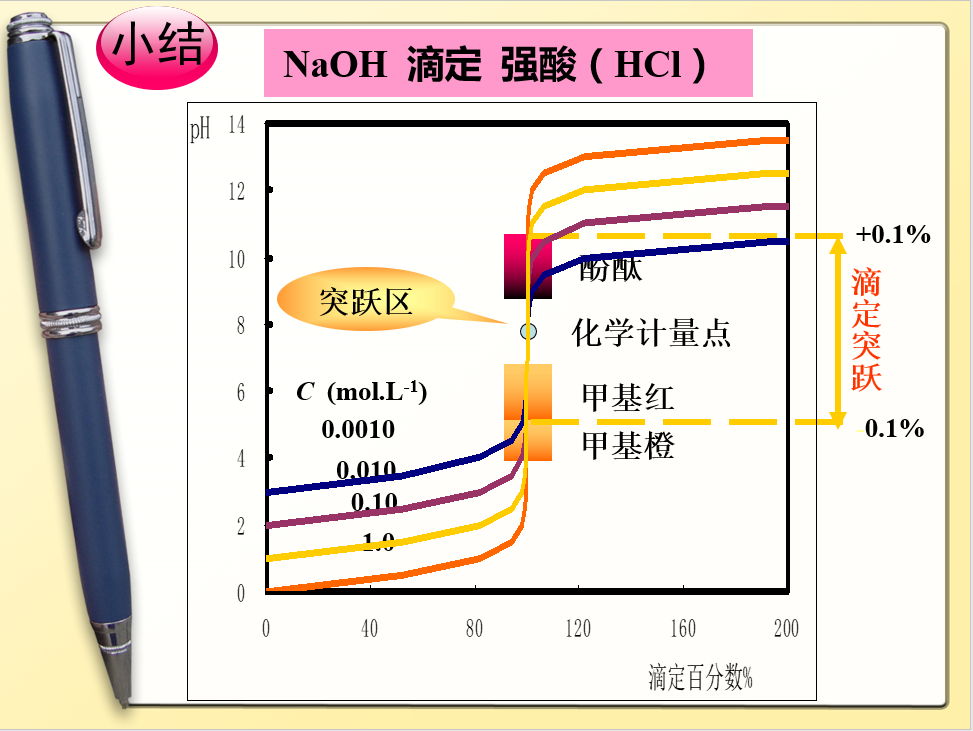
滴加体积:0~19.98 mL; DpH=4.40-1.00=3.40
滴加体积:19.98 ~20.02 mL;
0.04mL,约1滴,DpH=9.70-4.30=5.40,
这就是pH突跃。
0.1000mol·L-1NaOH滴定20.00mL 0.1000 mol·L-1HCl
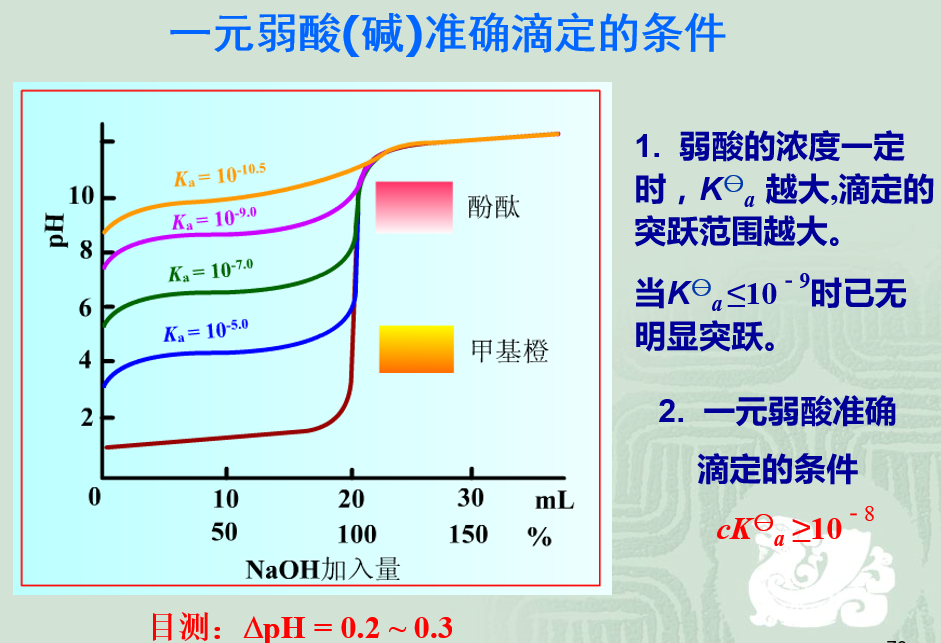
9.2.3.3 一元弱酸(碱)的滴定
0.1000 mol·L-1 NaOH 滴定20.00mL 0.1000 mol·L-1HAc
滴定过程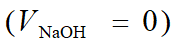
1. 滴定前
溶液中的H+主要来自于HAc的解离
由于cKya≥20KyW 、c /Kya≥105,
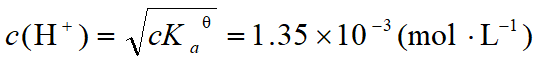
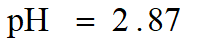
与强酸相比,滴定起点的pH值抬高。
0.1000 mol·L-1 NaOH 滴定20.00mL 0.1000 mol·L-1HAc
2. 至化学计量点前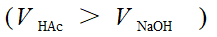
此时,形成了HAc-Ac-缓冲体系
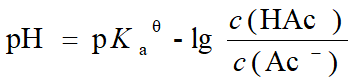
假设滴入19.98mL的NaOH溶液
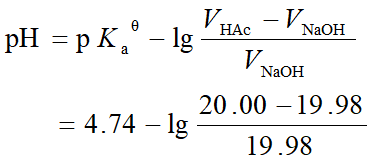
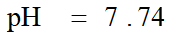
3. 化学计量点时
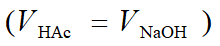
滴入20.00mL的NaOH溶液,HAc完全反应生成NaAc
由于cKyb≥20KyW、c /Kyb≥105,
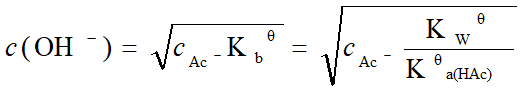
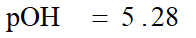
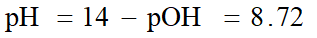
4. 化学计量点后
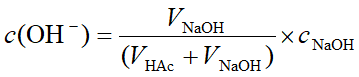
假设滴入20.02mL的NaOH溶液
(相对误差为+0.1%)
滴加体积:0~19.98 mL; DpH=1.00-4.40=3.40
滴加体积:19.98 ~20.02 mL;
0.04mL,约1滴,DpH=4.30-9.70=5.40
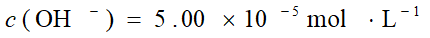
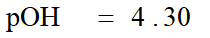
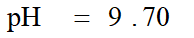
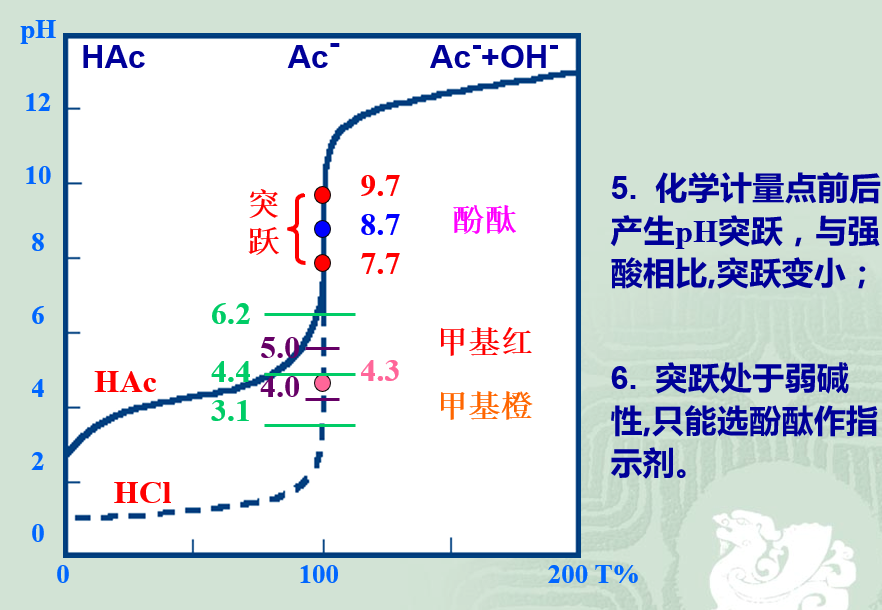
滴加体积:0~19.98 mL; DpH=7.74-2.87=4.87
滴加体积:19.98 ~20.02 mL;DpH=9.7-7.7=2
与NaOH滴定HCl相比,起点pH值提高,滴定突跃范围变小。
0.10 mol·L-1NaOH滴定20.00 mL 0.10 mol·L-1HAc![]()

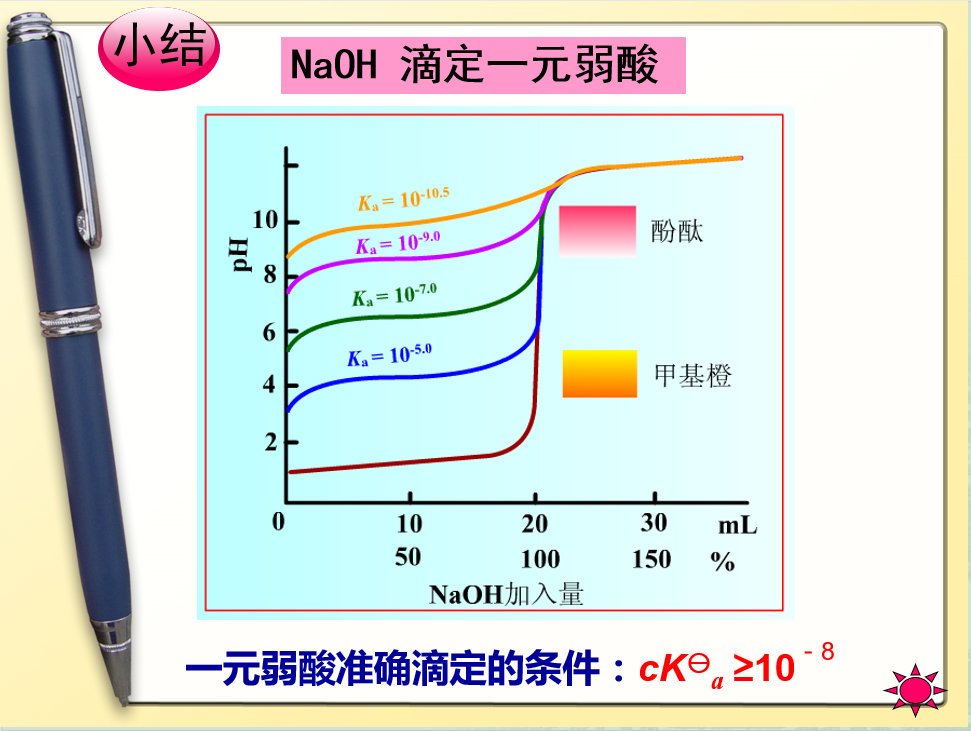
强碱滴定弱酸滴定曲线
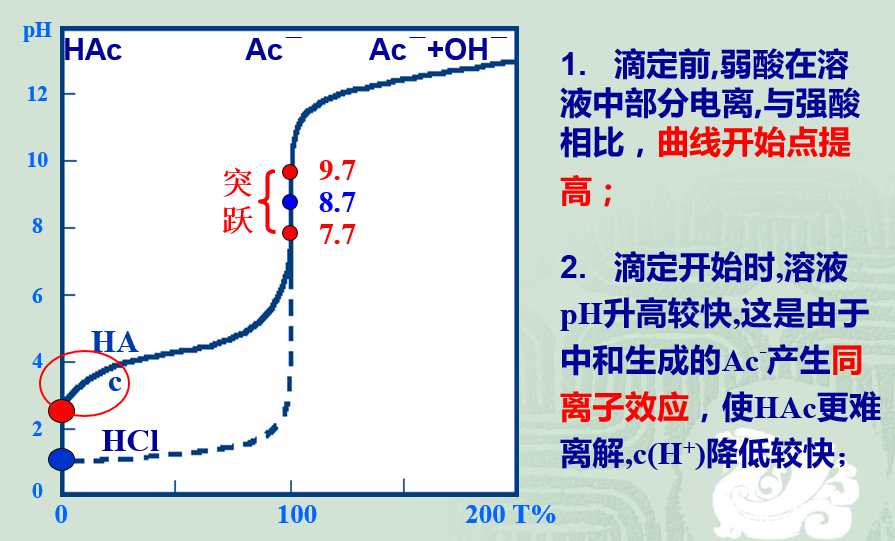
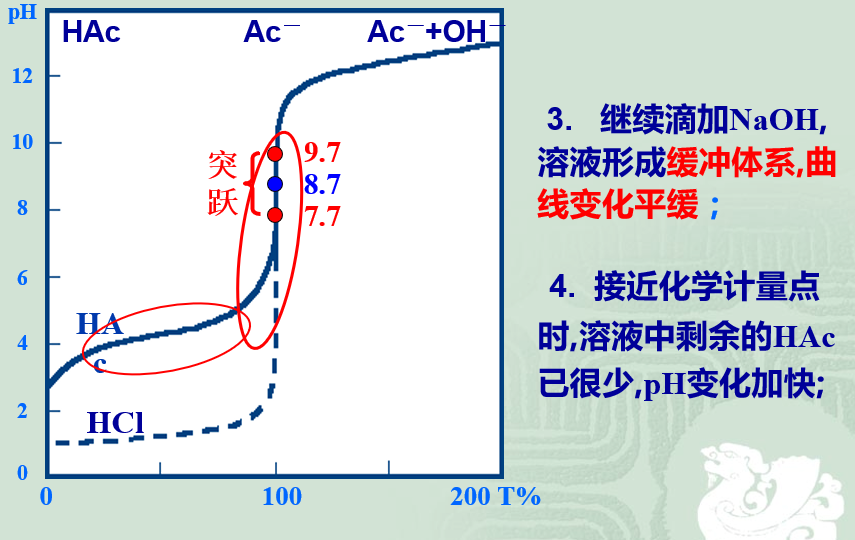
9.2.4多元酸(碱)、混合酸(碱)的滴定