9.1 滴定分析法概论
第9章 滴定分析法-1.ppt(下载附件 4.83 MB)滴定分析:将一种已知准确浓度的试剂溶液,滴加到一定体积的被测物质的溶液中,直到所加的试剂与被测物质按化学计量关系定量完全反应为止,然后根据标准溶液的浓度和体积,计算出被测物质的含量。滴定管读数时一定估至小数点后第2位。至少量取20mL,以保证读数误差≤0.1%,[0.02/V ≤0.1%]
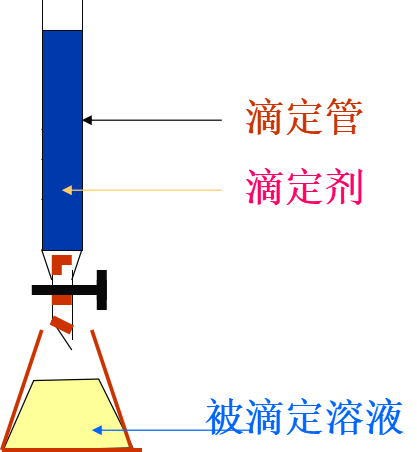
标准溶液:已知准确浓度的试剂溶液。
滴定:将标准溶液通过滴定管滴加到待测组分溶液中的过程。
滴定反应:滴定时进行的化学反应。
例:HCl + NaOH = NaCl + H2O
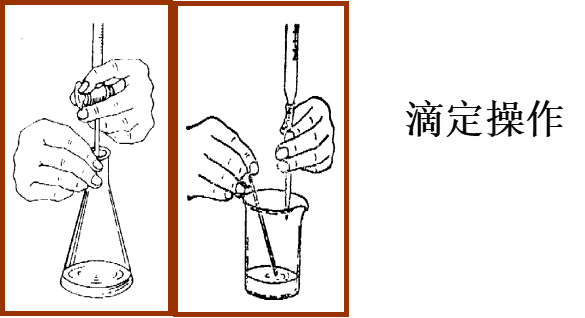
化学计量点:当所加入的标准溶液与被测物质完全反应所处于的状态,以sp 进行表示(stoichiometric point)。
滴定终点:化学剂量点一般依指示剂颜色变化来确定,在滴定中指示剂颜色变化那一点,简称终点, 用ep 表示。
指示剂:分析中用于指示终点的试剂。
9.1.1 滴定分析法的分类
按化学反应类型分类:

9.1.2 滴定分析法对化学反应的要求和滴定方式
1、按一定化学反应式进行,不发生副反应、反应定量、完全大于等于99.9%
2、反应迅速
3、具有合适的确定终点的方法
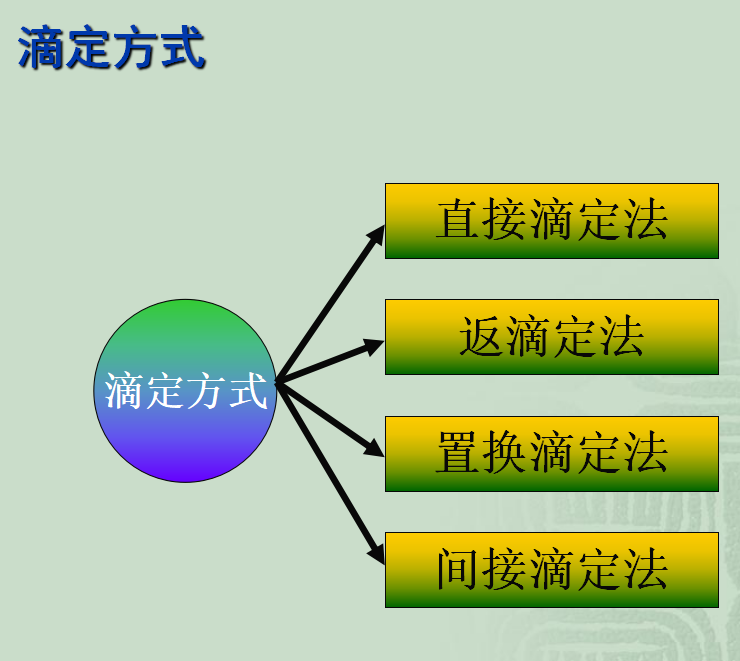
直 接 滴 定 法
能满足滴定分析3个要求的反应

返 滴 定 法
当反应较慢或被测物是固体时,可先加入过量的标准溶液,待反应完成后,再用另一种标准溶液滴定剩余的第一种标准溶液。
反应较慢
置 换 滴 定 法
先用适当试剂与待测物质反应,定量置换出另一种物质,再用标准溶液去滴定该物质的方法。
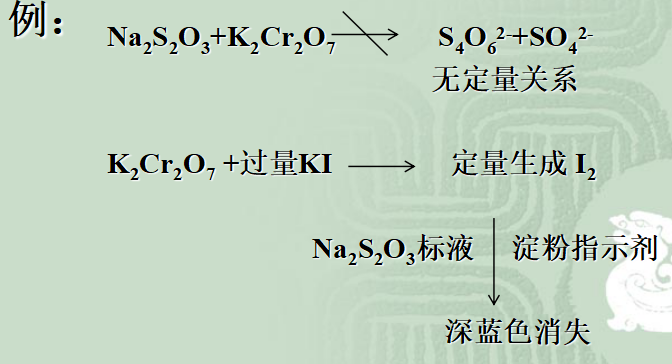
间 接 滴 定 法
概念:不能与滴定剂直接反应的物质,有时可以通过另外的化学反应,以滴定法间接进行测定。
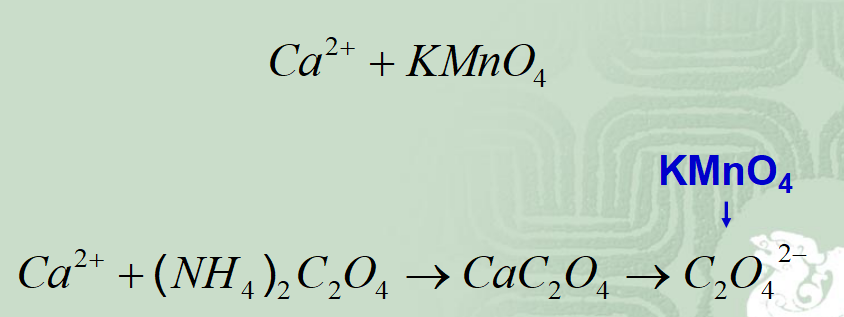
9.1.3 标准溶液的配制和浓度表示方法
标准溶液: 具有准确浓度的溶液
1. 直接配制:CaCO3、 KHC8H4O4、Na2C2O4
2. 标定法配制:NaOH、HCl、EDTA、KMnO4
基准物质:用以直接配制标准溶液或标定溶液浓度的物质
1. 组成与化学式相符( H2C2O4·2H2O、NaCl );
2. 试剂纯度 > 99.9%;
3. 稳定( Na2CO3、CaCO3、Na2C2O4等);
4. 反应时按一定的化学计量关系进行,没有副反应。
5. 有较大的摩尔质量;
v有较大的摩尔质量:
如MA=300, MB=150,
若同是一个质量,天平的误差为0.0002g,
[要求: 称量相对误差≤0.1%,称量的质量m≥0.2g] B的相对误差较大。


标准溶液的配制
直接法:两准得一准
1. 用分析天平称量基准物质;
2. 溶解;
3. 转移至容量瓶定容;
4. 计算出标准溶液的准确浓度。

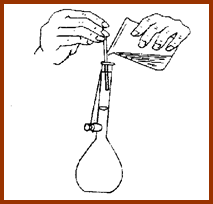
间接法(标定浓度):
1.配制溶液
配制成近似所需浓度的溶液。
2.标定(standardization)
浓度0.1 mol/L 左右,滴定剂消耗体积在 20~30mL 之间,由此数据可计算称取试样量的上限和下限。
或另一种已知浓度的标准溶液来准确测定滴定液浓度的操作过程。
3.计算浓度 由基准物的质量(或另一种已知浓度的标准溶液体积、浓度),计算确定之。
9.1.4 滴定分析中的基本计算
1、分析化学中常用的量和单位

2、标准溶液浓度的表示方法
物质的量的浓度
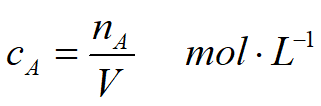
基本单元:可以是分子、原子、离子及其他粒子或这些粒子的某种特定组合。
![]()
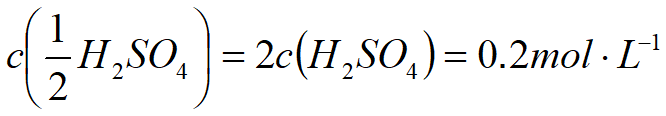
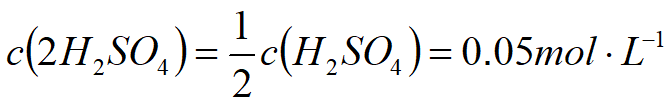
通式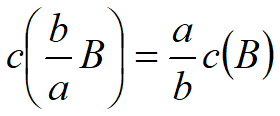
正确地选择基本单元
酸碱反应 :以酸给出1个H+或碱得到1个H+的粒子或粒子的特定组合作为反应物的计量基本单元;
例如,H2SO4+2NaOH==Na2SO4+2H2O
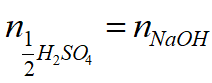
氧化还原反应 :以氧化剂得到1个电子或还原剂失去1个电子的粒子或粒子的特定组合作为反应物的化学计量基本单元;
例如,2MnO4-+5C2O42-+16H+===Mn2++10CO2+8H2O
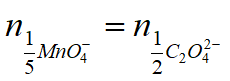
3、滴定度:按照反应式完全反应后,每ml标准溶液相当于被测物质的质量g。【或每mL标准溶液所含溶质的克数】。TA/B:g/ml, TB: g/ml
TFe2+/K2Cr2O7 = 0.005000 g/ml: 每ml K2Cr2O7可以滴定0.005000g Fe2+.
若V(K2Cr2O7)= 21.50 ml,则相当于Fe的质量为:
![]()

![]()
滴定度与物质的量浓度的转换: 以TFe2+/K2Cr2O7 = 0.005000 g/ml 为例:
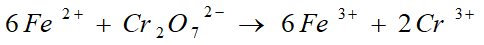
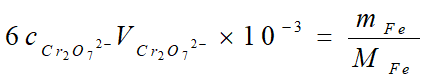
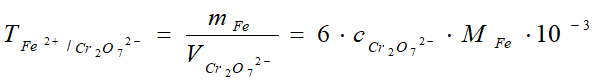
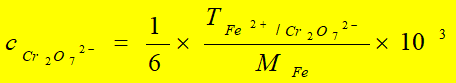
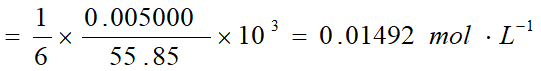
例题:
求 0.1000 mol·L-1 NaOH 标准溶液对 H2C2O4 的滴定度。
解:NaOH 与 H2C2O4 的反应为:
H2C2O4 + 2 NaOH = Na2C2O4 + 2H2O
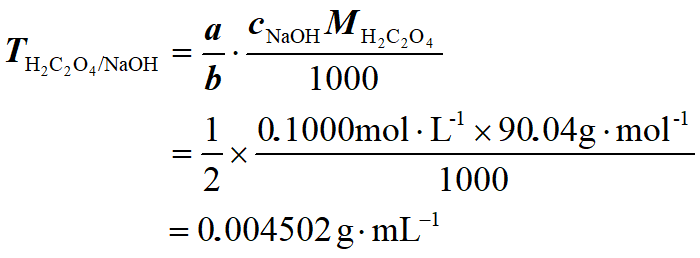
例:
有一KMnO4标准溶液,浓度为0.02010 mol·L-1,求其 TFe / KMnO4和TFe2O3 / KMnO4 。如果称取试样0.2718g,溶解后将溶液中的Fe3+还原成Fe2+,然后用KMnO4标准溶液滴定,用去26.30mL,求试样中Fe、Fe2O3的质量分数。
解; 5Fe2+ + MnO4-+ 8H+ = 5Fe3+ + Mn2+ + 4H2O
nFe = (5/1) n KMnO4
1Fe2O3→2Fe → nFe2O3= nFe/2
nFe2O3 = (5/2) n KMnO4

相关计算
一、被测物与滴定剂之间物质的量的关系—即计量关系
滴定剂与被测物之间的反应式为:
a A + b B c C + d D
当滴定到化学计量点时,a摩尔被测物A与b摩尔滴定剂B作用完全则:nA:nB=a:b
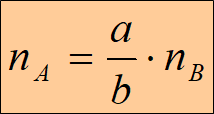
1.若待测物A为液体,滴定剂B为液体,即液-液反应,则:
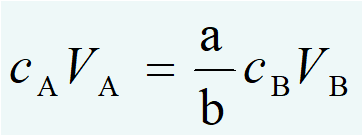
2.若待测物A为固体,滴定剂B为液体,即固-液反应,则:

(二)间接滴定与置换滴定(涉及到多个反应)
例:以 KBrO3 为基准物,测定 Na2S2O3 溶液浓度。
1. KBrO3 与过量的 KI 反应析出 I2 :
BrO3- + 6 I- + 6H+ = 3 I2 + Br- + 3H2O
n(BrO3-) = 1/3 n(I2)
2. 用Na2S2O3 溶液滴定析出的 I2
2 S2O32- + I2 = 2 I- + S4O62-
n(I2 ) = 1/2 n(S2O32-)
3. KBrO3 与 Na2S2O3之间物质的量的关系为:
n(BrO3-) = 1/3 n(I2 ) = 1/6 n(S2O32-)
(cV)S2O32- = 6(m/M)BrO3 -
二、被测物的质量分数的计算
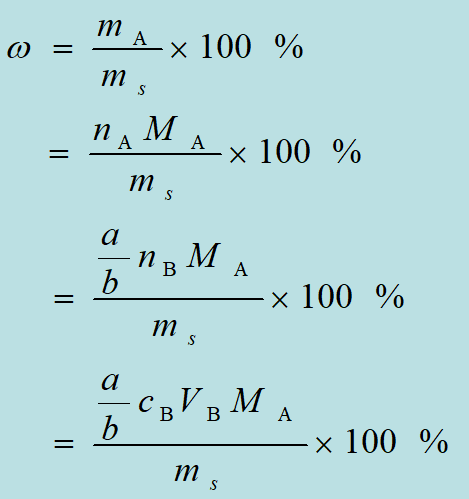
式中ω为质量分数,ms为试样质量。


