7.3 沉淀溶解平衡
第7章 水溶液中的解离平衡7.3.ppt(下载附件 3.99 MB)
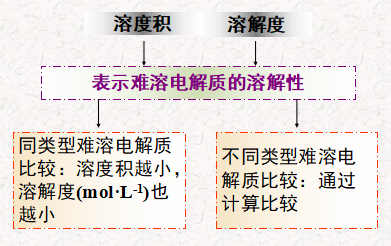
溶解度
定义:一定温度下,达到溶解平衡时,一定量的溶剂中所含溶质的质量称为溶解度,用符号 S表示。
单位: g/100gH2O; g · L-1; mol · L-1
7.3.1 溶度积常数![]()
1.沉淀-溶解平衡的引出
在一定温度下,将难溶电解质晶体放入水中时,就发生溶解和沉淀两个过程。
2. 溶度积常数表达式
一定条件下,当溶解和沉淀速率相等时,便建立了一种动态的多相离子平衡,可表示如下:

7.3.2 溶解度和溶度积的换算


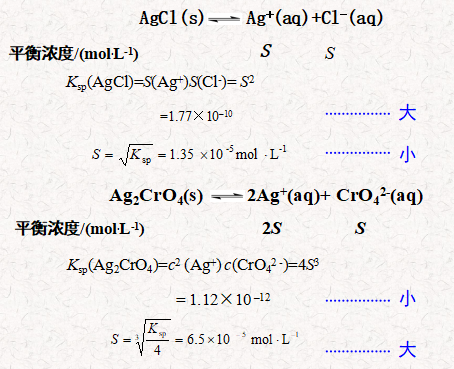
7.3.3 影响难溶电解质溶解度的因素



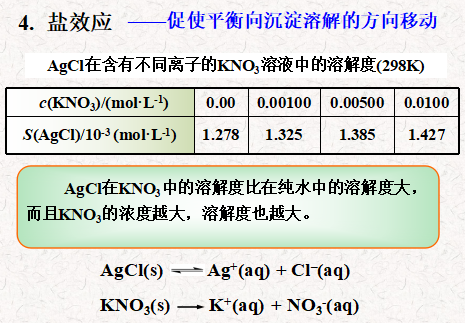

5. 酸效应
6. 配位效应
7. 氧化还原效应

![]()
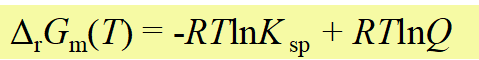
![]()
![]()
![]()


沉淀的生成、溶解与转化
7.3.4.1 沉淀的生成
沉淀生成的条件: J > Ksp,沉淀完全的界定,沉淀后溶液中被沉淀离子浓度≤10-5mol/L
促使沉淀生成的常用方法:
(1) 加入沉淀剂:沉淀剂选择、沉淀剂用量
(2) 改变溶液的条件:如溶液的pH值

7.3.4.2分步沉淀
由于难溶电解质的溶解度不同,加入沉淀剂后溶液中发生先后沉淀的现象。
对同一类型的沉淀,Kosp越小越先沉淀,且Kosp相差越大分步沉淀越完全。
对不同类型的沉淀,其沉淀先后顺序要通过计算出溶解度S才能确定。
两种离子通过沉淀达到分离的界定,加入沉淀剂后溶液中发生先后沉淀,当另一种离子开始沉淀时,先发生沉淀的离子浓度已经≤10-5mol/L。


7.3.4.3沉淀的溶解
当 J<Kosp 时,沉淀发生溶解
使J减小的方法有:
(1)酸碱反应,生成弱电解质或气体。
(2)利用氧化还原方法降低某一离子的浓度。
(3)生成配合物。
例 4. 100mL 0.10mol.L-1 MgCl2 和 100mL 0.10mol.L-1 NH3·H2O 相混合,(1) 是否有沉淀生成?(2)为不使Mg(OH)2 沉淀析出,至少应加入多少克NH4Cl(假定加入NH4Cl后溶液的体积不变)?
解:(1)求出混合后溶液中Mg2+浓度及由NH3·H2O 解离出的OH-浓度,利用溶度积规则判断是否有Mg(OH)2 沉淀生成。
(2)思路一,先由溶度积规则求出沉淀溶解时 [OH-],由NH3H2O解离平衡求出NH4Cl浓度。或利用缓冲溶液计算公式。
(2)思路二,利用Mg(OH)2 +2NH4+=Mg2++2NH3H2O总平衡进行计算,总平衡常数可以由组成总平衡的2个平衡常数得出。
7.3.4.4 沉淀的转化




