第二课时强电解质溶液
上一节
下一节
7.2 强电解质溶液
第7章 水溶液中的解离平衡.ppt(下载附件 3.99 MB)
一、电解质和非电解质
电解质:在水溶液中或在熔融状态下能导电的化合物
根据电离程度大小,可将电解质分为:

电离平衡
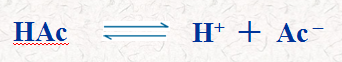
电离平衡:正、逆反应速率相等时,电解质分子和离子间达到的动态平衡

| 电解质 | 表观解离度 |
| HCl | 92% |
| HNO3 | 92% |
| NaOH | 84% |
| NaCl | 84% |
| KNO3 | 83% |

Ø 任何强电解质在水溶液中都是以离子形式存在,其理论解离度应为100%。Ø电导实验的测定结果似乎证明强电解质并不是完全解离。
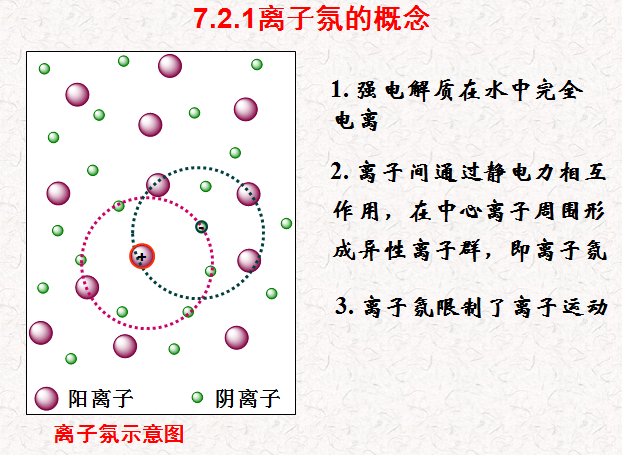
由于离子氛的影响,实验测得的强电解质的解离度并不是真正意义的解离度,因此这种解离度被称为“表观解离度”。
离子浓度越大,离子所带电荷越多,离子间的相互作用越强,表观电离度越小。
离子浓度越小,离子所带电荷越少,离子氛影响越小,表观解离度越大,越接近100%。
7.2.2活度和活度系数
活度:电解质溶液中,实际上可起作用的离子浓度
符号:a
活度与浓度的关系:
γi : 离子的活度系数,是溶液中离子间相互作用力大小的反映,通常小于1。
讨论:Ø 溶液越浓,离子电荷越高,离子间相互作用越大,γi越小,活度和浓度差距越大
Ø稀溶液,离子间相互作用越弱,γi→ 1,一般情况下,稀溶液中,离子间的作用较小,可以忽略,r=1,a=c


