第7章 水溶液中的解离平衡
7.1 酸碱平衡
7.1.1 酸碱质子理论
7.1.2 酸碱溶液的pH计算
7.1.3 同离子效应与缓冲溶液
◆ 最初
酸:有酸味,能使蓝色石蕊试纸变红的物质
碱:有涩味、滑腻感,使红色石蕊试纸变蓝的物质
◆ 酸碱理论的发展:
1884年,S.Arrhenius提出酸碱电离理论;
1923年,J.N.Brönsted、 T.M.Lowry分别提出酸碱质子理论;
1923年,Lewis 提出酸碱电子理论。
酸碱电离理论:
酸:水溶液中,能电离出H+ 的物质;
碱:水溶液中,能电离出OH- 的物质。
酸碱(中和)反应实质:H+ + OH- ⇌ H2O
▲ 意义:
1、首次赋予酸碱以科学的定义,是对酸碱的认识从现象到本质的飞跃。
2、对化学发展起到了积极作用,目前仍普遍应用。
▲ 局限性:把酸、碱局限于水溶液;
把碱限制为氢氧化物。
7.1.1 酸碱质子理论
(1) 酸碱定义:
酸:凡是能释放出质子(H+)的分子或离子。
碱:凡是能与质子(H+)结合的分子或离子。
即:酸(质子酸) —— 质子的给予体;
碱(质子碱) —— 质子的接受体。
两性物质:既能给出质子又能接受质子的物质。

酸碱反应的实质
根据酸碱质子理论,酸和碱成对存在,酸给出质子,必须有接受质子的碱存在,质子才能从酸转移至碱。因此,酸碱反应的实质是两个共轭酸碱对之间的质子转移反应,可用通式表示为:
酸1 + 碱2 ⇌ 酸2 + 碱1
①酸碱中和反应、水解等都是质子转移反应
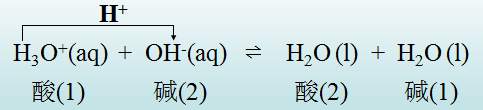
(2) 酸碱的强度与酸碱解离常数
● 酸和碱的强度是指酸给出质子的能力和碱接受 质子的能力的强弱。
给出质子能力强的物质是强酸,接受质子能力强的碱是强碱;反之,便是弱酸和弱碱。
酸碱的本性
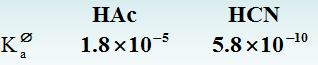
Ka为酸的解离常数, Ka越大酸性越强。 Kb为碱的解离常数, Kb越大碱性越强。
酸性:
HClO4 > H2SO4 > H3PO4 > HAc > H2CO3 > NH4+ > H2O
碱性:
ClO4- < HSO4- < H2PO4- < Ac- < HCO3- < NH3 < OH-
酸或碱本身给出质子或接受质子的能力,在具有共轭关系的酸碱对中,它们的强度是相互制约的。酸强,其共轭碱就弱;酸弱,其共轭碱就强。
溶剂的影响
质子酸和质子碱的酸碱性要通过溶剂分子转移质子来体现,同一种酸在不同的溶剂中,呈现出不同的强度。
如HNO3:
HNO3 + H2O ⇌ H3O+ + NO3- (HNO3为强酸)
HNO3 + HAc ⇌ H2Ac+ + NO3- (HNO3为弱酸)
HNO3 + H2SO4 ⇌ H2NO3+ + HSO4- (HNO3为碱)
所以,讨论酸碱的相对强度,必须以同一溶剂作为比较标准。
酸碱质子理论与电离理论相比,扩大了酸和碱的范畴,增加了离子酸和离子碱,排除了“盐”的概念。在酸碱半反应通式中,质子从一种物质酸转移到另一种物质碱上,故反应可在水溶液中,也可在非水溶剂或气相中进行,扩大了酸碱反应的范围,酸碱可以是阳离子、阴离子,也可以是中性分子。
溶剂水的作用
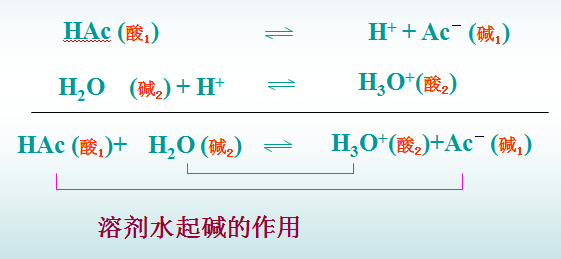
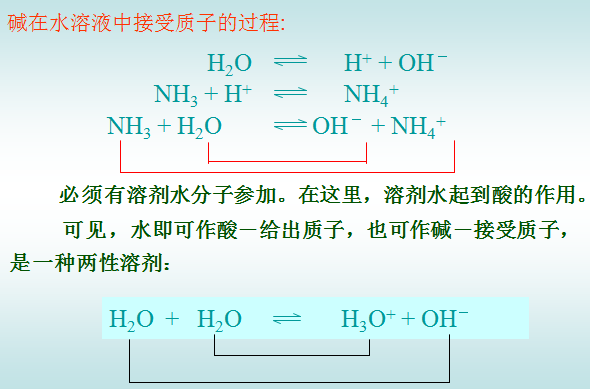
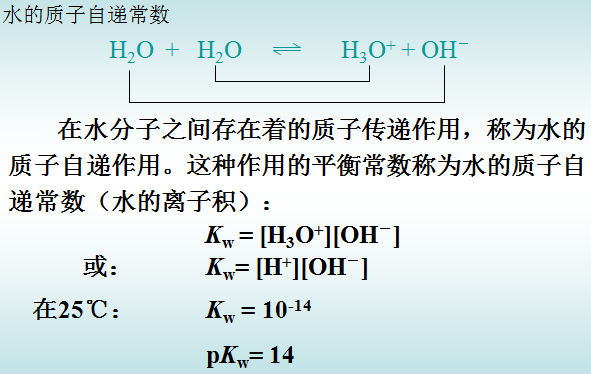
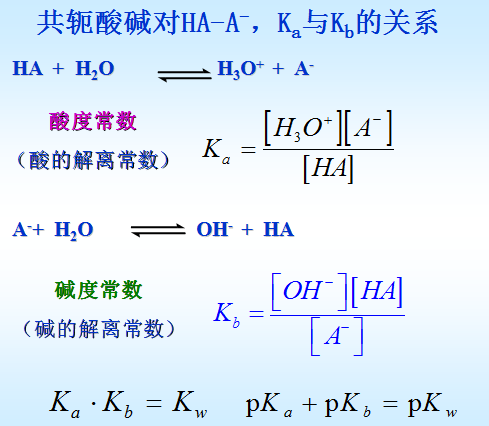

n元酸的共轭酸碱对Ka与Kb 的关系
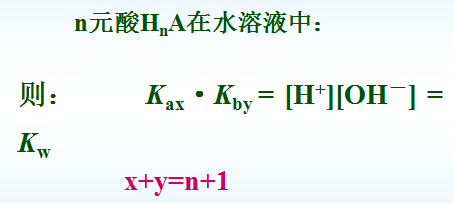
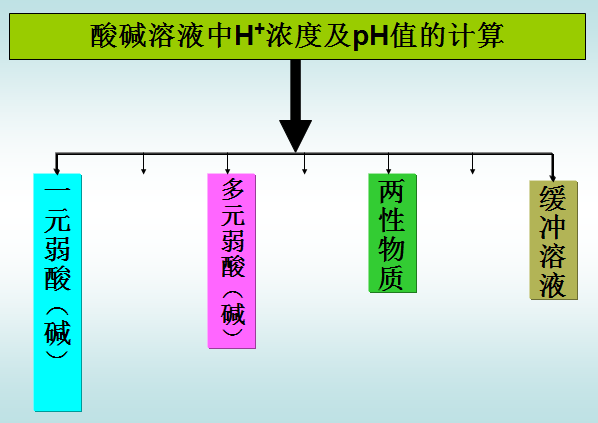
7.1.2 酸碱溶液的pH计算
7.1.2.1质子条件式
一、溶液中平衡关系式
 反应平衡式,即平衡常数表达式
反应平衡式,即平衡常数表达式
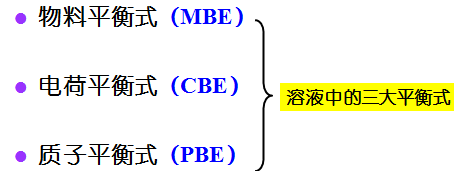
质子条件式(PBE)
平衡时,酸失去的质子数与碱得到的质子数一定相等。
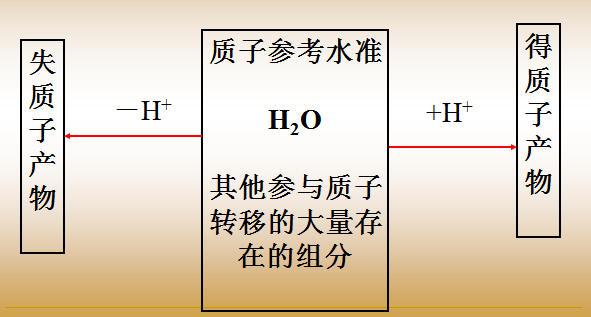
写PBE时,首先要确定零水准(大量存在并且参与质子转移的物质),然后根据零水准得失电子情况写出等式。
质子条件 (proton balance equation, PBE)
准确反映整个平衡体系中质子转移的严格数量关系式。列出质子条件的步骤:
(1) 选择参考水平(大量存在, 参加质子转移)
(2) 判断质子得失
(3) 总的得失质子的物质的量(单位mol)应该相等,列出的等式([ 各种型体平衡浓度]的等式),即为质子条件。
列列出质子条件的简易方法
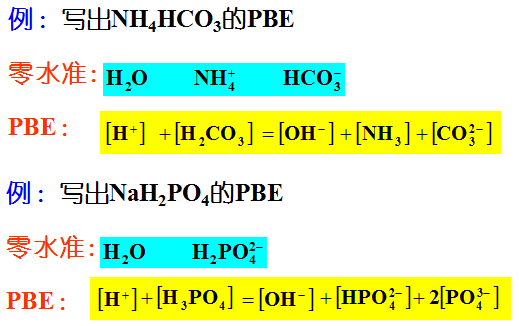


• 例1 计算0.010mol·L-1HAc溶液的pH?Ka = 1.80×10-5• 解:cKa>10Kw,c/Ka>105,采用最简式(4)计算:•••
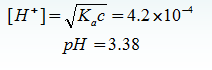
例2 计算0.10mol·L-1一氯乙酸溶液的pH?Ka = 1.40×10-3• 解: cKa>10Kw,c/Ka<105,采用近似式(2)计算:
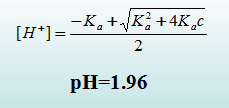
•例3 计算1.0×10-4mol·L-1HCN溶液的pH? Ka = 6.2×10-10• 解:cKa<10Kw,但c/Ka>105,采用近似式(3)计算:
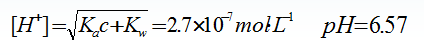
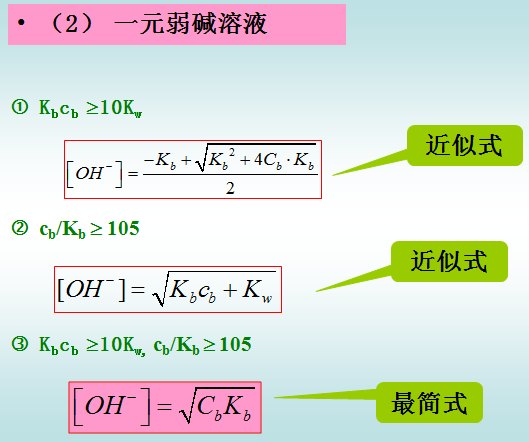
•例4 计算0.10mol·L-1NH3溶液的pH?(Kb = 1.80×10-5• )解:cKb>10Kw,c/Kb>105,用最简式计算:
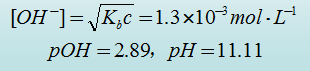
多元酸(碱)溶液
多元酸(碱)溶液与一元酸(碱) pH计算类似,满足条件时,可将多元酸碱看作一元酸碱来处理,否则,需考虑水解离、多级解离等,可采用迭代法计算处理。
7.1.2.3、两性物质溶液pH值的计算
•酸式盐(如NaHA)
离子条件:[H+] + [H2A] = [A2-] + [OH-]
[H+] = [A2-] + [OH-]-[H2A]
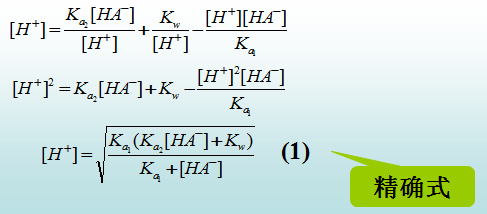






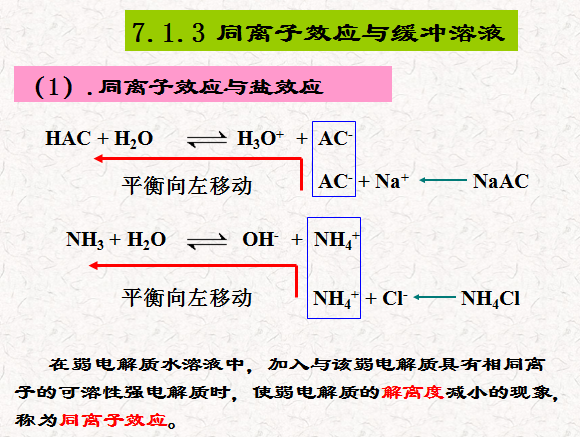
在弱电解质水溶液中,加入与该弱电解质没有相同离子
的可溶性强电解质时,使弱电解质的解离度增大的现象,称
为盐效应。
例如:在0.10mol·L-1HAc溶液中加入固体NaCl,使其浓
度为0.10mol·L-1,则溶液中的 [H+]由1.32×10-3mol·L-1增大
为1.82×10-3mol·L-1,HAc的解离度由1.32%增大为1.82%。
(2) . 缓冲溶液
•样品1:0.10mol·L-1 NaCl溶液 • 样品2:含 HAc和 NaAc均为0.10mol·L-1的混合溶液• 操作:分别滴加强酸 1mLHCl(0.10 mol·L-1)• 观察现象:pH的变化
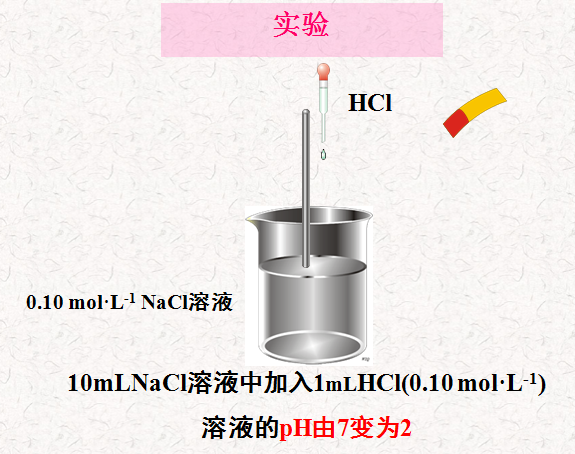
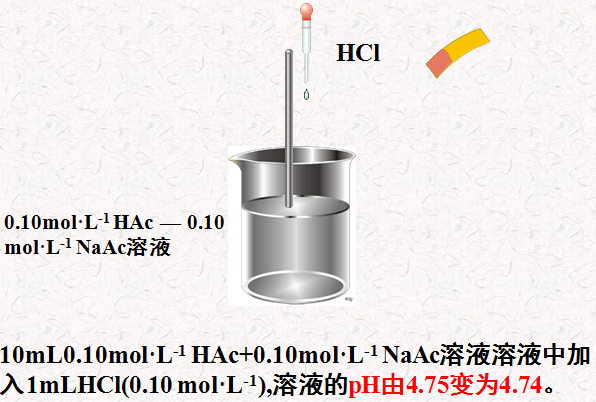
•结论 • HAc-NaAc混合溶液具有抵抗外来少量强酸、强碱而保持pH基本不变的能力。
缓冲溶液
1.定义:能够抵抗外加少量酸碱或水的稀释, 而
保持pH基本不变的溶液称为缓冲溶液。

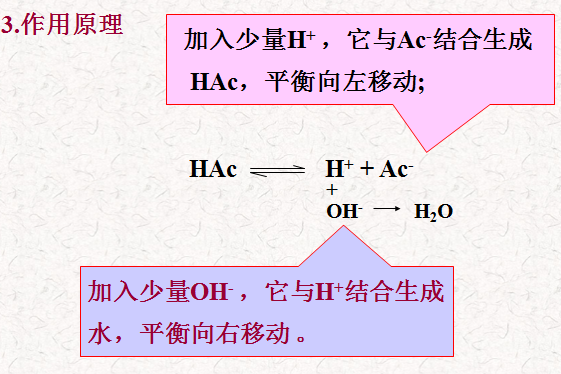


5. 缓冲溶液的性质
缓冲溶液的缓冲能力是有限的,只有当c酸(碱)/c盐的比值在一定范围内,溶液的缓冲性能才比较显著。
缓冲能力:在保持缓冲溶液的pH值基本不变前提
下,缓冲溶液所能抵抗外加酸碱的量,
又叫缓冲容量。
决定缓冲能力大小的因素:
★ 酸(碱)和盐的总浓度越大,缓冲溶液的缓冲能力
越大。
★ 酸(碱)和盐的总浓度为定值且c酸(碱)/c盐=1 时,缓
冲能力为最大。
★ 缓冲溶液的缓冲能力是有限的,当缓冲溶液中的
抗酸(或抗碱)成分消耗完时,则失去缓冲作用。
缓冲范围
pKa-1 < pH <pKa+1的变化范围称为缓冲范围。
6. 缓冲溶液的选择和配制
a.选择适当的缓冲对, 缓冲溶液的pH应该落在
pKa-1 < pH < pKa+1之间,并尽量接近弱酸pKa

b. 所选择的缓冲对不能与反应物或生成物发生作用,
药用缓冲溶液还必须考虑是否有毒性等。
c. 为了使缓冲溶液具有较大的缓冲容量,应尽量使
缓冲比接近于1。并计算出所需共轭酸、碱的量。
例:用1.0mol/L氨水和固体NH4Cl为原料,如何配制500mLpH=9.0,其中氨水浓度为0.20mol/L的缓冲溶液?已知(或查表),pKb=4.74,MNH4Cl=53.49g/mol。
解:Ka=Kw/Kb=10-14/10-4.74=10-9.26。

7.2 强电解质溶液
一、电解质和非电解质
电解质:在水溶液中或在熔融状态下能导电的化合物
根据电离程度大小,可将电解质分为:

电离平衡
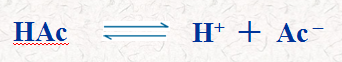
电离平衡:正、逆反应速率相等时,电解质分子和离子间达到的动态平衡

| 电解质 | 表观解离度 |
| HCl | 92% |
| HNO3 | 92% |
| NaOH | 84% |
| NaCl | 84% |
| KNO3 | 83% |

Ø 任何强电解质在水溶液中都是以离子形式存在,其理论解离度应为100%。Ø电导实验的测定结果似乎证明强电解质并不是完全解离。
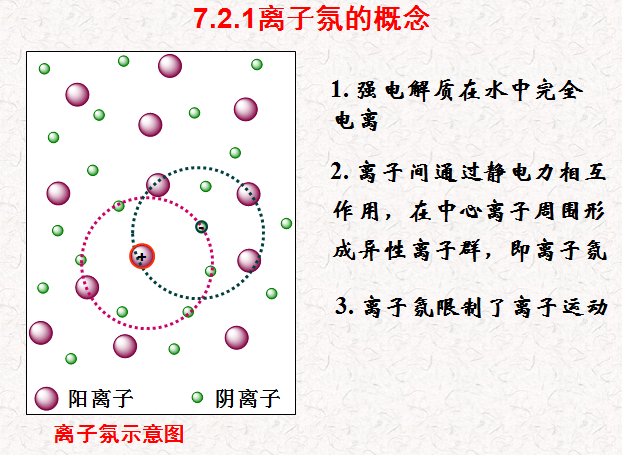
由于离子氛的影响,实验测得的强电解质的解离度并不是真正意义的解离度,因此这种解离度被称为“表观解离度”。
离子浓度越大,离子所带电荷越多,离子间的相互作用越强,表观电离度越小。
离子浓度越小,离子所带电荷越少,离子氛影响越小,表观解离度越大,越接近100%。
7.2.2活度和活度系数
活度:电解质溶液中,实际上可起作用的离子浓度
符号:a
活度与浓度的关系:
γi : 离子的活度系数,是溶液中离子间相互作用力大小的反映,通常小于1。
讨论:Ø 溶液越浓,离子电荷越高,离子间相互作用越大,γi越小,活度和浓度差距越大
Ø稀溶液,离子间相互作用越弱,γi→ 1,一般情况下,稀溶液中,离子间的作用较小,可以忽略,r=1,a=c


