6.4 有限实验数据的统计处理
第6章 定量分析化学概述6.4.ppt(下载附件 1.31 MB)
6.4.1 平均值的置信区间
1、 置信区间与置信度
目的:在无真实值的情况下,如何评价测定结果的可靠性?
需要在测量值附近估计出真实值可能存在的范围以及这一范围估计正确与否的概率,由此引出置(可)信区间与置信度(概率)的问题。
置信区间 :在一定置信度下,以测定结果为中心的、包括总体平均值μ在内的可靠性范围。
置信度P:测定值在置信区间内出现的概率(也称置信概率、置信水平、可信度)。
![]() 一般分析化学选95%。
一般分析化学选95%。
2. 平均值的置信区间
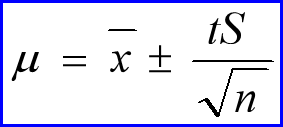
式中:s为标准偏差,n为测定次数,t为在选定的某一置信度下的概率系数,可根据测定次数n(或自由度f)和置信度由表6.1(P123)查得。
总结:
(1)置信区间越小, 和μ越接近,平均值的可靠性就越大。
(2)测定次数越多、精密度越高、S越小,置信区间越小。
(3) t越小,置信区间越小。
6.4.2 可疑数据的取舍
在一组平行测定的数据中,有时会有个别数据偏离其他数据较远,这些偏离较远的数据称为可疑值(或异常值、离群值)。
Q 检验法(适于测定次数3~10次)
步骤:(1) 将测定值由小到大排列:![]()
(2) 求极差R:![]()
(3) 求可疑数据与相邻数据之差:![]()
(4) 计算Q计:![]()
(5) 根据测定次数和要求的置信度P,查表123页6.2得Q表
(6)将Q计与Q表 相比,若Q计> Q表,则舍弃可疑值;若Q计< Q表 , 保留该数据。
6.4.3 显著性检验
(1)已知标准值的t检验
a. 计算t值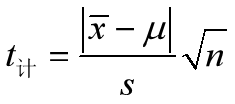
b. 由要求的置信度和测定次数,查表,得: t表(123页表6.1)
c. 比较
t计> t表,
表示有显著性差异,存在系统误差,被检验方法需要改进。
t计< t表,
表示无显著性差异,被检验方法可以采用。
例,一种新方法用来测定试样含铜量,用含铜量为11.7mg/kg的标准试样,进行五次测定,所得数据为:10.9, 11.8, 10.9, 10.3, 10.0,判断该方法是否可行?(是否存在系统误差)

(2).两组数据的平均值比较(同一试样,不同方法)
F检验法(方差检验法)
F 检验法是在判断比较两组数据是否有显著性差异时,首先考察它们的精密度是否有显著性差异,即数据的分散性。
对于两组数据之间是否存在系统误差,则在先进行F 检验并确定它们的精密度没有显著性差以后,再进行t 检验才是合理的。如果精密度有显著性差,就没有必要再进行t 检验。


6.4.4 分析结果的数据处理和报告
数据处理步骤:
(1) 对偏差较大的可疑数据进行Q检验,决定其取舍;
(2) 根据保留值,计算平均值、平均偏差、标准偏差等;
(3) 按要求的置信度求出平均值的置信区间。


例3,选择题:(只有一个选项正确)
(1)、下面论述中正确的是:
A.精密度高,准确度一定高
B.准确度高,一定要求精密度高
C.精密度高,系统误差一定小
D.分析中,首先要求准确度,其次才是精密度
答案:B

(3)、在分析测定中,论述偶然误差正确的是
A.大小误差出现的几率相等
B.正误差出现的几率大于负误差
C.负误差出现的几率大于正误差
D.正负误差出现的几率相等
答案:D
例 4、试对以下七个数据进行Q检验,置信度90%: 5.12、6.82、6.12、6.32、6.22、6.32、6.02
解:1. 5.12,6.02,6.12,6.22,6.32,6.32,6.82
2. xn - x1 = 6.82 - 5.12 = 1.70
3. x2 – x1 = 6.02 – 5.12 = 0.90
4. Q = (x2 – x1 )/(xn - x1 )= 0.90/1.70 = 0.53
5. 查表Q0.90,n=7=0.51
6. 0.53 > Q0.90,n=7,舍弃5.12
再检验6.82
Q =( 6.82 – 6.32)/(6.82 - 6.02)= 0.625
0.625 > Q0.90,n=6(0.56),舍弃6.82

例6、填空:(1)、一同学测得某溶液的pH = 6.24,则该数据的有效数字为 2 位。
(2)、某同学测得某式样中含铁量为0.923%,此数据的有效数字为 4 位。


