6.3 定量分析中的误差问题
第6章 定量分析化学概述6.3.ppt(下载附件 1.31 MB)
6.3.1 误差产生的原因
1. 系统误差(可定误差)
某些固定的原因造成的误差。
特点:a.对分析结果的影响比较恒定;单向性
b.同一条件下,重复测定,重复出现;重现性
c.大小正负可以测定; 可测性
d.用适当方法进行校正或加以消除。可减免
(1)方法误差——分析方法本身不够完善。(反应不完全、终点不一致)
例: 重量分析中沉淀的溶解损失;滴定分析中指示剂选择不当。
(2)仪器误差——仪器本身不准确或未经校准引起的误差。
例:天平两臂不等,砝码腐蚀;滴定管、容量瓶等量器刻度不准,未校正。
(3)试剂误差——所用试剂、蒸馏水纯度不够引起的误差。
例:试剂纯度不够(含待测组份或干扰离子) 蒸馏水不合格
(4)主观误差——操作人员主观因素造成(也称操作误差)。
例:对指示剂颜色辨别偏深或偏浅;滴定管读数习惯性偏高或偏低。
2、偶然误差(随机误差、不定误差)
由某些难以控制、无法避免的偶然因素引起而造成的误差。
例如:滴定体积最后一位读数的不确定性;实验室中温度、气压、湿度等的变化引起的微小误差。
由某些难以控制、无法避免的偶然因素引起而造成的误差。
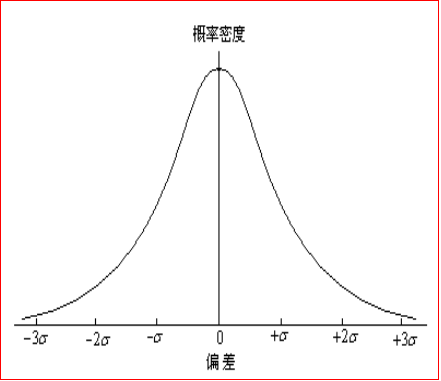
规律:偶然误差时刻都存在,大、小、正、负不可测、不固定,难以控制,难以避免,是消除不了的。 但在消除了系统误差之后,在同一条件下多次重复测定,发现随机误差符合高斯正态分布
多次测定时随机误差规律性:
①对称性——大小相近的正负误差出现的概率相等。
②单峰性——小误差出现的频率较高,而大误差出现的频率较低,很大误差出现的概率近于零。
③抵偿性——无限多次测定结果误差的算术平均值趋于零,测定次数大于10次时,减小不明显,一般测定3-5次至多10次即可。
3. 过失误差
除了系统误差和随机误差外,还有一种由工作人员粗心大意,违反操作规程造成的错误,称 “过失误差”。
例如:容器不洁净、加错试剂、丢损试液、读错数据、记录错误、计算错误等。
要求:
这类差错是可以避免的。
对已发现因过失而产生的结果应舍弃。
6.3.2 误差与准确度
准确度─表示测定结果(X)与真实值(Xt)的接近程度, 准确度的高低用误差E 的大小来衡量;
误差——测定结果 X与真实值 Xt之间的差值。一般用绝对误差(E)和相对误差(Er)表示。
绝对误差 E =X–Xt
误差越小,分析结果越接近真实值,准确度也越高。
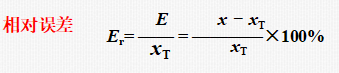
例6.3 用分析天平称得A、B两物质的质量分别为1.7765g、0.1776g; 两物体的真实值分别为:1.7766g、0.1777g, 哪种称量准确度高?

6.3.3 精密度与偏差
精密度——指在相同条件下,多次平行测定同一样品所得的测定结果之间的相互接近程度。
精密度高低用偏差来衡量。
(1)偏差 :绝对偏差、相对偏差、平均偏差及相对平均偏差。

(2) 标准偏差 S:总体标准偏差σ、标准偏差S、相对标准偏差CV
标准偏差也称均方根偏差,它和相对标准偏差都是用统计方法处理分析数据的结果,二者均可反映一组平行测定数据的精密度。标准偏差越小,精密度越高。
总体标准偏差σ: 测定次数趋于无限大时的标准偏差。
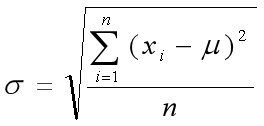
式中μ 为无限多次测定的平均值(总体平均值,真实值)
n 通常指大于30次的测定 。
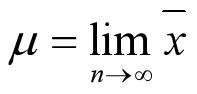
标准偏差S :对有限测定次数(n<20)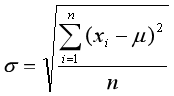
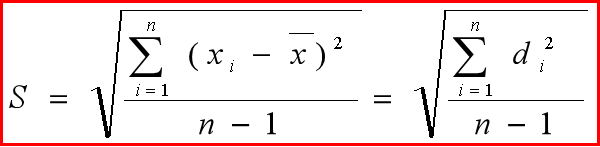
式中n-1称为自由度 f ,表示独立变化的偏差数目。
相对标准偏差CV(又称变异系数):![]()

6.3.4 误差、准确度和精密度的关系
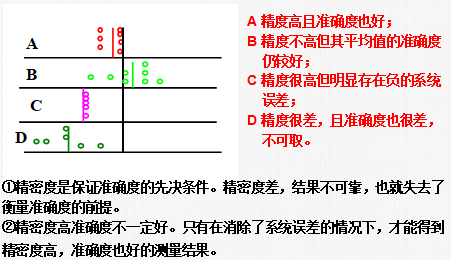
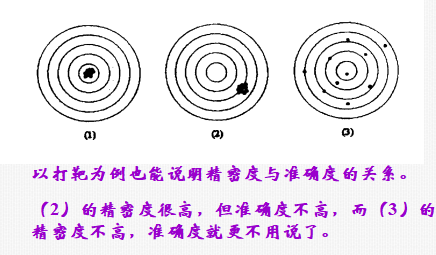
6.3.5 提高分析结果准确度的方法
1. 选择合适的分析方法——根据具体要求选择。
化学分析法
(重量法和滴定分析法)测定的准确度高(千分之几),但灵敏度低,适用于常量(>1%)组分的分析。
仪器分析法
测定的灵敏度高,但准确度较低,适用于微量(0.01%~1%)或痕量(<0.01%)组分的分析。
2. 减少测量的相对误差
选择合适的测量值的范围可减小测量的相对误差,如称量的质量,滴定剂的体积,吸光度的范围等。
3. 检查和消除系统误差
(1) 对照试验——用标准试样、标准方法。
(2)回收试验——在测定试样某组分含量x1的基础上,加入已知量的该组分xs,再次测定该组分含量x2。
![]()
(3) 空白试验——不加试样测定、扣空白。用于检验并消除由试剂、蒸馏水及容器引入杂质造成的系统误差 。
(4) 方法校正——用标准方法对照试验,找出校正数据。
(5) 仪器校正——校正测量仪器,如砝码、滴定管、移液管、容量瓶等。
4. 减少偶然误差
适当增加测定次数,一般测定次数3~5次。
5. 避免过失误差


