6.2 有效数字及其运算规则
第6章 定量分析化学概述6.2.ppt(下载附件 1.31 MB)
6.2.1有效数字的概念
6.2.2有效数字修约规则
6.2.3有效数字运算规则
6.2.1 有效数字的概念
1.两类数字
(1)非测量数字:如测定次数;倍数;系数;分数
(2)测量数字:有效数字。(最后一位为可疑数字)记录的数字不仅表示数量的大小,而且要正确地反映测量的精确程度。
结果 绝对误差 相对误差
0.51800 ±0.00001 ±0.002%
0.5180 ±0.0001 ±0.02%
0.518 ±0.001 ±0.2%
2、有效数字位数的确定:
1.0008, 43.181 5位
0.1000, 10.98% 4位
0.0382, 1.98×10-10 3位
54, 0.0040 2位
0.05, 2×10-5 1位
3600, 100 不确定
3.数据中零的作用
数字零在数据中具有双重作用:
(1)作普通数字用,如 0.5180
4位有效数字 5.18010-1
(2)作定位用:如 0.0518
3位有效数字 5.1810-2
4.注意:
(1)容量器皿:滴定管;移液管;容量瓶 保留至小数点后2位
(2)分析天平(万分之一)保留至小数点后4位
(3)标准溶液的浓度,用4位有效数字表示: 0.1000 mol/L
(4)对pH, pM, lgc, lgK等对数值,有效数字为小数部分 pH 4.34 2位有效数字
(5)位数不定的,可视情况科学计数例如:3600,可写为3.6×103,3.60×103,3.600×103,有效数字分别为2,3,4位
(6)分析化学中遇到的分数、倍数可视为无限多位
(7)8以上的数可多算一位,如9.00,9.83,可当作4位有效数字
(8)分析结果的有效数字保留高含量组分ω>10%,分析结果保留四位有效数字。
例如铁矿石含铁56.18%。
中含量组分1%<ω<10%,分析结果保留三位有效数字。
例如,水中钙、镁总含量5.18%。
微量组分ω< 1%,分析结果保留两位有效数字。
例如,食盐中碘含量0.0050%
6.2.2、 有效数字的修约规则
① “四舍六入五留双”; 将下列数字修约为两位
3.249 3.2 “四舍”
8.361 8.4 “六入”
6.550 6.6 “五留双”
6.250 6.2 “五留双”
6.2501 6.3 “五后有数需进位”
②只可保留最后一位欠准确数字;一次修约。
如:将5.5491修约为2位有效数字?
一次修约为5.5 √
多次修约为5.549~5.55~5.6 ×
“四舍六入五留双”
例 7 将下列数字修约为4位有效数字。
3.1124 3.1126 3.1115 3.1125 3.11251
3.112 3.113 3.112 3.112 3.113
6.2.3、 有效数字的运算规则
(1)加减法
原则:结果的有效数字的位数以小数点后位数最少(即绝对误差最大)为标准。
如:3.72+10.6355=?
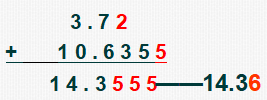
(2)乘除法
原则:结果的有效数字的位数以各数中相对误差最大为标准。
例:(0.0325 x 5.103 x 60.06)/ 139.8 = 0.071179184
0.0325 ±0.0001/0.0325x 100%=±0.3%
5.103 ±0.001 /5.103x 100%=±0.02%
60.06 ± 0.01 /60.06x 100%=±0.02%
139.8 ±0.1 /139.8x 100% =±0.07%
例 8 计算(混合运算)
0.0121+25.64+1.05782 +2×(3.261×10-5×1.78)=?
解: 0.0121+25.64+1.05782 +2×5.80×10-5
= 0.0121+25.64+1.05782 +11.60 ×10-5
= (26.7099316)
= 26.71


