4.2 配位化合物的化学键理论
4.2.1 价键理论
第4章 配位键和配位化合物4.2 4.2.ppt(下载附件 8.15 MB)
4.2.1 价键理论
4 . 2 . 1.1 配合物价键理论的要点
(1)中心离子M(或原子):价电子层有空轨道,是电子对接受体;
配体(L):提供孤对电子,是电子对给予体;二者形成配位键ML。
(2)中心离子(或原子)价层上的空轨道首先杂化,杂化类型决定于中心离子的价层电子构型和配体的数目 及配位能力的强弱。
(3)中心离子(或原子)的杂化轨道与配位原子中的孤对电子的原子轨道重叠成键,形成配合物。
(4)配合物的空间构型取决于中心离子(或原子)的杂化轨道类型。
4.2.1.2 中心离子的杂化轨道
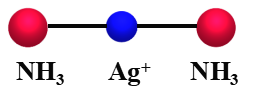
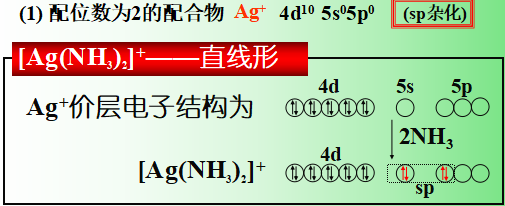
(1) 配位数为2的配合物
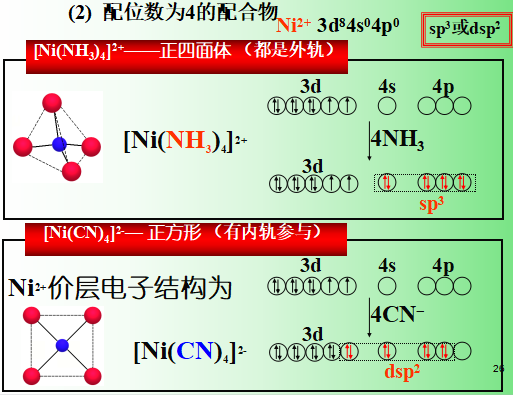
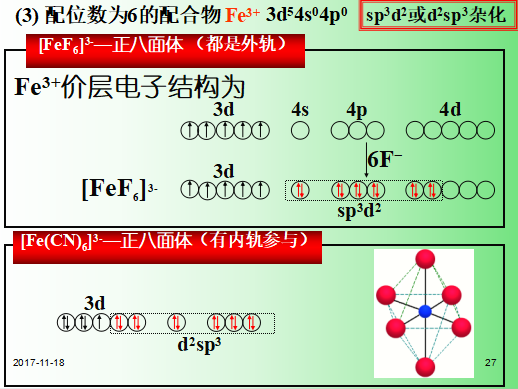
3. 内、外轨型配合物
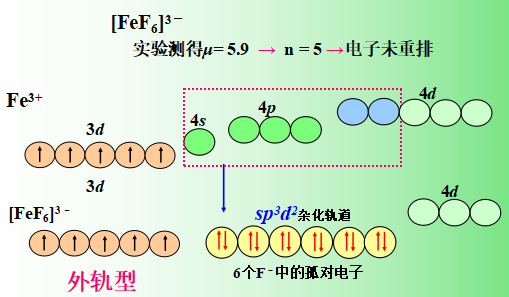
①外轨型配合物:中心离子以最外层的ns、np、nd 轨道杂化,配位原子的孤对电子投入中心离子的外层轨道上,这样形成的配合物叫外轨型配合物, 由于没有电子重排,单电子数较多,磁矩较大。
如:sp、sp3、sp3d2 杂化形成的配合物。
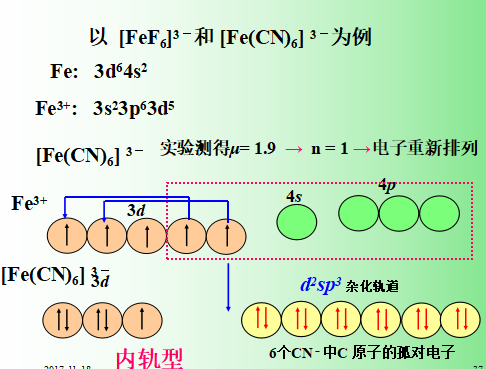
②内轨型配合物:受配位原子影响,中心离子内层的d轨道重排,以(n-1)d 、ns 、np 轨道杂化,配位原子的孤对电子插入中心离子的内层轨道上,所形成的配合物叫内轨型配合物,其稳定性较强(内层轨道上电子能量低);由于电子重排配对,单电子数减少,磁矩减小,甚至变为反磁性物质。
如: dsp2、d2sp3杂化形成的配合物。
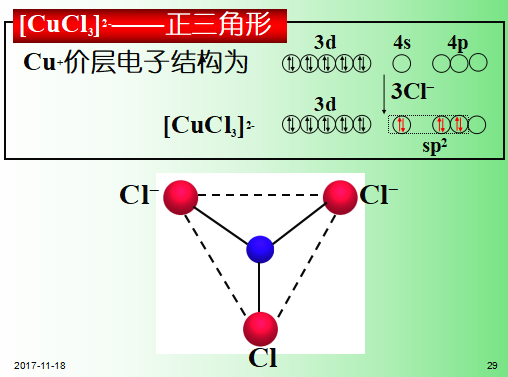
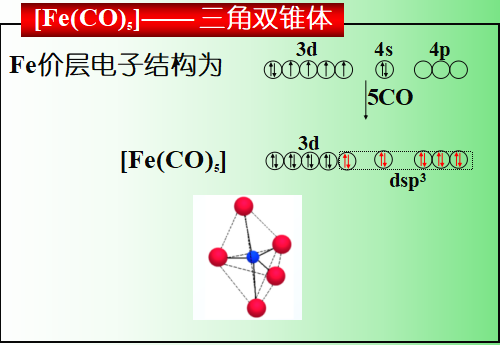
4.2.1.3价键理论的应用
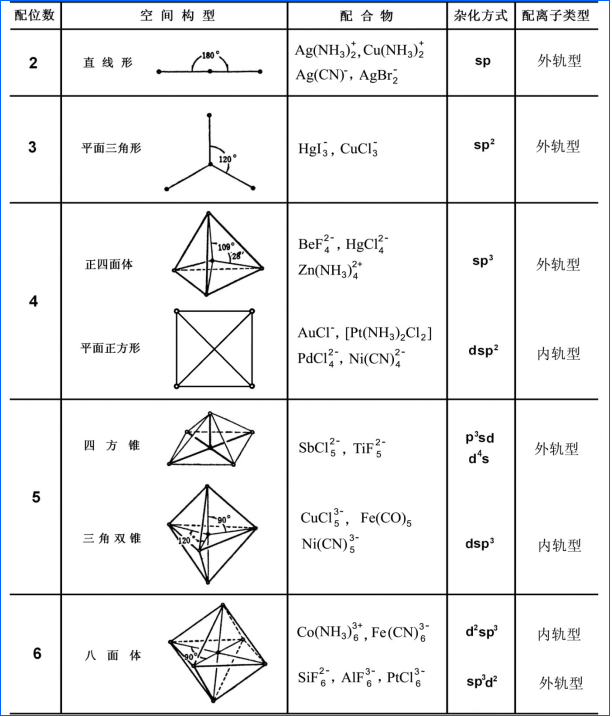
⑴判断配合物的空间构型
判断中心离子杂化类型及配合物空间构型的方法
(1)根据配位数=杂化轨道数,初步判断中心离子杂化类型;
(2)写出中心离子电子排布;
(3)根据中心离子价电子和配位原子电负性,进一步判断中心离子杂化类型及配合物空间构型。
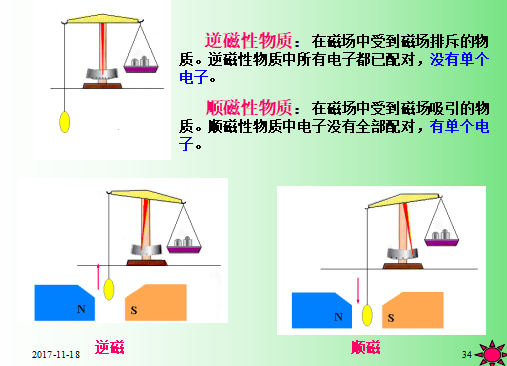
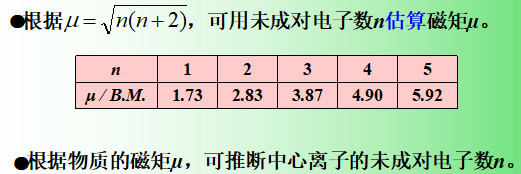
⑵判断配合物的磁性
磁 性:物质在磁场中表现出来的性质
顺磁性:被磁场吸引 n > 0 , µ > 0 O2
反磁性:被磁场排斥 n =0 , µ = 0 N2
铁磁性:被磁场强烈吸引 Fe、Co、Ni


4.1]实验测得的磁矩μ=5.88,试根据此数据推测配离子:①空间构型;②未成对电子数;③中心离子杂化轨道类型;④属于内轨型还是外轨型配合物?
解: ①配位数=6,所以配离子为正八面体结构。 ②根据得,n≈ 5(未成对电子数)。 ③ 根据未成对电子数为5,Fe3+: 3s23p63d5知,中心离子采取sp3d2空轨道杂化,形成6个杂化空轨道来接受6个配体H2O中O原子提供的孤电子对。 ④中心离子采取sp3d2空轨道杂化,所以是外轨型配合物。


