第4章 配位键和配位化合物
第4章 配位键和配位化合物4.1.ppt(下载附件 8.15 MB)
4.1 配位化合物的基本概念
4.2 配位化合物的化学键理论
4.3 配位化合物的应用
4.1 配位化合物的基本概念
4.1.1 配位化合物的定义
4.1.2 配位化合物的组成
4.1.3 配位化合物的命名
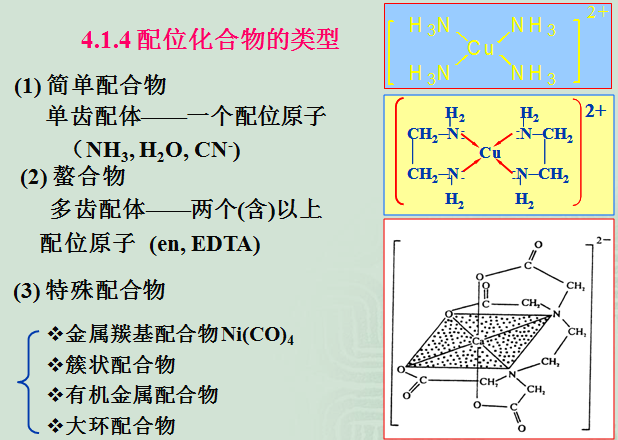
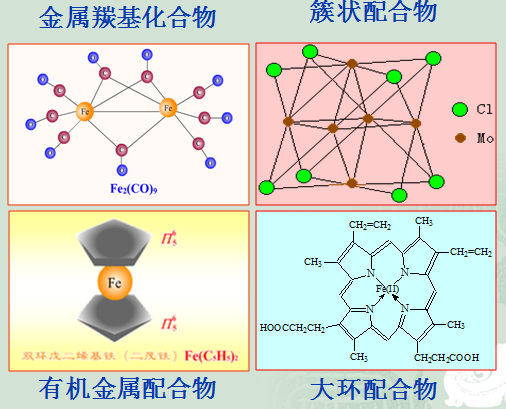
4.1.4 配位化合物的类型


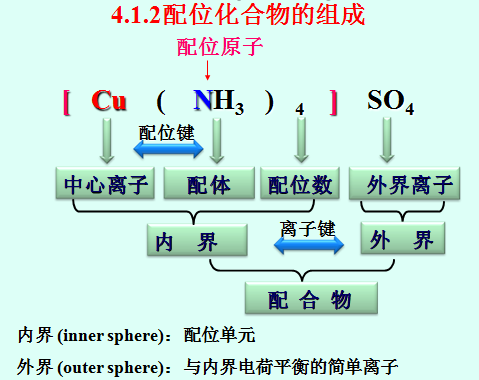
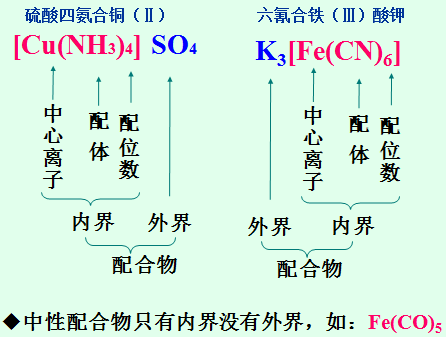
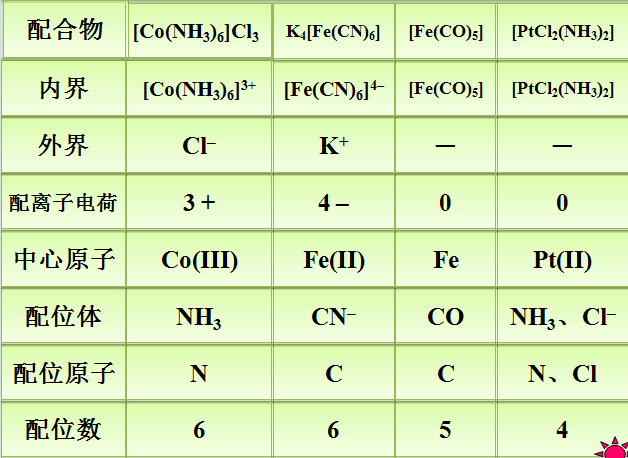
内界
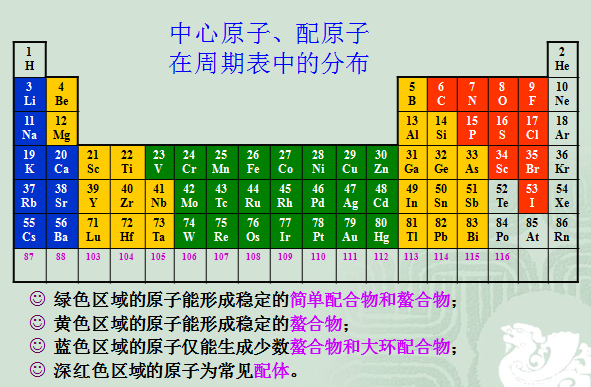
(1)、中心离子(或原子)
v 一般为带正电的过渡金属离子
[Co(NH3)6]3+, [Fe(CN)6]4-, [HgI4]2-
v电中性原子:Ni(CO)4 , Fe(CO)5 , Cr(CO)6v 非金属元素原子:SiF62- , PF6-
(2)、配位体和配位原子

配位原子:配体中直接与中心离子相连的原子。
F, Cl,Br,I,C,N,O,S,P,H,As,Sb,Se,Te

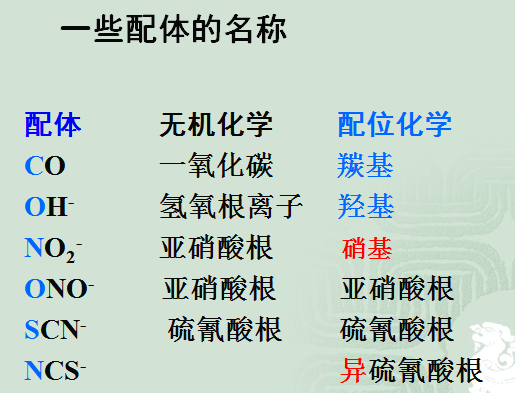
表4.1常见的单齿配体及名称
| 中性分子配位体及其名称 | 阴离子配位体及其名称 | ||||
| H2O | 水 | F- | 氟 | NH2- | 胺基 |
| NH3 | 氨 | Cl- | 氯 | NO2- | 硝基 |
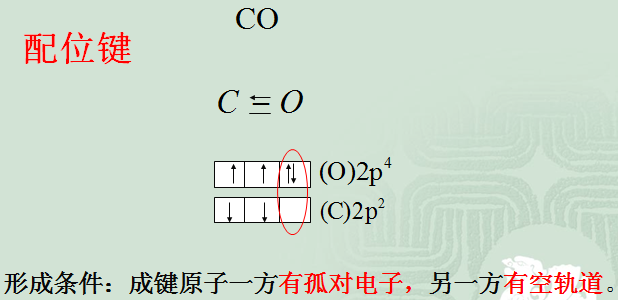
| CO | 羰基 | Br- | 溴 | ONO- | 亚硝酸根 |
| NO | 亚硝酰基 | I- | 碘 | SCN- | 硫氰酸根 |
| CH3NH2 | 甲胺 | OH- | 羟基 | NCS- | 异硫氰酸根 |
| C5H5N | 吡啶(Py) | CN- | 氰 | S2O32- | 硫代硫酸根 |
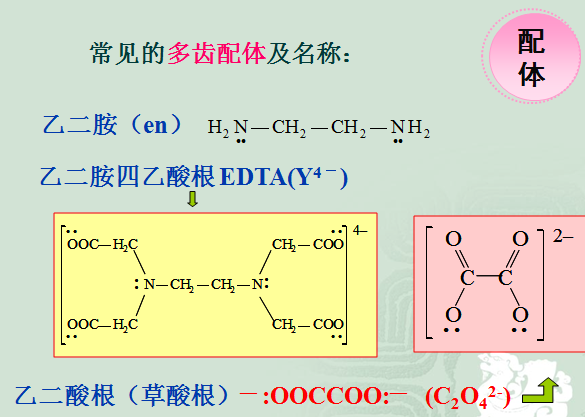
两可配体:
配体虽然具有两种或多种配位原子,但在一定条件下,
仅有一种配位原子与中心离子配位。
SCN-
| 配合物实例 | [Ag(SCN)2]- | [Fe(NCS)6]3- |
| 配位原子 | *SCN- | * NCS- |
| 配体名称 | 硫氰酸根 | 异硫氰酸根 |
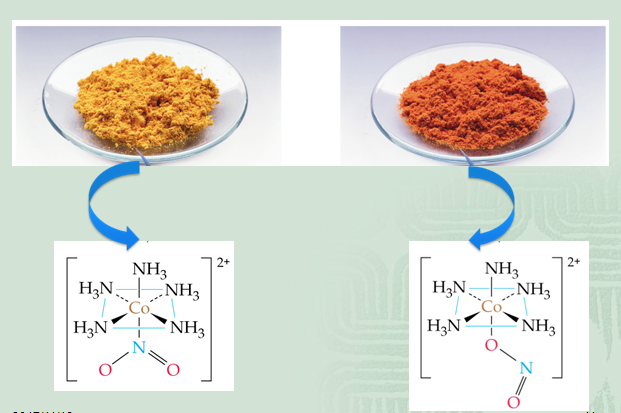
NO2-
| 配合物实例 | [Co(NH3)5(NO2)]2+ | [Co(NH3)5(ONO)]2+ |
| 配位原子 | *NO2- | ONO*- |
| 配体名称 | 硝基 | 亚硝酸根 |
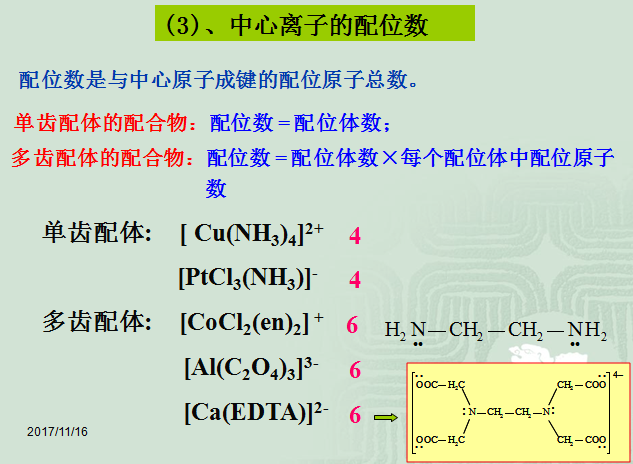
影影响配位数的因素:
v中心离子的氧化数越高,配位数往往越大。
如:Ag+、Cu+、Au+等离子的特征配位数为2,
Cu2+、Zn2+、Hg2+、Co2+、Ni2+等离子的特征配位数为4,
Fe3+、Co3+、Al3+、Cr3+等离子的特征配位数为6。
v中心离子的半径越大,配位数往往越大。
如:[BF4]-中,中心离子的配位数是4,
[AlF6]3-中,中心离子的配位数是6。
v一般来说,配体的体积越大,中心离子的配位数越小。
如:[AlF6]3-中,中心离子的配位数是6,
[AlCl4]-中,中心离子的配位数是4。
v另外配位数还受到中心离子和配位体之间的相互作用以及配合物生成时的外界条件(温度、浓度等)的影响。
v总之,确定配位数要根据实验事实。
4、配离子的电荷
配离子电荷等于中心离子和配体两者电荷的代数和。

4.1.3 配位化合物的命名
1. 习惯命名法
K4[Fe(CN)6]: 黄血盐 Fe(C5H5)2: 二茂铁
K3[Fe(CN)6]: 红血盐 K[PtCl3(C2H4)]:蔡斯盐
2. 系统命名法
原则:服从一般无机化合物的命名原则。
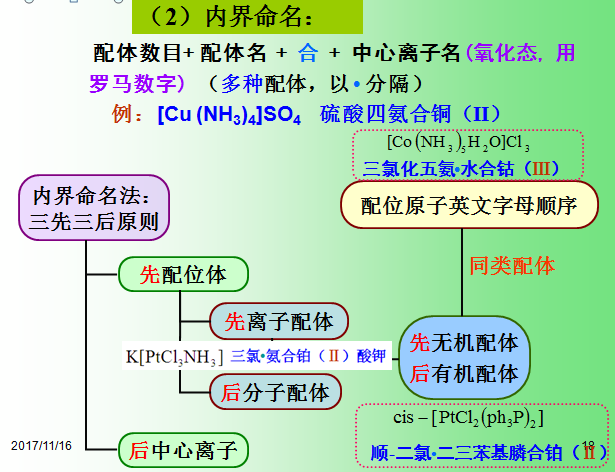
(1)外界命名:
外界是简单阴离子酸根,则称“某化某”。
[CoC12(NH3)4]Cl 一氯化二氯·四氨合钴(III)
外界是复杂阴离子酸根,则称“某酸某”。
[Cu(NH3)4]SO4 硫酸四氨合铜(II)
外界为氢离子,配阴离子后用酸字结尾,它的盐类似。
H[PtCl3(NH3)] 三氯·一氨合铂(II)酸
K [PtCl3(NH3)] 三氯·一氨合铂(II)酸钾