3.6 离子的极化
第3章 分子结构和晶体结构-2015.10.21 3.6.ppt(下载附件 9.6 MB)
3.6.1 离子极化
离子的极化:在阴、阳离子自身电场的作用下,使其周围带异号电荷的离子的电子云发生变形的现象。
离子的变形性:离子在电场作用下,电子云发生变形的难易程度。
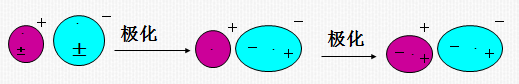
决定离子极化强弱因素:离子的极化力和离子的变形性
![]()
正离子半径小,变形能力弱,主要表现出极化力,即:使其它离子变形的能力。
•离子的电荷:电荷 ,极化力 (Al3+ >Na+)
•离子的半径:半径 ¯ ,极化力 (Na+ >K+)
•离子的电子构型:


![]()
负离子半径大,核外电子云较易发生变形,主要表现出变形性。
1.负离子的电荷越高,变形性越大。
2.负离子的半径越大,变形性越大。
3.最外层为18电子构型或最外层有d电子的正离子,
变形性也比较大。
18e , 18+2e型 > 9~17e型 > 8e 型>2e 型
正离子:电荷多,半径小,极化力大
2e , 18e , 18+2e型 > 9~17e型 > 8e 型
负离子:电荷多,半径大,变形性大
18e , 18+2e型 > 9~17e型 > 8e 型>2e 型
18e , 18+2e型 > 9~17e型:附加极化作用
d电子数越多,电子层数越多,附加极化作用越大
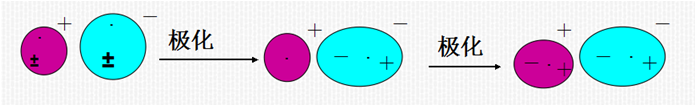
3.6.2 离子极化对物质结构和性质的影响
极化作用增强使化合物键型由离子键向共价键过渡
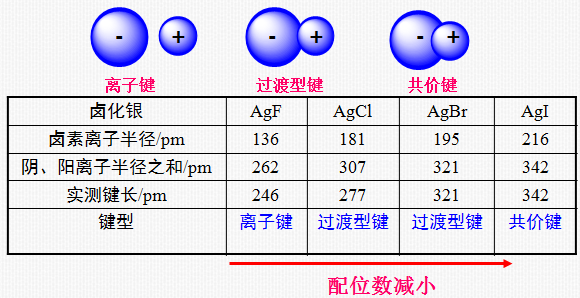
1. 极化作用增强使化合物的热稳定性降低
CuCl2 993℃分解
CuI2 常温易分解
2. 极化作用增强使化合物的熔沸点降低
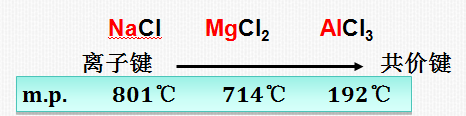
3. 极化作用增强使化合物溶解度减小

4. 极化作用增强使化合物颜色加深



