3.4 原子晶体和分子晶体
第3章 分子结构和晶体结构-2015.10.21 3.4.ppt(下载附件 9.6 MB)
3.4.1 分子晶体
分子晶体——靠分子间力或氢键结合而成的晶体。
特点:晶格上的质点——分子;
质点间作用力——分子间力或氢键; CO2的晶体结构
晶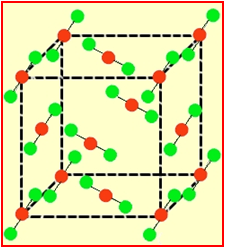 体中存在独立的简单
体中存在独立的简单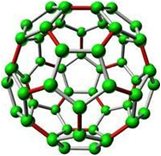 分子。
分子。
分子晶体的性质:
熔点低,硬度小,易挥发,(分子间力弱),
通常为电的不良导体,但一些强极性键的分子晶体(HCl),溶于水导电。
典型的分子晶体:
(1)所有非金属氢化物:H2O,H2S,NH3,CH4,HX
(2)部分非金属单质:X2,O2,H2,P4,C60
(3)部分非金属氧化物: CO2,SO2,NO2
(4)几乎所有的酸:HCl,H2SO4,HNO3,H3PO4
(5)绝大多数有机物的晶体:乙醇,冰醋酸,蔗糖
(6)稀有气体
v熔沸点高低规律
分子间作用力越强,熔沸点越高。
①组成和结构相似的分子晶体,一般相对分子质量越大,分子间作用力越强,熔沸点越高。例如:元素周期表中第ⅦA族的元素单质其熔沸点变化规律为:F2<Cl2<Br2<I2<At2 。
②若分子间有氢键,则分子间作用力比结构相似的同类晶体大,故熔沸点较高。例如:HF > HI > HBr > HCl;
H2O> H2Se> H2S
③组成和结构不相似的分子晶体,分子极性越大,其熔沸点越高,例如:CO>N2
3.4.2 原子晶体
原子晶体 —靠共价键结合的晶体。
通常情况下是由“无限”数目的原子所组成。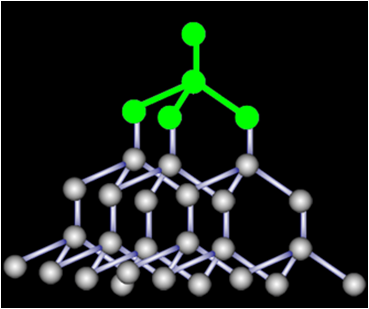
特点:晶格结点上的质点——原子;
质点间作用力——共价键;
原子晶体中不存在独立分子,是个巨型分子。
常见原子晶体:
(1)某些非金属单质:金刚石(C)、硅(Si)、锗(Ge)(2)某些非金属化合物:SiC、BN等
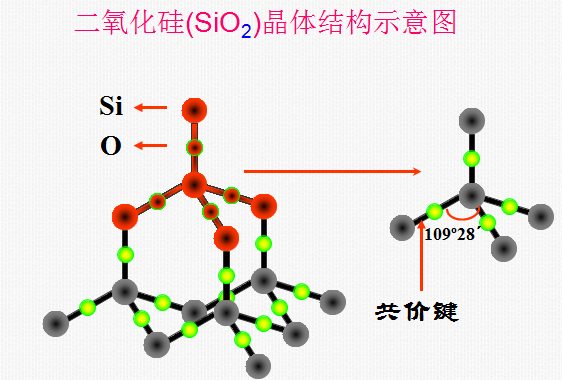
(3)某些氧化物:SiO2 等

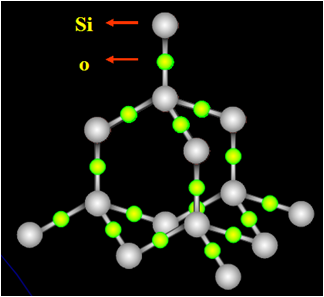
u熔沸点高低规律
(1)一般地,熔沸点:原子晶体>离子晶体>分子晶体
(2)对于结构相似的原子晶体,组成晶体的原子半径越小,共价键的键长越短,即共价键越牢固,晶体的熔、沸点越高,
熔沸点: 金刚石 > 碳化硅 > 硅晶体


