3.3 分子间力与氢键
第3章 分子结构和晶体结构-2015.10.212.ppt(下载附件 9.6 MB)、
3.3.1 分子的极性和变形性
3.3.2 分子间作用力的种类
3.3.3 分子间作用力与物质性质的关系
3.3.4 氢键
3.3.1 分子的极性和变形性
1、非极性分子和极性分子
(1) 非极性分子:整个分子的电荷分布均匀的、正负电荷重心重合的分子是非极性分子。如: H2、Cl2、N2、O2等。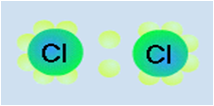
(2) 极性分子:整个分子中电荷分布不均匀、正负电荷重心不重合的分子叫做极性分子。
如:HCl、H2O、NH3等。
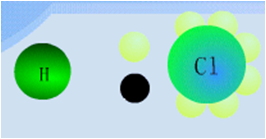
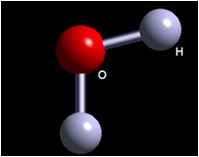
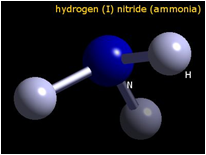
2、化学键的极性与分子极性的关系
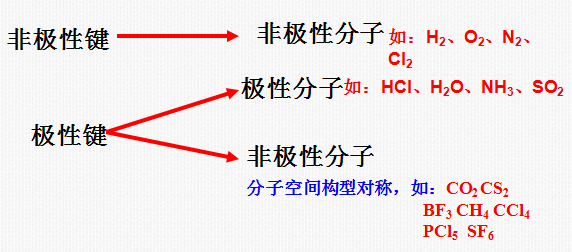
判判断下列分子的极性、杂化轨道类型和分子空间构型

3.偶极矩μ
偶极长(极性分子正负电荷中心间的距离)d与偶极电荷(极性分子正负电荷中心所带电荷)q的乘积。
μ=q·d,方向: +→- 单位:德拜D
μ= 0,为非极性分子;
μ≠0,为极性分子。 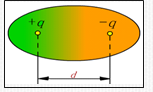
偶极矩越大,分子极性越强。
HF HCl HBr HI
μ/D 1.92 1.03 0.79 0.38
三种常见的偶极
⑴ 永久偶极:极性分子的正、负电荷中心不重合,分子中始终存在正极端和负极端。
⑵ 诱导偶极:分子在外电场影响下,正、负电荷重心发生相对位移,使分子发生变形,产生的这种偶极叫诱导偶极。![]()
![]()
外加电场使分子变形的作用称为极化作用。
分子在外加电场下发生变形的能力称为分子的变形性。一般分子的体积越大,变形性越大。
![]()
⑶ 瞬间偶极:非极性分子即使没有外电场作用,正负电荷重心可能发生变化,某一瞬间,分子的正、负电荷重心发生不重合现象时所产生的偶极。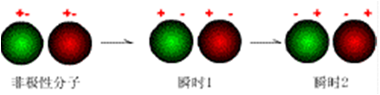
3.3.2 分子间作用力的种类
⑴ 取向力
⑵ 诱导力
(3) 色散力
1、取向力
由于极性分子的取向而产生的分子间作用力,叫取向力
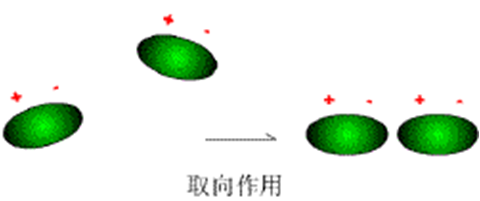

取向力发生在极性分子和极性分子之间。
2、诱导力
一个分子的永久偶极与另一个分子的诱导偶极之间的相互作用力称为诱导力。
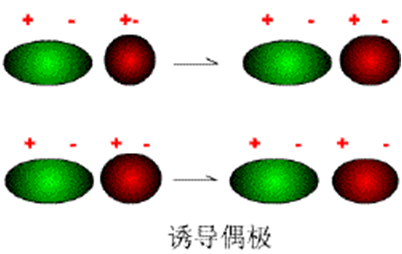
诱导力发生在极性分子和非极性分子、极性分子和极性分子之间。
3、色散力
一个分子的瞬间偶极与另一个分子的瞬间偶极之间的相互作用力称为色散力。
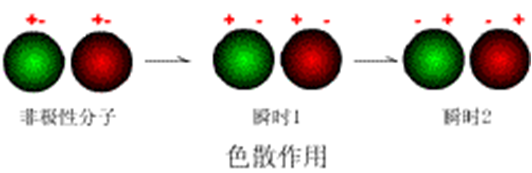
色散力发生在各种分子之间,并且是范德华力的主要形式。
•分子间力与分子极性
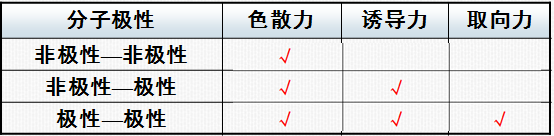
•分子间力的特点:
a ) 本质是静电作用;
b ) 力的作用很小(一般为0.1~50 kJ•mol-1 );
c ) 无方向性和饱和性;
d ) 作用范围有限,是近程力,F ∝ 1 / r7;
e ) 经常是以色散力为主,极性很大的分子以取向力为主
3.3.3 分子间作用力与物质性质的关系
1. 分子间作用力与物质熔沸点的关系
结构相似的同系列物质(如:卤素、稀有气体等),分子量越大,分子间作用力越强,物质的熔沸点越高。
F2 CI2 Br2 I2
聚集态 气 气 液 固
熔点/K 53.38 172.02 265.92 386.5
沸点/K 84.86 238.95 331.76 457.35
2. 分子间作用力与物质溶解度的关系
“相似相溶”经验规律:
极性相似者分子间作用力较大,其溶解度也大,反之亦然。
如:CCl4与H2O之间互溶性差;
NH3和H2O 之间可以互溶。
3.3.4 氢键
H2O、HF、NH3等物质的熔沸点反常现象:
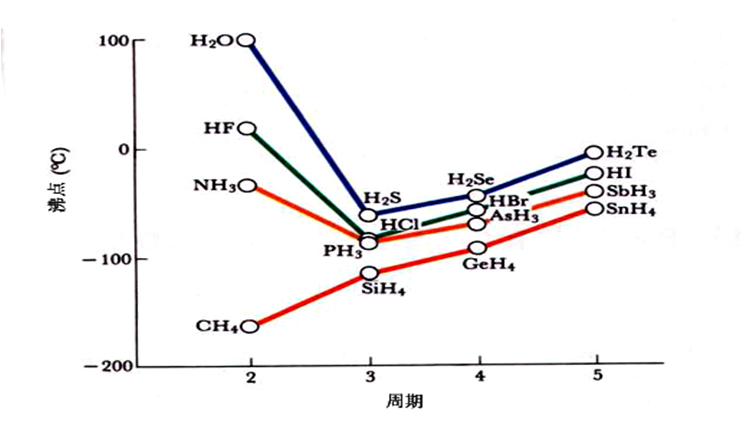
1. 氢键
n氢原子与电负性大的X原子以共价键结合以后,它还可以和另一个电负性大的Y原子产生吸引力,这种吸引力叫做氢键。![]()
n X、Y-代表 N、F、O等电负性大而且原子半径较小的原子,可相同,也可不同。n 形成条件:X、Y电负性大,半径小
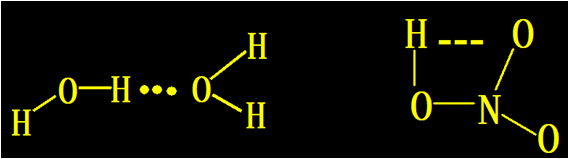
2 氢键的特点:
(1)方向性:X—H与Y尽可能在同一直线上
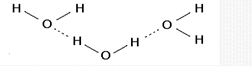
2)饱和性:每一个X—H只能与一个Y原子形成氢键
3)氢键的强弱与X和Y的电负性和原子半径有关:
电负性越大,则氢键越强;半径越小,形成的氢键越强.
F—H······F > O—H······O > N—H······N
4)氢键的强度介于化学键和分子间作用力之间
分子间作用力 < 氢键 << 化学键
3 氢键对物质性质的影响
(1) 氢键的形成对物质溶沸点的影响:
分子间氢键的形成可使物质的熔点和沸点显著升高。
H2O、HF、NH3等物质的熔沸点很高。
分子内氢键的形成可使物质的熔点和沸点降低。
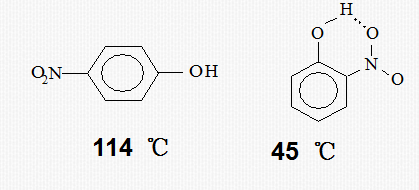
(2) 氢键的形成对物质的溶解度的影响:
Ø在极性溶剂中,如果溶质分子和溶剂分子之间可以形成分子间氢键,则溶质的溶解度增大。n例如,氨和水、乙醇和水n如果溶质分子能够形成分子内氢键,则在极性溶剂中的溶解度减小,而在非极性溶剂中的溶解度增大。


