3.2 共价键理论
3.2.1 经典共价键理论
3.2.2 现代共价键理论(VB)
3.2.3 杂化轨道理论(HOT)
3.2.4 价层电子对互斥理论(VSEPR)
3.2.5 分子轨道理论(MO)
3.2.6 键参数
3.2.1 经典共价键理论
第3章 分子结构和晶体结构-2015.10.211.ppt(下载附件 9.6 MB)
1916年,美国化学家路易斯(G.N.Lewis)提出了共价键的概念。
分子中原子间通过共用电子对而结合成的化学键称为共价键。
原子间共用电子对而形成稀有气体原子的稳定电子层结构,这样就服从了“八隅规则”。
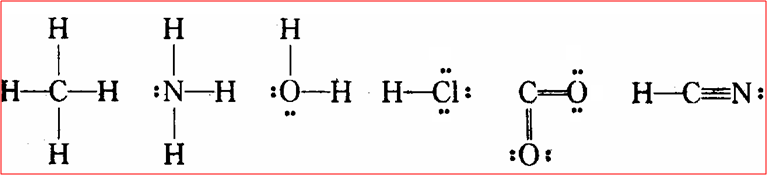
路易斯理论有局限性:
① 许多不遵循八隅规则的分子存在。如
BF3 PCl5 SF6
B2s22p1 P3s23p3 S3s23p4
② 不能说明共用电子对形成稳定分子的本质原因。
③ 不能解释分子空间的几何形状。
④ 不能说明电子对与原子轨道之间的关系。
![]()
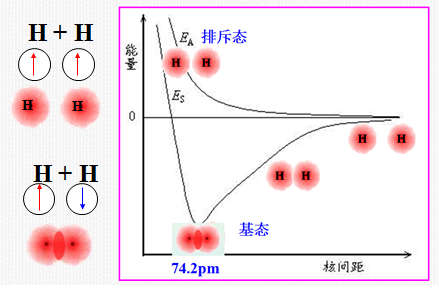
自旋平行的氢原子相互靠近:两核间电子云密度稀疏,体系能量升高,不发生原子轨道重叠,无法成键(排斥态)
自旋相反的氢原子相互靠近:原子轨道重叠,两核间电子云密度增大,体系能量降低,形成稳定的化学键(基态)
1. 共价键的特征
1 共价键结合力的本质是电性的。
共价键是共用电子对形成的负电区域对两个原子核的吸引力, 而不是正负离子之间的静电作用。
共用电子对的数目越多,核间电子云密度越大,结合力越强。
2饱和性![]()
共价键形成的条件是必须有成单的价电子,已经成对的电子不再和别的电子配对。![]()
一个原子有几个未成对的电子,就最多只可与几个自旋相反的单电子配对成键,所以共价键有饱和性。
3方向性
形成共价键时,根据最大重叠原理,两个原子成键时只有沿着轨道伸展的方向进行重叠,才能实现最大限度的重叠,这就决定了共价键的方向性。
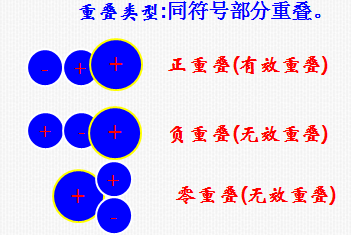
不能2. 共价键的类型
根据原子轨道重叠部分的对称性,共价键可分
为三类:
σ 键
π 键
配位键
1)σ 键
若两个原子轨道沿键轴(二原子核之间的连线)方向,以“头碰头”的方式发生最大重叠所形成的键称为σ键。
说明共用
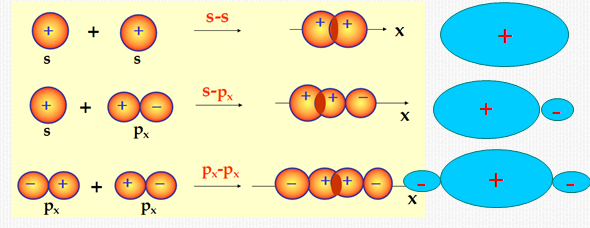
重叠程度大,牢固,可单独存在。
2) π 键
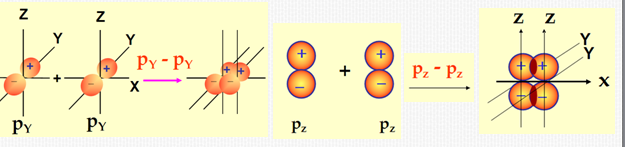
π键轨道重叠程度小于σ键,能量比较高,易断开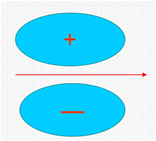
例:N2分子形成示意图
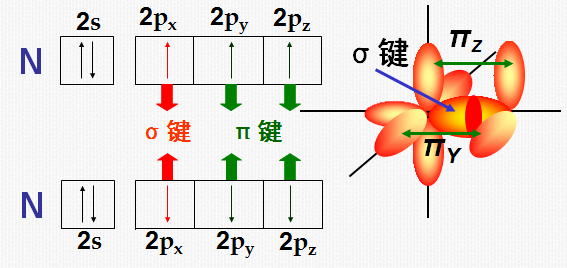
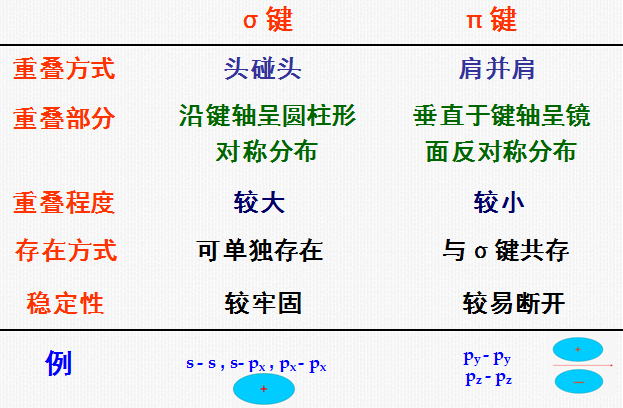
注:在价键理论中:

(3) 配位键
形成条件:成键原子一方有孤对电子,另一方有空轨道。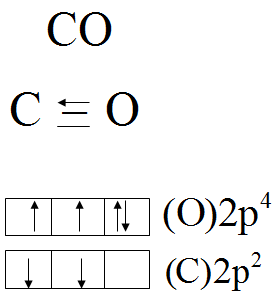
[Cu(NH3)4]2+、[Ag(NH3)2]+、Fe(CO)5
![]()
共价键理论局限性
例如:由于C 的电子排布式为:1s22s22px12py1,在C与 H 形成的化合物 CH4 中,分子呈正四面体结构,四个键角相等,都为 109o28′。
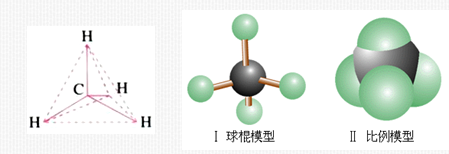

1931年,鲍林在价键理论的基础上,提出杂化轨道理论——可解释空间构型等。
原杂化轨道理论基本要点:
1)在形成分子过程时,由于原子的相互影响,同一原子中若干不同类型的、能量相近的原子轨道混合起来,重新分配能量和调整空间方向而组成一组新的轨道,这种重新组合的过程叫杂化,所形成的新轨道叫杂化轨道。
2)形成的杂化轨道数目等于参加杂化的原子轨道总数。杂化轨道相互排斥,在空间取得最大键角,杂化轨道的空间伸展方向决定了分子的空间构型。
3)杂化轨道的电子云分布集中,成键时轨道重叠程度大,故杂化轨道的成键能力比杂化前的成键能力强,因此形成的分子更稳定。
杂化轨道的类型: sp、sp2和sp3
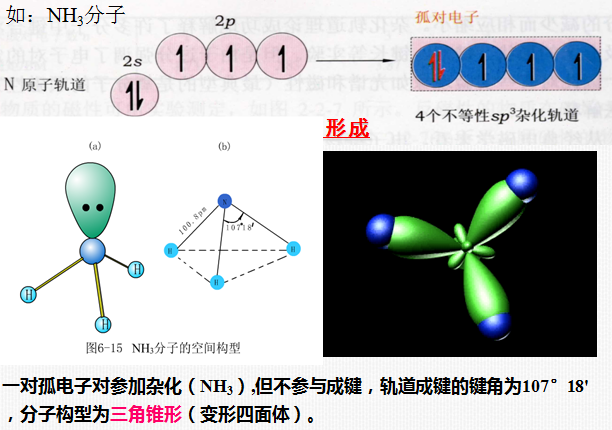
1)sp3 杂化
同一原子内由一个s轨道和三个p轨道发生的杂化。
sp3杂化后得到4个sp3杂化轨道。
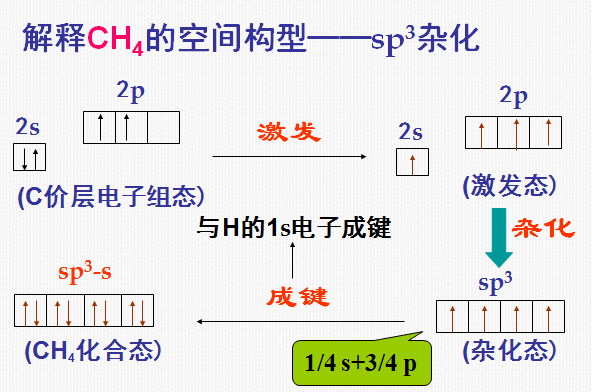
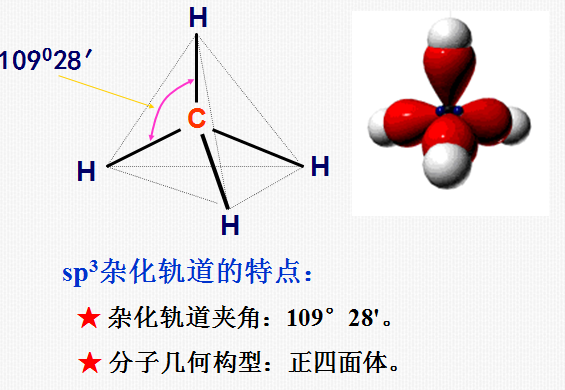
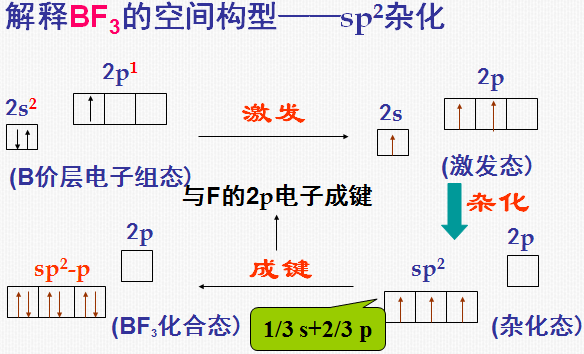
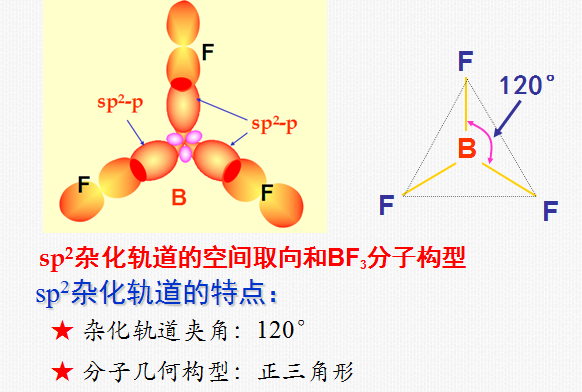
2)sp2 杂化
同一原子内由一个s轨道和二个p轨道发生的杂化
sp2杂化后得到3个sp2杂化轨道。
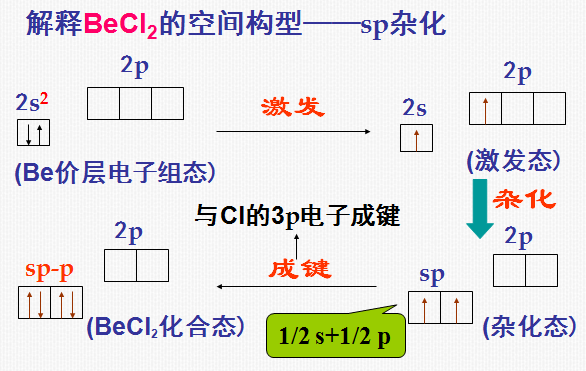
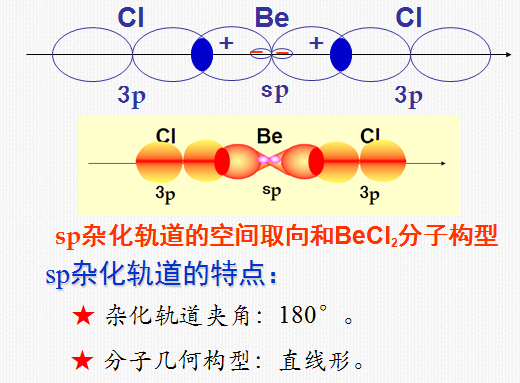
3) sp杂化
同一原子内由一个s轨道和一个p轨道发生的杂化。
sp杂化后得到2个sp杂化轨道。
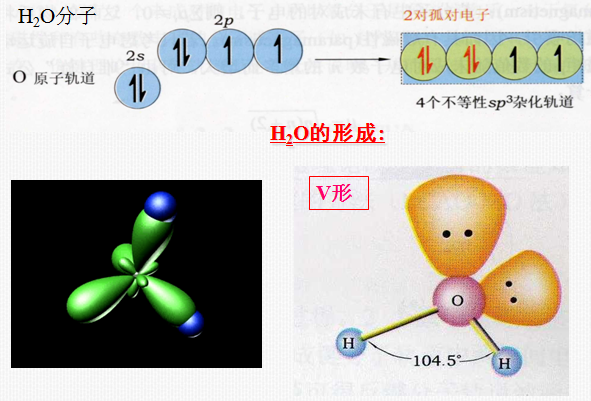
4) 等性杂化和不等性杂化
轨道的s、p的成分相同,能量、成键能力也都相等,这样的杂化称为等性杂化。但当有不参与成键的孤对电子存在时,可使组成的几个杂化轨道中的s、p成分不等,从而产生不完全等同轨道的杂化,称为不等性杂化。
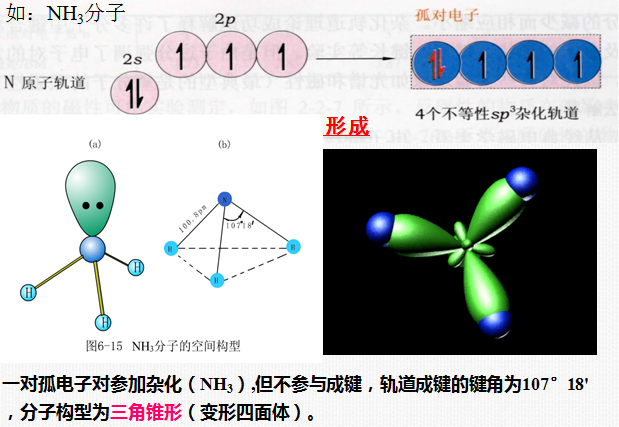
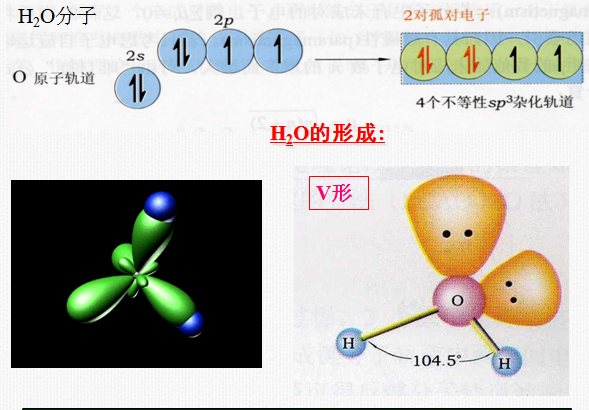
s-p杂化与分子的几何构型
化轨
杂化轨道类型 |
sp |
sp2 |
sp3 | |||
参与杂化的 原子轨道 |
1个ns,1个np |
1个ns,2个np |
1个ns,3个np | |||
杂化轨道 数目 |
2 |
3 |
4 | |||
杂化轨道中 孤电子对数 |
0 |
0 |
0 |
1 |
2 | |
空间构型 |
直线型 |
平面三角形 |
正四面体 |
三角锥 |
V形 | |
杂化轨道间的夹角 |
180° |
120° |
109°28′ | |||
成键能力 |
依次增强→ | |||||
实例 |
BeX2、CO2、 CS2 、HgCl2、C2H2 |
BX3、CO32-、 C2H4 |
CH4、SiH4、SiCl4、CCl4 |
NH3、PH3、NCl3 |
H2S、H2O、HClO 、H2O | |
分子极性 |
无 |
无 |
无 |
有 |
有 | |
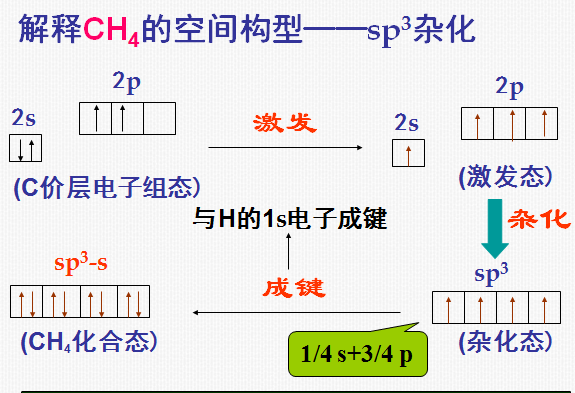
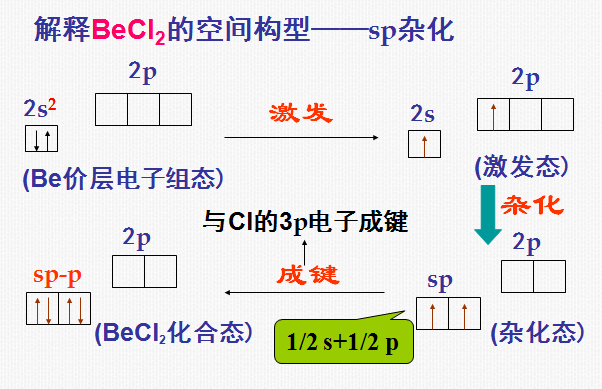
杂化轨道理论的不足
一个分子具有什么样的空间构型,中心原子采用什么类型的杂化轨道,这些问题杂化轨道理论都不能解决,在不少情况下难以预言,一般只能用来解释某些已知空间构型的分子。
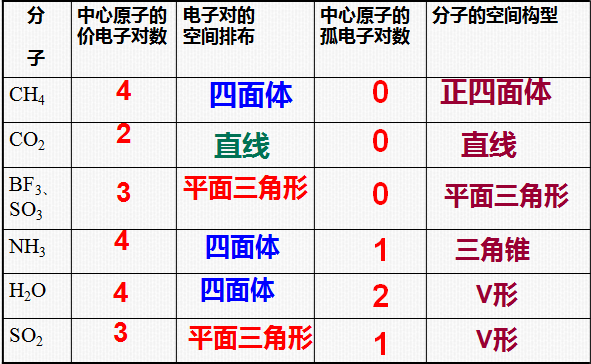
3.2.4 价层电子对互斥理论
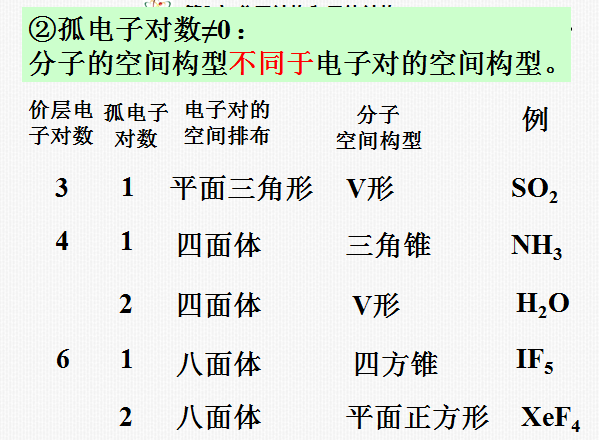
分子的共价键的电子对以及孤对电子对由于相互排斥作用,而趋向尽可能彼此远离,分子尽可能采取对称的空间构型。
仅依据分子中成键电子对及孤对电子对的数目
就可以判断分子属于哪种几何构型!
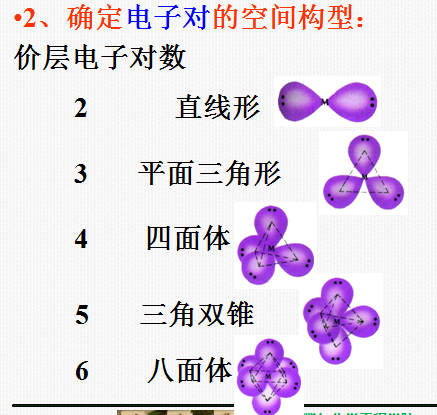
推断分子或离子的空间构型的具体步骤:
1、确定中心原子的价层电子对数,以AXm为例 (A—中心原子,X—配位原子) :
价层电子对数=1/2[A的价电子数+X提供的价电子数×m

CO2 , H2O,NH3 ,CH4, SO2
2 4 4 4 3

价键理论—解决了共价键的饱和性和方向性,共价键的本质;
杂化和价层电子对理论解决分子的空间构型;
不能解决某些物理性质问题,如O2具有成单电子,有磁性(或顺磁性)
3.2.5 分子轨道理论-简称MO法
分子轨道理论的要点
⑴ 原子在形成分子时,分子中的电子不再从属于某个原子,而是在整个分子空间范围内运动。
在分子中每个电子的运动状态也可用波函数Ψ来描述,Ψ称为分子轨道。
⑵ 每一个分子轨道Ψi都有其相应的能量Ei和图像。按照分子轨道能量的大小,可以排列出分子轨道的近似能级图。
⑶ 分子轨道由能量相近的不同原子轨道线性组合而成,形成的分子轨道的数目同参与组合的原子轨道数目相同。
⑷ 原子轨道组合成分子轨道时,分子轨道中电子的排布遵循能量最低原理、泡利不相容原理和洪特原则。
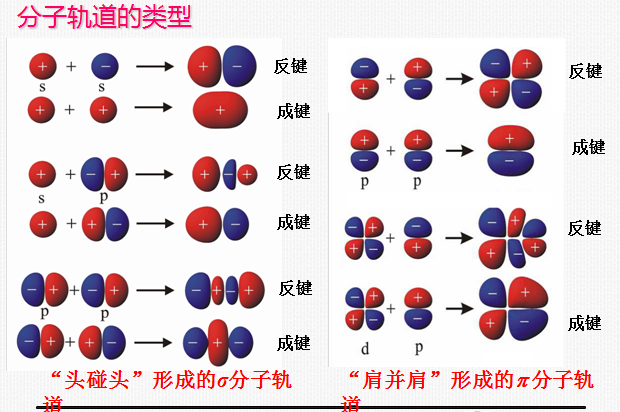
2 . 原子轨道线性组合的类型
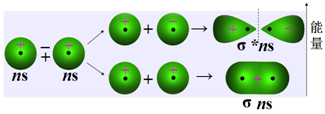
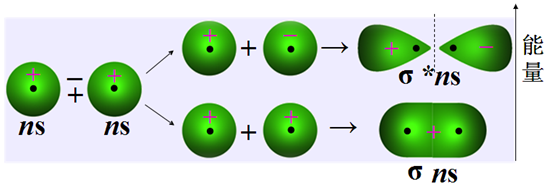
Ψ1= C1(Ψa+Ψb ),两个符号相同的波函数叠加(+ +或- -)(或两原子轨道相加),形成成键分子轨道(s) 。
Ψ2= C2(Ψa-Ψb ),两个符号相反的波函数叠加(+ -)(或两原子轨道相减),形成反键分子轨道( s* )
道的 轨
轨
道的s、
p的
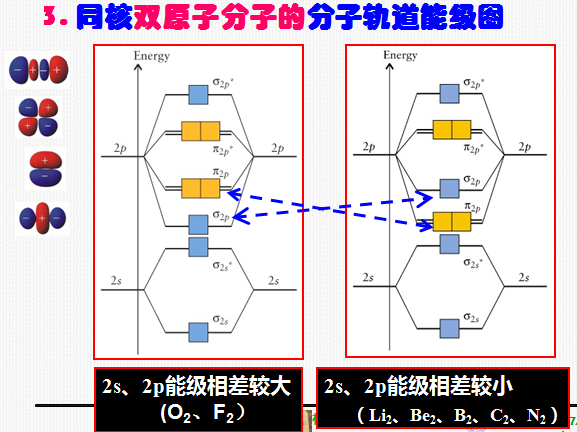
双原子分子的轨道能级与电子结构
成分相
同核双原子分子

4. 分子轨道理论的应用
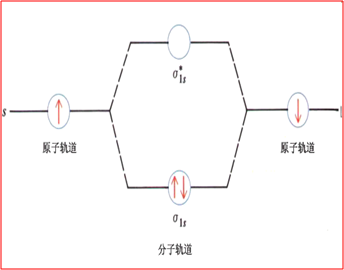
(1) H2的分子轨道能级

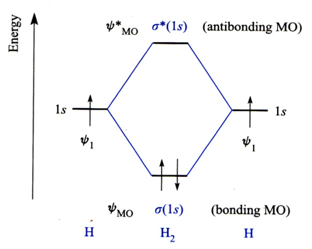
(2) N2的分子轨道能级
,能N2的分子轨道电子排布式
![]()
![]()
N2氮分子中的三键十分牢固,因此氮分子性质非常稳定。
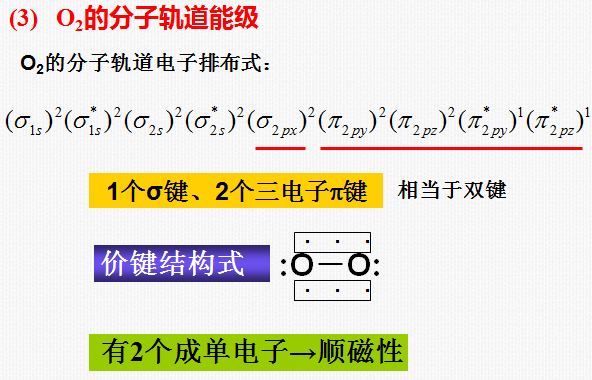
O2与N2比较:
①分子轨道能级次序不同。
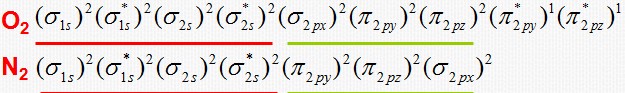
②由于O2比N2多两个电子,这两个电子占据了能级较高的反键轨道,因此,O2化学键没有N2分子的化学键牢固。
③由于O2分子中有两个自旋未配对的电子,所以O2分子具有顺磁性,N2分子没有自旋未配对的电子,具有反磁性(逆磁性)。
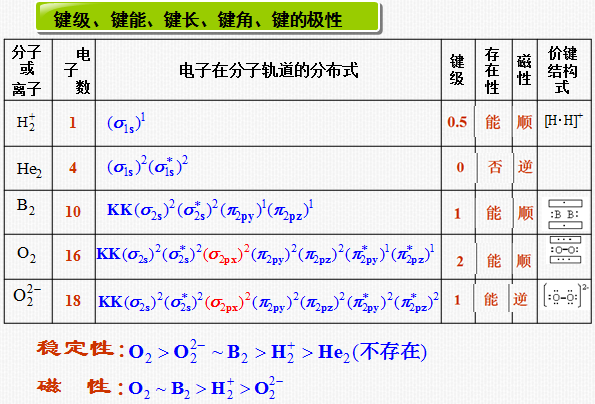
3.2.6 键参数(键级、键能、键长、键角、键的极性)
1. 键级
分子轨道法中成键电子数与反键电子数之差(即净成键电子数)的一半就是分子的键级。键级的大小表示两个相邻原子间成键的强度。
键级越大,分子越稳定;键级为零,分子不存在。
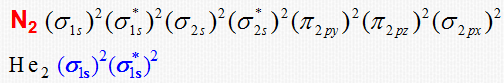
2. 键能(E)
在标准状态下,将1mol理想的气态分子AB,解离成理想的气态A原子和B原子所需的能量叫做A-B键的离解能,单位为kJ · mol-1 ,用符号D (A-B)表示。
双原子分子:键能E(A-B)=键离解能D(A-B)
D(H-H)=E(H-H)=432 kJ·mol-1
多原子分子:键能与键离解能有区别,如NH3中
NH2-H D1=435.1
NH-H D2=397.5
N-H D3=338.9
一般说,键能越大,化学键越牢固,含有该键的分子越稳定。
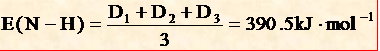
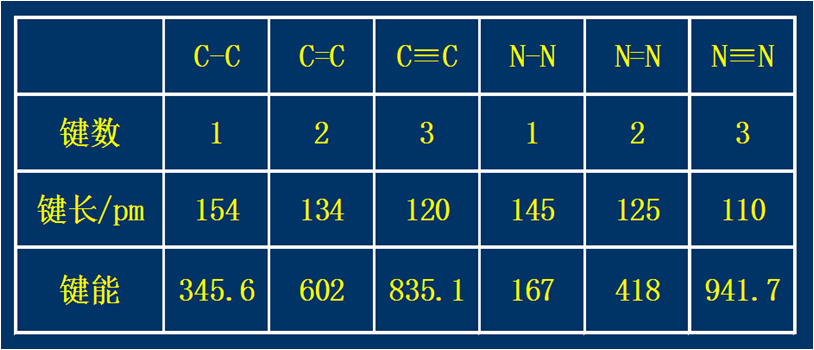
3. 键长
键长:分子中两个原子核间的平衡距离。
两原子间形成的键越短,表示键越强、越牢固。
4. 键角
键角:分子中键与键之间的夹角。
键角是反映分子空间结构的重要因素。
知道分子中所有键长和键角,就可确定分子的几何构型。
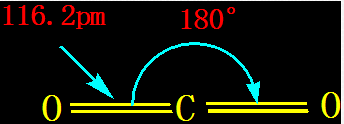
CO2,键长116.2pm,键角180°,直线型。
5. 键的极性
非极性共价键:成键原子的正、负电荷中心重合。H2,Cl2,金刚石,晶态硅等。
极性共价键:成键原子的正负电荷中心不重合。HCl,H2O等。
判断依据:电负性
成键原子的电负性差越大,键的极性越大。
H2 HI HBr HCl HF NaCl
△x 0 0.46 0.76 0.96 1.78 2.2
非极性键 │ ←极性共价键→│ 离子键
成键能力也都相等,这样的杂化称为等性杂化。电子云分布集中,成键时轨道重叠程度大,故杂化轨道的成键能力比杂化前的成键能力强,因此形成的分子更稳定。


