第3章 分子结构和晶体结构
第3章 分子结构和晶体结构-2015.10.21.ppt(下载附件 9.6 MB)
3.1 离子键理论与离子晶体
3.2 共价键理论
3.3 分子间力与氢键
3.4 原子晶体和分子晶体
3.5 金属键和金属晶体
3.6 离子的极化
分子或晶体中,原子(或离子)之间直接的、主要的和强烈的相互作用,称为化学键。
若原子原子之间形成了分子,则分子与分子之间也存在相对较弱的相互作用,称为分子间力或范德华力。
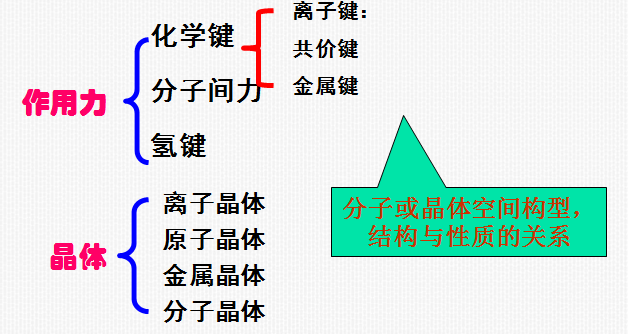

离子键:正、 负离子之间静电引力作用而形成的化学键
离子型化合物:由离子键形成的化合物。
![]() (以 NaCl 为例)
(以 NaCl 为例)
第一步 电子转移形成离子:
Na - e- —— Na+ , Cl + e- —— Cl—
相应的电子构型变化:
2s 2 2p 6 3s 1 —— 2s 2 2p 6 , 3s 2 3p 5 —— 3s 2 3p 6
形成 Ne 和 Ar 的稀有气体原子构型,形成稳定离子。
第二步 正负离子靠静电吸引, 形成化学键 。
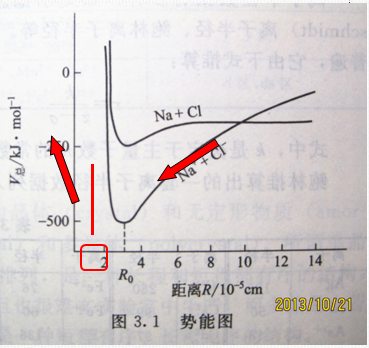
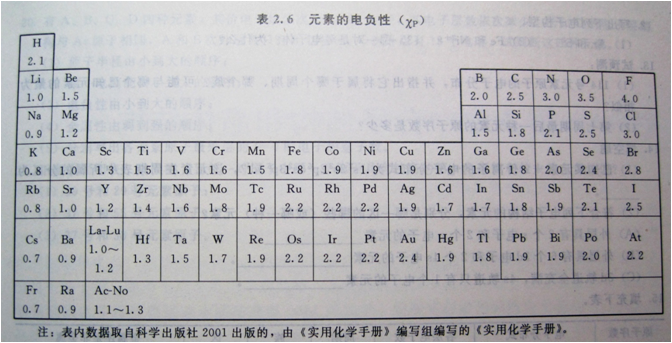
离子键的形成条件:元素的电负性差值要足够大,
电负性的差值x 越大,形成的离子键越稳定。

离子键的特征
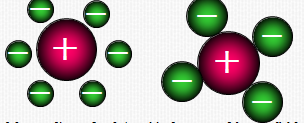
没有方向性:正负离子可近似地看成一个弥漫着电子云的圆球体,电荷分布球形对称,离子能从任何方向吸引带相反电荷的离子。
没有饱和性:只要空间许可,一个离子周围可同时和几个电荷相反的离子相互吸引。
离子键的离子性大小取决于电负性差值大小
电负性差值越大,电子的偏向越明显,相互作用越强。

1. 离子的电荷
离子电荷越高、半径越小、静电引力越强,则离子键越强,熔点越高。
2. 离子的半径
离子半径:假定晶体中中正、负离子为相互接触的球体,并将实验测得的正、负离子的平均距离视为正、负离子的半径之和。
离子半径的变化规律:
(1)同一主族元素的电荷相同的离子的半径,随电子层数增加而增大。
![]()
(2)同一周期电子层结构相同的正离子的半径,随离子电荷增加而减小;而负离子的半径随离子电荷增加而增大。
r(Na+)>r(Mg2+)>r(Al3+) >r(Si4+)
r(F-)<r(O2-)
(3)同一种元素的负离子半径大于原子半径而正离子半径小于原子半径,且正电荷越多,半径越小。例如:![]()
(4)对等电子离子言,离子半径随负电荷的降低和正电荷的升高而减小。例如:r(Mg2+)< r(Na+) <r(F-)<r(O2-)

3.1.3 离子晶体
1. 晶体的基本概念
固体物质按其中原子排列的有序程度不同可分为晶体和无定形物质两种。
晶体 是质点(分子、离子、原子)在空间有规则的排列成的,具有整齐外形,以多面体出现的固体物质。
晶体又分单晶体和多晶体。
单晶:结晶体内部的微粒在三维空间呈有规律地、周期性地排列,是一种长程和短程都有序的结构。
多晶:由若干不同取向的小单晶体(即晶粒)组成的一种晶体,是一种短程有序,长程无序的结构。
晶体的特征:
(1) 有规则的几何构型;
(2) 有固定的熔点;
(3) 有各向异性。
结点(节点):晶体中规则排列的微粒抽象为几何学中的点。
空间点阵:这些结点的总和。
晶格:沿着一定方向按某种规则把结点联结起来,描述各种晶体内部结构的几何图像——晶体的空间格子,简称为晶格。
晶胞:在晶格中,能表现出其结构一切特征的最小重复单位。
晶格是由晶胞在三维空间无限重复而构成。
根据晶胞的特征,可以划分成七个晶系:
表3.4 七个晶系的性质
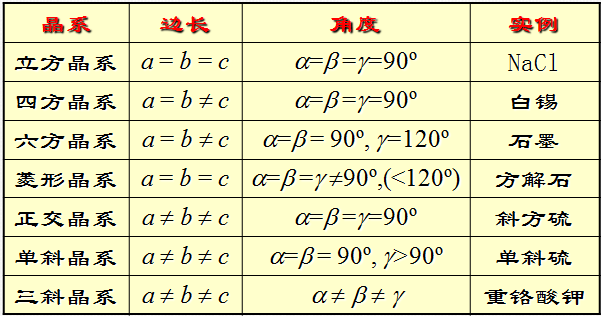
2、 离子晶体的结构类型及其性质
正、负离子通过离子键结合堆积形成离子晶体 。
离子晶体无方向性和饱和性,因此晶体中不存在单个分子,而是一个巨大的分子,如NaCl只表示晶体的化学式,而不是其分子式。
典型的离子晶体:
强碱、部分金属氧化物、部分盐类
在离子化合物中,各种离子的配位数是确定的。离子配位数的多少主要决定于阴阳离子的半径比。
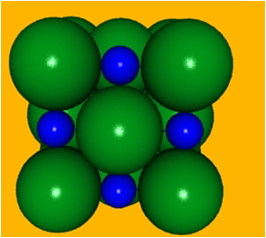
离子晶体中正负离子在空间的排布情况多种多样,对于最简单的AB型离子晶体,有三种典型的空间构型:
NaCl型、CsCl型和立方ZnS型。
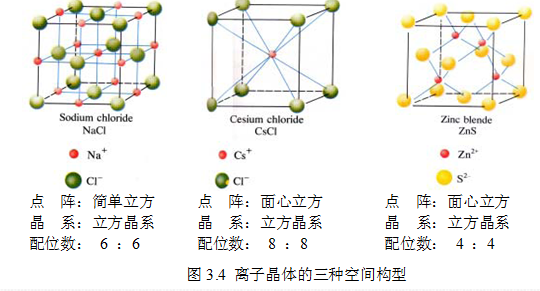
【 NaCl 型 】
1、在NaCl晶体中每个Na+同时吸引着_6_个Cl-。
2、它们所围成的空间几何构型是 __正八面体_________。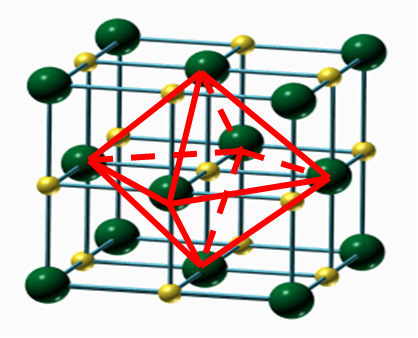
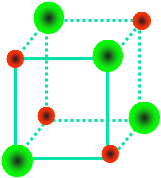
3、在NaCl晶体的一个晶胞中,
Cl-的个数等于4 ,Na+的个数等于4
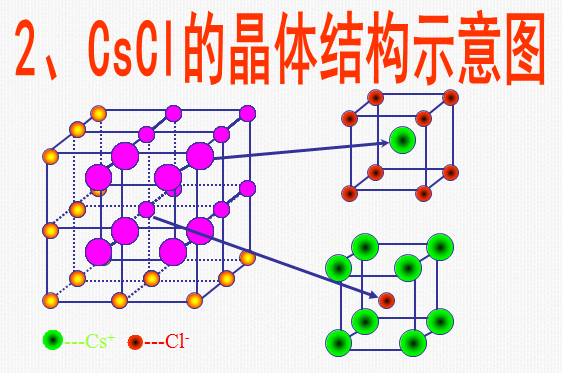
3. 离子晶体的性质
晶格能:在标准状态下,由相互远离的气态正、负离子生成1mol离子晶体时所释放的能量。常用U表示,单位:kJmol-1。
晶格能的绝对值越大,离子晶体的正、负离子间作用力越强,形成离子键的强度越大。
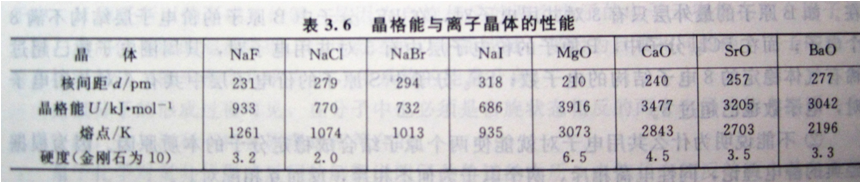
离子晶体
① 熔沸点较高,硬度较大,难挥发,难压缩。
② 水溶液或者熔融状态下能导电。


