2.3 多电子原子核外电子的分布
第2章-原子结构和元素周期律.ppt(下载附件 5.92 MB)
•2.3.1 多电子原子轨道的能级
•2.3.2 基态原子中电子分布的原理
•2.3.3 基态原子中电子的分布
•2.3.4 简单基态阳离子中电子的分布
2.3.1 多电子原子轨道的能级
•近似能级图是按原子轨道的能量高低顺序排列的,能量相近的划为一组,成为能级组,共七个能级组。

–能级组的存在,是周期表中化学元素可划分为各个周期及每个周期应有元素数目的根本原因。
-对于4、5、6、7能级组,在一个能级中包含不同电子层的能级现象称为能级交错
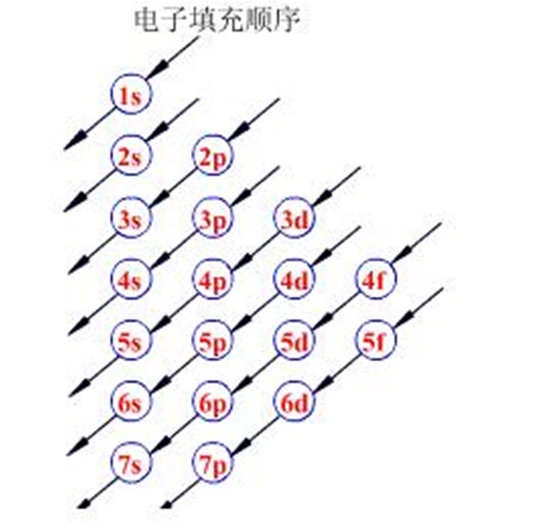
n=1, 2, 3, 4, 5, 6, 7
电子层 K L M N O P Q








•一个原子中不允许有两个电子处于完全相同的状态。
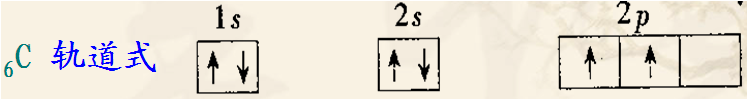



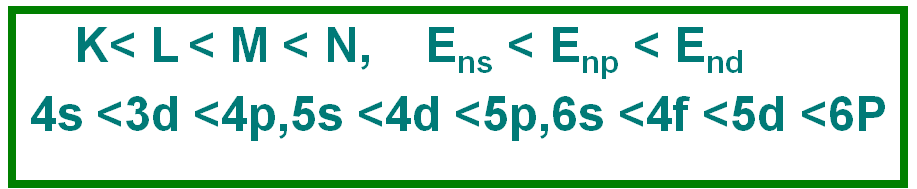




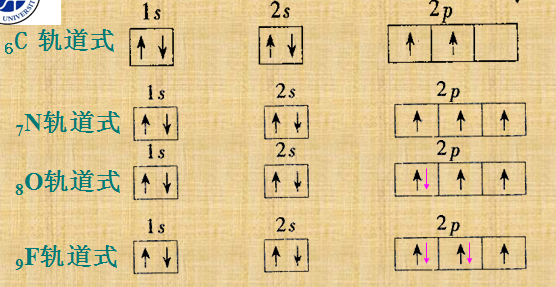
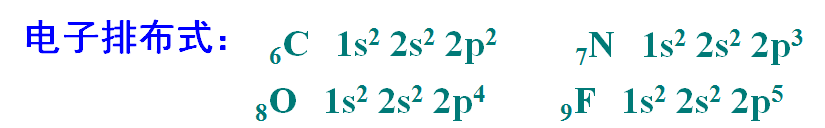
2.3.3基态原子中电子的分布
(1) 按电子层的顺序写。
(2) 一般地按照三原理书写。个别例外,应以实验为依据。
3) 可用原子实(稀有气体元素符号)简写电子排布式。
例: ① 26Fe 1s22s22p63s23p63d64s2
26Fe [Ar] 3d64s2
② 47Ag 1s22s22p63s23p63d104s24p64d105s1
47Ag [Kr] 4d105s1
① 1H~2He 1s1 ~ 1s2
3Li~ 10Ne 1s22s1 ~ 1s22s22p6
11Na~18Ar 1s22s22p63s1 ~ 1s22s22p63s23p6
19Na~36Kr 1s22s22p63s23p64s1 ~ 1s22s22p63s23p63d104s24p6
② 24Cr 1s22s22p63s23p63d44s2(错误)
24Cr 1s22s22p63s23p63d54s1(正确)
29Cu 1s22s22p63s23p63d94s2(错误)
29Cu 1s22s22p63s23p63d104s1(正确)
注意:
电子排布顺序与书写顺序并不一致:
① 25Mn [Ar]4s23d5(排布顺序)
② 25Mn [Ar]3d54s2
(书写顺序)
2.3.4 简单基态阳离子中电子的分布
(1)基态原子外层电子填充顺序:
→ns →(n-2)f →(n-1)d →np
(2)价电子解离顺序:
→np→ns→(n-1)d →(n-2)f
① 25Mn [Ar]3d54s2
② 25Mn2+ [Ar] 3d5


