2.2 原子的量子力学模型
第2章-原子结构和元素周期律.ppt(下载附件 5.92 MB)
2.2.1 微观粒子的运动特征
2.2.2 波函数和原子轨道
2.2.3 四个量子数
2.2.1 微观粒子的运动特征
(一)量子性
•如果某一物理量的变化是不连续的,这一物理量就是量子化的,其最小单位---量子;
•量子化特征——表征微观粒子运动状态的某些物
理量具有不连续变化的特征。
(二)波粒二象性
L deBroglie的假设
1905年爱因斯坦根据光的干涉、衍射和光电效应,提出了光具有波粒二象性
1924年法国物理学家德布罗意(L.de Brogile)在研究电子的运动规律时,受光的波粒二象性的启发,大胆提出了电子等实物粒子(微观粒子:原子、质子、中子)不仅具有粒子性,也具有波动性
的假设。提出了“物质波”公式,称为德布罗意关系式,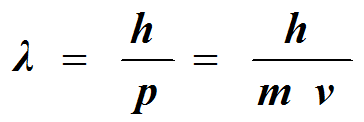
P为微粒的动量,m为微粒的质量, υ为微粒的运动速度, h为普朗克常数, λ为微粒波的波长。
德布罗意关系式把微观粒子的粒子性p (m 、υ)和波动性λ统一起来。
德布罗意的微观粒子波动性的假设三年后被多个实验所证实。如:
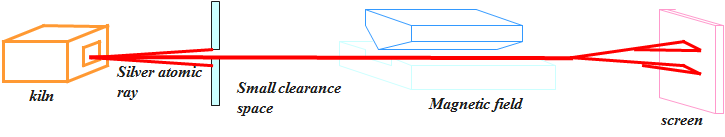
电子衍射实验 1927年,美国的Davisson和Germer用电子束代替X射线,用一薄层镍的晶体代替衍射光栅,投射到照相底片上,得到了衍射图像。证明了电子束同X射线一样具有波动性。如下图:
(三)微观粒子运动的统计性:
考察电子衍射实验,
若电子流很强,则很快得到明暗相间
的衍射环纹—显示波动性;
若电子流强度很小,电子一个一个从
阴极灯丝飞出,底片上会出现一个一
个的点—显示电子具有粒子性。经一
定时间同样得到明暗相间的衍射环纹。
亮环纹处,衍射强度大,电子出现的机会多,即几率大;
暗环纹处则相反。
量子力学认为,原子中核外电子的运动不象经典力学
认为的那样有确定的轨道,但具有按几率分布的统计
性规律。
2.2.2波函数和原子轨道
波函数是描述核外电子运动状态的数学函数式,又是
空间坐标Ψ(x,y,z)的函数,其空间图象可理解为电子运动的
空间范围,俗称“原子轨道”。
波函数Ψ通常叫做原子轨道(两者是同义语)
描述核外电子运动状态——SchrÖdinger方程
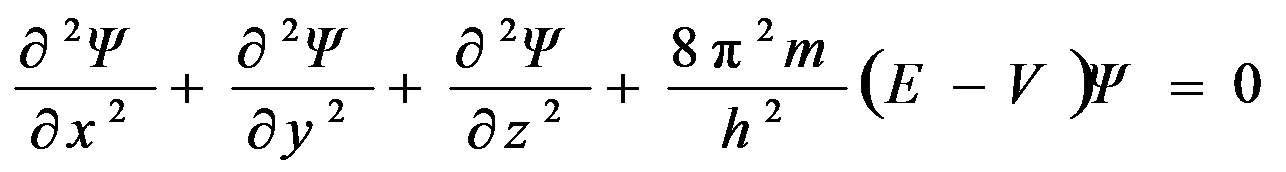
1. SchrÖdinger方程
(二阶偏微分方程)
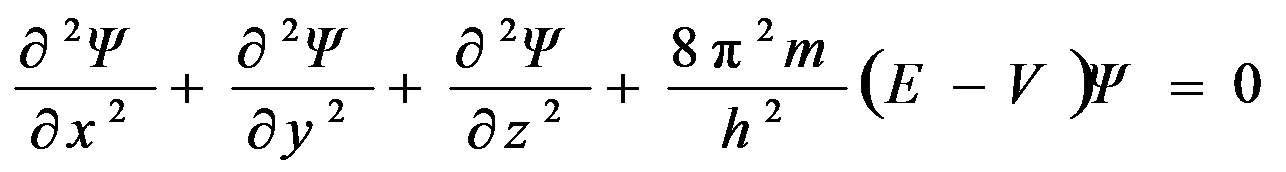
综上所述:Ψ是描述核外电子运动状态的数学函数式;
在量子力学中把每一个这种波函数称为原子轨道;
它代表原子中核外电子的一种运动状态;
每一种原子轨道即每一个Ψ都有与之对应的E。
SchrÖdinger方程的物理意义:
方程的每一个特定的解 Ψ(r,θ, ) n,l,m 表示原子中电子的一种运动状态,与Ψ 相应的常数 E 即为该状态的能量。
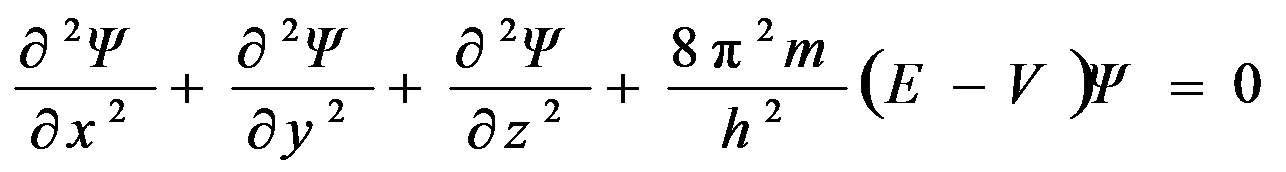
★ 解得的ψ不是具体的数值, 而是包括三个常数 (n, l, m)和三个变量
(r,θ,φ)的函数式Ψn, l, m (r,θ,φ) ;
★ 数学上可以解得许多个Ψn, l, m (r,θ,φ), 但其物理意义并非都合理;
★为了讨论方便,一般将三个量子数n, l, m确定的一个波函数式称为一个原子轨道.这里的轨道已经失去本来的意义。
波函数 = 薛定锷方程的合理解 = 原子轨道
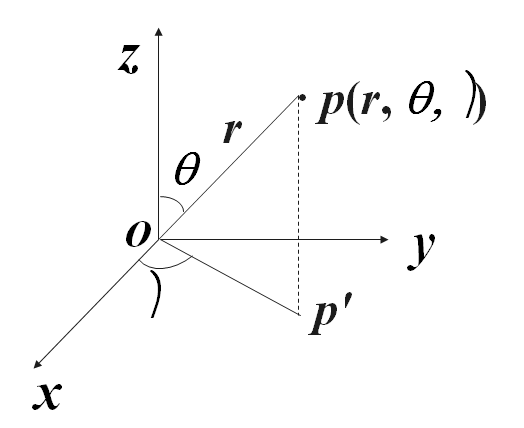
直角坐标( x,y,z)与球坐标(r,θ,φ)的转换
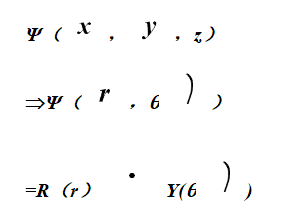
![]() 波函数的径向部分——只与离核半径有关
波函数的径向部分——只与离核半径有关
![]() 波函数的角度部分——只与角度θ,φ有关
波函数的角度部分——只与角度θ,φ有关
根据量子力学理论,电子不是沿着固定轨道绕核旋转,而是在原子核周围的空间很快地运动着。因此,我们不能肯定电子在某一瞬间在空间的什么位置上。即,在原子核外运动的电子没有运动的轨道。
但这并不是说电子运动没有规律性,大量电子的运动或一个电子的千百万次运动具有一定的规律性。可以统计的方法推算出电子在空间出现的几率大小。
电子运动具有一定的几率分布规律。
2. 概率密度和电子云
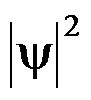 表示:电子在核外空间某处单位微体积内出现的几率 ——即概率密度;
表示:电子在核外空间某处单位微体积内出现的几率 ——即概率密度;
几率(概率)——电子在核外空间某一区域出现的机会;
电子云——以小黑点疏密描述电子在核外出现的几率
密度分布的空间图象。
是电子在核外空间出现的几率密度大小的形象化描述

基态氢原子1s电子云
(1)原子轨道的角度分布
表示原子轨道的形状及其在空间的伸展方向



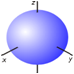
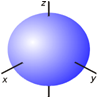
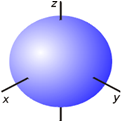
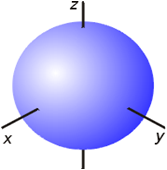
(2)电子云的角度分布图
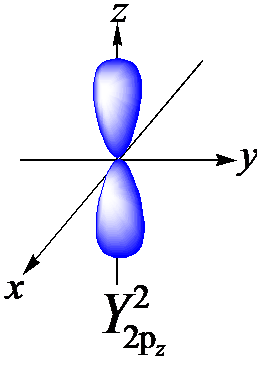


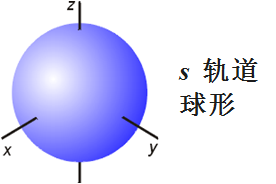
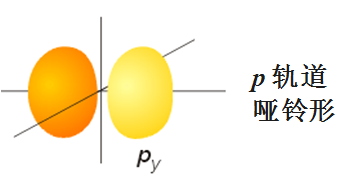
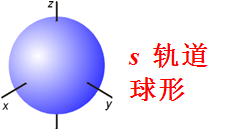
s电子云:球形对称
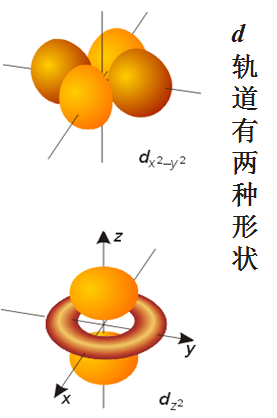
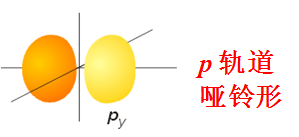
p电子云:哑铃形,px py pz
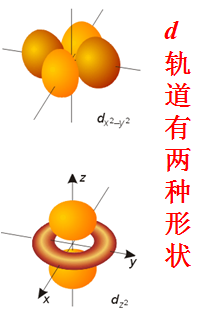
d电子云:花瓣形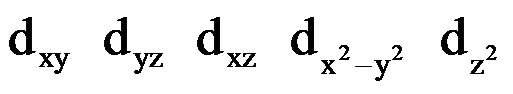
2.2.3 描述电子运动状态的四个量子数
像玻尔的固定轨道一样, 波动力学的轨道也由量子数所规定. 、
不同的是, 原子轨道用三个量子数而不像玻尔轨道只用一个量子数描述.
(1)主量子数n
◆ 确定电子出现几率最大处离核的距离,能量高低。
◆ 不同的n 值,对应于不同的电子层
1 2 3 4 5……..
K L M N O……..
(2) 角量子数l
◆ 与角动量有关,对于多电子原子, l也与E 有关
◆ l 的取值 0,1,2,3……n-1(亚层)
s, p, d, f…...
◆ l 决定了原子轨道或者电子云角度部分的形状
n=1, l=0, 1s
n=2, l=0,1, 2s,2p
n=3, l=0,1,2 3s,3p,3d
n=4, l=0,1,2,3 4s,4p,4d,4f
磁量子数m
◆ 与角动量的取向有关,取向是量子化的
◆ m可取 0,±1, ±2……±l,共有 2l+1 种可能
◆ 决定了原子轨道或电子云在空间的伸展方向
◆ n、l相同而m 值不同的轨道互为等价轨道
| l | 0 | 1 | 2 |
| m | 0 | 0,+1,-1 | 0,+1,-1,+2,-2 |
| 原子轨道符号 | s | pz,px,py |
|
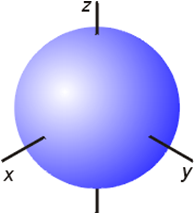
s轨道 (l = 0,m = 0 ) :
m 一种取值, 空间一种取向, 一条 s轨道.
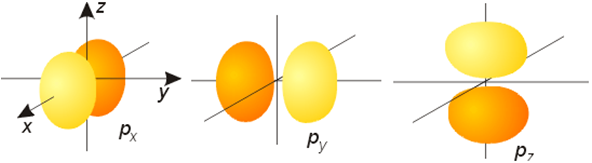

p轨道(l= 1,m = +1, 0, -1)
m 三种取值, 三种取向, 三条等价(简并) p轨道.
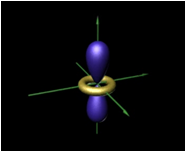

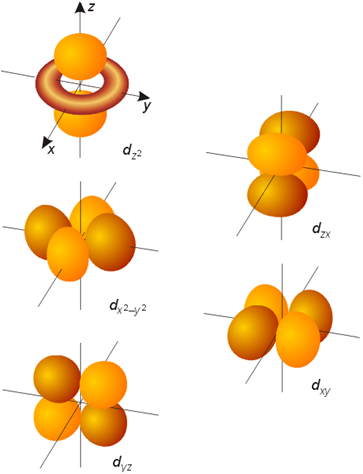
d 轨道(l = 2,m = +2, +1, 0, -1, -2) :
m 五种取值, 空间五种取向, 五条等价(简并)d 轨道.
本课程不要求记住 f 轨道具体形状!
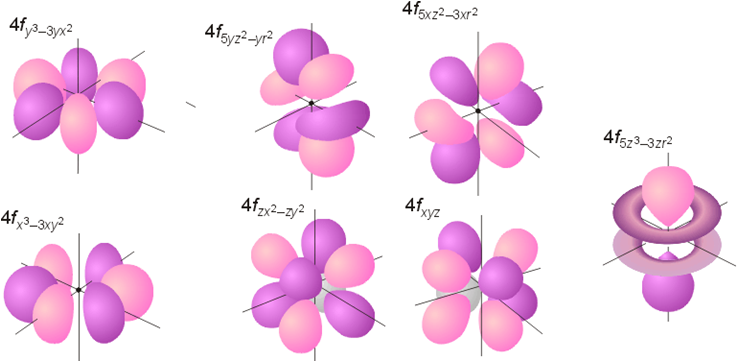
f 轨道 ( l = 3,m = +3, +2, +1, 0, -1, -2, -3 ) :
m 七种取值, 空间七种取向, 七条等价(简并)f轨道.
4) 自旋量子数ms
◆ 描述电子绕自轴旋转的状态
◆ 自旋运动使电子具有类似于微磁体的行为
◆ ms 取值+1/2和-1/2,分别用↑和↓表示
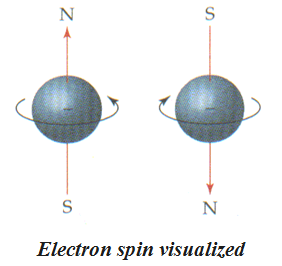
想象中的电子自旋
★两种可能的自旋方向:
正向(+1/2)和反向(-1/2)
★产生方向相反的磁场
★相反自旋的一对电子, 磁场相互抵消.
内容小结:核外电子运动状态的描述


主量子数— n
取值 1, 2, 3, 4, … n 为正整数(自然数)
能量量子化
光谱学上用K , L , M , N , … 表示
意义:
表示电子离核平均距离远近及电子能量高低的量子数。n= 1表示第一层(K层),能量最低,离核最近。n的数值大,电子距离原子核远,则具有较高的能量。
主量子数— n
| 主量子数n | 1 | 2 | 3 | 4 | 5 | 6 | 7 | ··· |
| 电子层 | 一 | 二 | 三 | 四 | 五 | 六 | 七 | ··· |
| 符号 | K | L | M | N | O | P | Q | ··· |
角量子数— l
用来描述核外电子运动所处原子轨道(或电子云)形状的,也是决定电子能量的次要因素。 对于确定的主量子数 n,角量子数 l 可以为 0,1, 2, 3, 4, … ( n-1 ), 共 n个取值,光谱学上依次用 s , p , d , f , g ,… 表示 。
意义 角量子数 l决定原子轨道的形状


磁量子数— m
描述电子自旋方式的量子数,用 ms 表示。
ms称为自旋量子数,取值只有两个,+ ½ 和-½ 。电子的自旋方式只有两种,通常用 “ ” 和 “ ¯ ”表示顺时针、逆时针。
(3)量子数和原子轨道的关系
| n | l | m | 原子轨道 | ms | ||
| 取值 | 符号 | 取值 | 符号 | 取值 | 符号 | 取值 |
| 1 | K | 0 | s | 0 | ±1/2 | |
| 2 | L | 0 | s | 0 | ±1/2 | |
| 1 | p | 0, ±1 | ±1/2 | |||
| 3 | M | 0 | s | 0 | ±1/2 | |
| 1 | p | 0, ±1 | ±1/2 | |||
| 2 | d | 0, ±1 ±2 | ±1/2 | |||
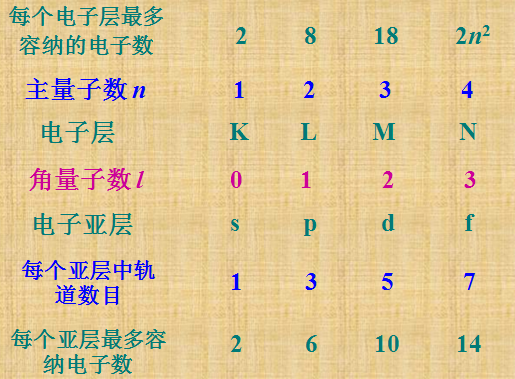
量子数,电子层,电子亚层之间的关系
END


