一、蛋白质分离纯化方法
1.沉淀法(precipitation):蛋白质、酶的初步纯化往往用沉淀法。原理是使蛋白质胶体颗粒破坏,从而沉淀蛋白质。常用盐析法、有机溶剂沉淀法、等电点沉淀法、与靶物质结合沉淀法(如抗体—抗原)等。
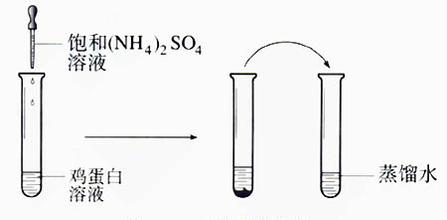

2.按照分子大小分离的方法
v超滤法、透析法(即膜分离方法)、超速离心法。其中透析法可用于生物大分子物质的浓缩、分级和脱盐。
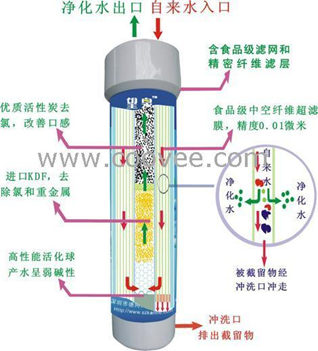
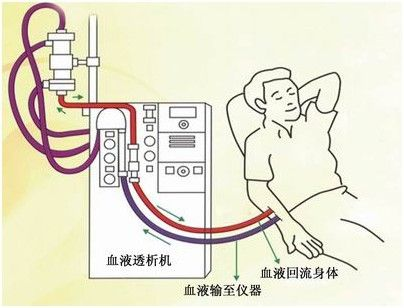
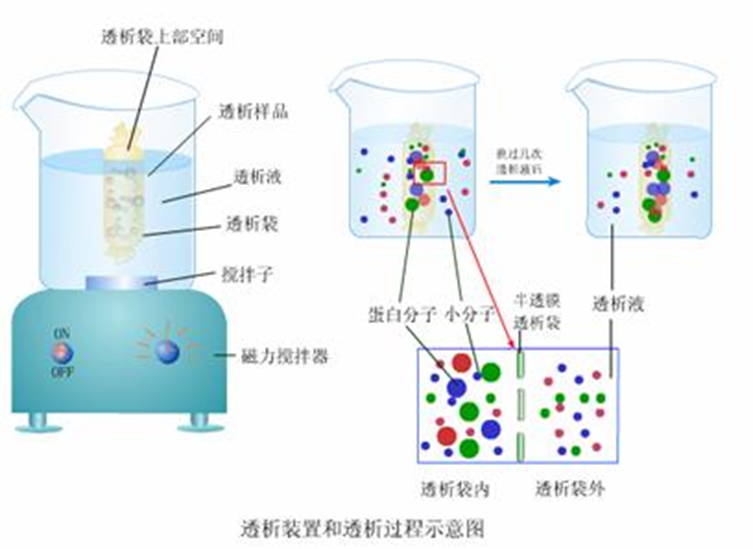
3.按分子所带电荷进行分离的方法
v氨基酸、多肽、蛋白质、酶均为两性电解质。它们具有等电点,在离开等电点的pH时便会带正或负电荷。例如某蛋白质等电点为7.0,当溶液pH为4.0时,分子则带有正电荷。由于具有该性质,利用带电性质进行分离是极其有效的方法。
v利用电学性质进行分离的方法有离子交换柱层析法、电泳法、等电聚焦电泳法等。
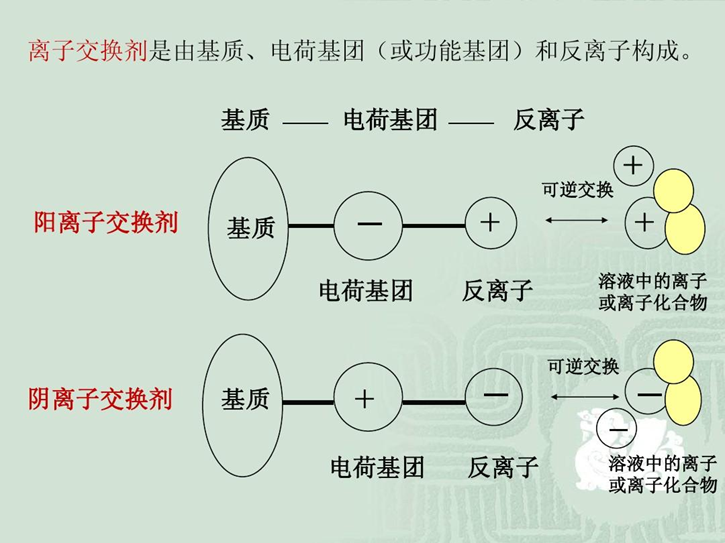
离子交换层析(IonExchange Chromatography,IEC)
v是以离子交换剂为固定相,依据流动相中的组分离子与交换剂上的平衡离子进行可逆交换时的结合力大小的差别而进行分离的一种层析方法。
v在生物化学及临床生化检验中主要用于分离氨基酸、多肽及蛋白质,也可用于分离核酸、核苷酸及其它带电荷的生物分子。
v操作过程:预处理和装柱--加样与洗脱。

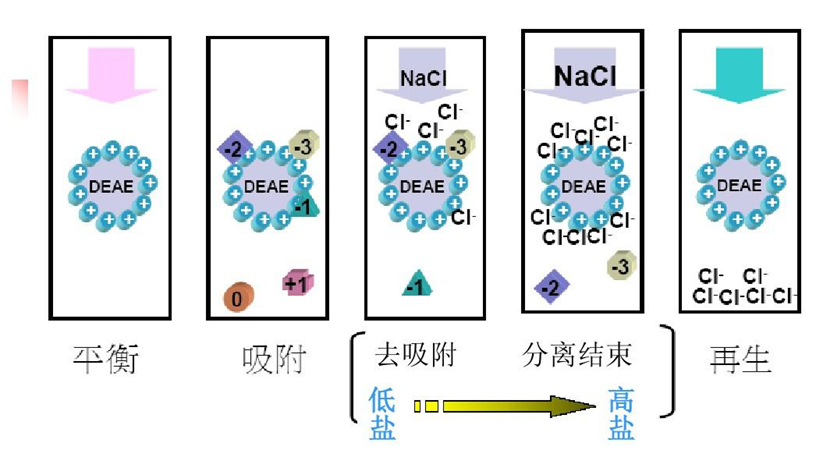
DEAE-纤维素为二乙氨乙基纤维素,是阴离子交换剂。
电泳法
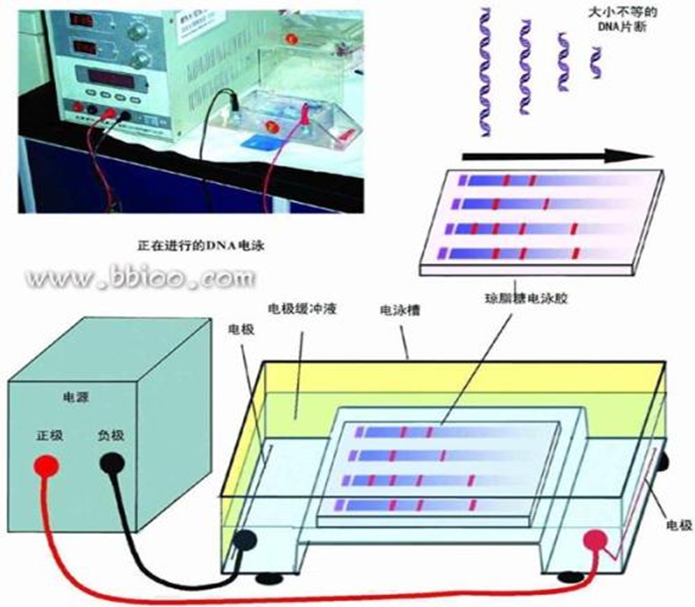
是指带电荷的供试品(蛋白质、核苷酸等)在惰性支持介质(如纸、醋酸纤维素、琼脂糖凝胶、聚丙烯酰胺凝胶等)中,于电场的作用下,向其对应的电极方向按各自的速度进行泳动,使组分分离成狭窄的区带,用适宜的检测方法记录其电泳区带图谱或计算其含量(%)的方法。
4.亲和层析法
v大部分生物活性物质都有其作用的靶物质,如酶与底物(或抑制剂)、抗原与抗体、激素与受体等,它们之间有特异的亲合作用,利用该性质设计的特异层析分离技术称为亲和层析。
v亲和层析分离专一性强,操作简便,是当前应用很广泛的分离方法之一。
v另外,最近出现的新方法还有疏水层析等。

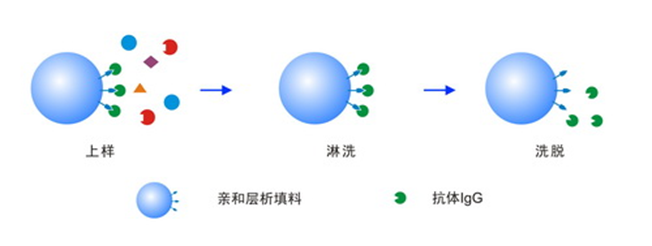
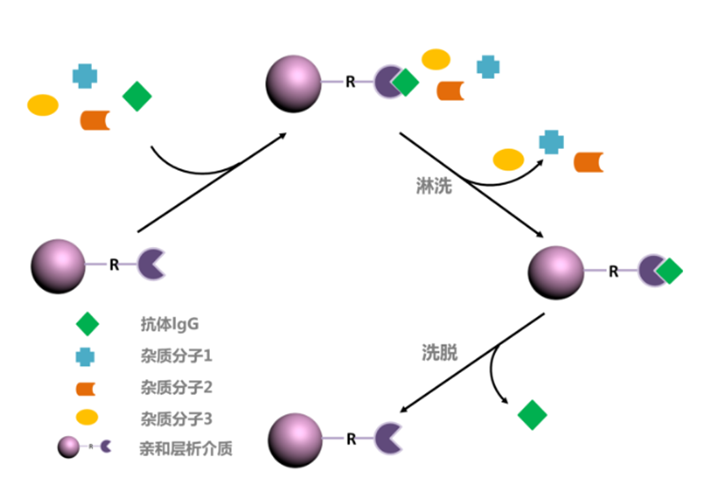
黄曲霉毒素B1亲和层析
v黄曲霉毒素B1亲和层析柱是以抗原抗体反应为基础,在柱体内部的载体上偶联有抗黄曲霉毒素B1的抗体,该抗体可与黄曲霉毒素B1产生特异性结合,通过淋洗除去无关杂质,再通过洗脱操作将目标物黄曲霉毒素B1洗脱,取最终的洗脱液用于分析。
v适用于玉米、大豆、花生、小麦、大麦和大米等谷物样本以及成品饲料样本的检测。

黄曲霉毒素B1亲和层析示意图
疏水层析原理如下:
v蛋白质表面一般有疏水与亲水基团,疏水层析是利用蛋白质表面某一部分具有疏水性,与带有疏水性的载体在高盐浓度时结合。在洗脱时,将盐浓度逐渐降低,因其疏水性不同而逐个地先后被洗脱而纯化,可用于分离其它方法不易纯化的蛋白质。
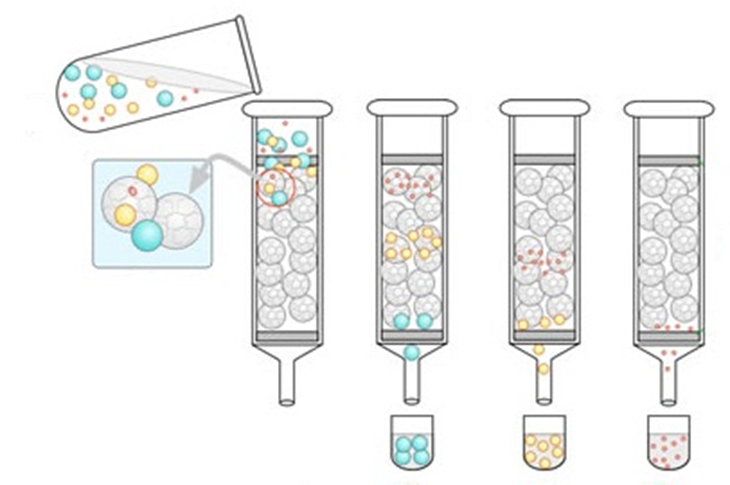
疏水层析原理示意图
二、核酸类制品的分离纯化方法
v核酸类药物生产方法主要有提取法和发酵法。
v提取法生产DNA和RNA,先提取核酸和蛋白质复合物,再解离核酸与蛋白质,然后分离RNA与DNA。
v发酵法主要用于生产单核苷酸。
三、糖类制品的分离纯化方法
v由于各种糖类制品的性质和原料来源不同,没有统一规范的提取和纯化工艺。这里只介绍多糖和黏多糖的一般分离纯化方法。
v黏多糖是含氮的不均一多糖,是构成细胞间结缔组织的主要成分,也广泛存在于哺乳动物各种细胞内。化学组成为糖醛酸和酪氨基己糖交替出现,有时含硫键。也称为糖胺聚糖。
(1)提取方法 (extraction)
v非降解法:适用于从含一种黏多糖的动物组织中提取粘多糖,提取采用的溶剂是水或盐溶液。
v降解法:适用于从组织中提取结合比较牢固的黏多糖。如从软骨中分离提取硫酸软骨素,就是用碱处理进行降解。又如用酶处理法可提取与蛋白质结合的多糖。
(2)分离方法(isolation)
v常用的分离方法是沉淀法和离子交换层析法。
v1.乙醇沉淀法(alcohol precipitation):是从提取液中沉淀多糖的最简易方法,也适用于分级分离。4-5倍体积的乙醇可以使任何结缔组织中的黏多糖完全沉淀。用季铵化合物也可沉淀粘多糖。黏多糖的聚阴离子能与某些阳离子表面活性剂结合成不溶于水的盐,如十六烷基三甲基铵(CTA)等。
2.离子交换层析法:
v黏多糖的聚阴离子能够很好地被阴离子交换剂吸附和分离,如DowexI-X2(商品名)离子交换树脂、DEAE-离子交换纤维素(二乙胺乙基)等。洗脱可用NaC1溶液进行梯度洗脱。
四、脂类制品的分离纯化方法
(1)提取方法(extraction )
v脂类自然状态下是以结合形式存在的。非极性脂是与其他脂质分子或蛋白质分子的疏水区相结合的。
v提取脂质就是要选择适当的溶剂来破坏这种结合键,将脂质溶解出来。常用的溶剂有组合溶剂,醇是其中的主要成分,此外还有氯仿、甲醇、水等。
(2)纯化方法
1)沉淀法(precipitation):由于不同脂质在丙酮中溶解度不同,故常用它进行沉淀。
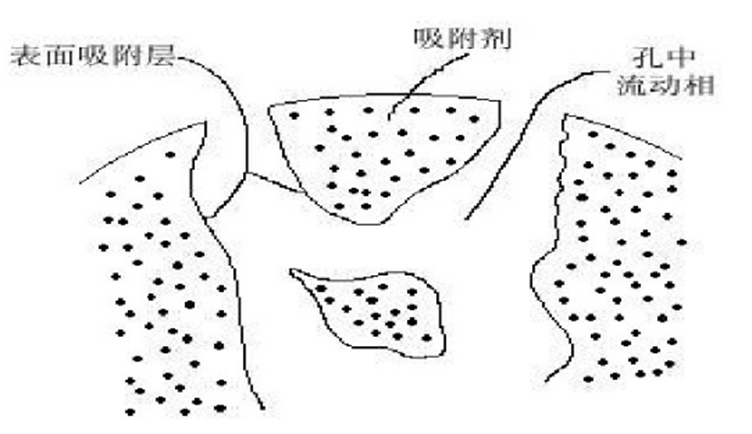
2)吸附层析法 (adsorption chromatography):常用吸附剂有硅胶、氧化铝等。它是通过极性和离子力等把各种化合物结合到固体吸附剂上。洗脱同一般是采用极性逐渐增大的洗脱液来进行,非极性的先流出,极性的后流出。
v吸附层析法是运用较多的一种层析方法,是化学实验中常用的分离方法。
v特别适用于很多中等分子量的样品(分子量小于1,000的低挥发性样品)的分离,尤其是脂溶性成分,一般不适用于高分子量样品如蛋白质、多糖或离子型亲水住化合物等的分离。
v吸附层析的分离效果,决定于吸附剂、溶剂和被分离化合物的性质这三个因素。

3)离子交换层析法
脂质分子的存在有非解离、两性离子和酸式解离三种状态。根据他们在一定pH条件下的解离情况,选择适当的离子交换剂可将它们提纯。如TEAE-纤维素对分离脂肪酸和胆汁酸等特别有效。
五、氨基酸类制品的分离纯化方法
(1)氨基酸的生产方法
a.蛋白质水解法(protein hydrolysis)
v水解法有酸水解(acid hydrolysis)碱水解(base hydrolysis)酶水解(enzyme hydrolysis)三种。
b.发酵法
①用盐酸、硫酸水解
为常用方法,其优点是水解迅速、完全,产物全部是L-型氨基酸,缺点是色氨酸全部被破坏,丝氨酸和酪氨酸部分被破坏。
②碱水解法
(用氢氧化钠或氢氧化钡100℃水解6小时)水解迅速彻底,且色氨酸不被破坏,但易产生消旋作用,较少应用。
③酶水解法
(蛋白质酶,一定温度,pH)反应条件温和,氨基酸不被破坏,但水解不够完全,很少用于生产氨基酸,主要用于生产水解蛋白和蛋白胨。
v菌株经过发酵后,从培养液中提纯氨基酸。
v化学合成与酶促合成法
v化学合成法一般得到的是DL-型氨基酸,尚需要对异构体拆分;酶促合成法也是酶工程在医药工业上的应用,优点是技术工艺简单,转化率高,副产物少和易提纯等。
(2)氨基酸的分离方法
v有沉淀法、吸附法和离子交换法。
a.沉淀法(precipitation):根据行成沉淀的原理不同分为两种:(1)依据不同氨基酸在水中或其他溶剂中的溶解度差异进行沉淀分离。(2)是用特殊试剂沉淀某种氨基酸,如用邻二甲苯-4-磺酸与亮氨酸形成不溶性盐沉淀,再用氨水分离,使亮氨酸游离出来。
b.吸附法(adsorption ):这是利用吸附剂根据氨基酸吸附力的差异进行氨基酸分离的方法。苯丙氨酸、酪氨酸、色氨酸的分离就是利用活性炭对其吸附的原理。
c.离子交换法(ion-exchange):氨基酸是两性电解质,在一定pH条件下,不同氨基酸带电性质及解离状态是不同的,因此在离子交换剂上被吸附的强度不同。常用的离子交换剂为强酸性阳离子交换树脂,洗脱主要用pH梯度洗脱。
(3)分离纯化技术应满足的要求
v技术条件要温和,要抑制宿主细胞或分泌产物中相应的酶活性,防止其消化降解待提纯产物,以保持目的产物的生物活性;
v选择性要好,优化选择与组合各种分离纯化技术方法以达到较高纯化倍数;
v去除细胞或分泌产物中非目标产物成分,同时尽量保持较高的目标产物成分的回收率;
v要直接衔接,不需要对物料加以处理或调整;
v整个分离纯化过程要快,时间短,能够满足高生产率的要求;
v保持环境清洁,防止杂物污染。


