固相反应是高温条件下固体材料制备过程中的一个普遍的物理化学现象。它是一系列材料(包括各种传统的、新型的金属材料和无机非金属材料)制备所涉及的基本过程之一。狭义地说,固相反应是固相和固相之间发生化学反应,生成新的固相产物的过程。广义地说,凡是有固相物质参与的化学反应都可称为固相反应。
本章所讨论的固相反应采用后一种定义,指固相物质为主要物相参与的化学反应过程。因此,固相反应的研究范围,包括了固相与固相、固相与液相、固相与气相之间三大类的反应现象和反应过程。相应地,除了传统的固相—固相之间的反应类型外,固相反应还应包括固相—液相之间,以及固相—气相之间进行化学反应的类型。
从反应过程分析,固相反应的最大特征是先在两相界面上(固—固界面、固—液界面、固—气界面等)进行化学反应,形成一定厚度的反应产物层;然后经扩散等物质迁移机制,反应物通过产物层进行传质,使得反应继续进行。同时,在上述化学反应过程中还常常伴随一些物理变化过程,有些固相反应的速度也不完全由反应物本身在界面上的化学反应速度所控制,而是由其中的某一物理过程所决定。下面就对固相反应的相关问题进行较为详细的论述。
狭义:固相反应是固相和固相之间发生化学反应,生成新的固相产物的过程。
广义:凡是有固相物质参与的化学反应都可称为固相反应。
一 固相反应的特征:
两相界面进行化学反应;
经扩散等物质迁移机制传质
(i)非均相反应体系
(ii)反应开始温度
(iii)反应过程复杂性
(iV)固相反应的速度
(v)反应中间产物
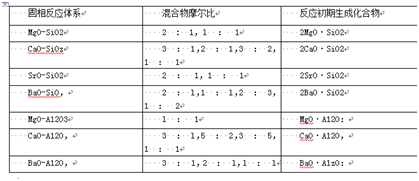
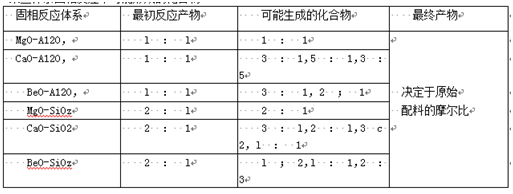
大量实验研究结果表明,固相反应最初产物大多数是结构比较简单的化合物。以碱土金属氧化物与Si02的固相反应为例,无论原始配料比如何,反应首先生成的是摩尔比为2:1的孤岛状结构的正硅酸盐。而碱土金属氧化物与A1;O。的反应,首先生成的是摩尔比为1:1的简单化合物。表6—1和6—2列出了某些体系固相反应可能生成的最初产物及可能生成的一些中间产物种类,而其最终产物则取决于原始配料的摩尔比。
碱土金属氧化物与SiO2,A12O3反应形成的最初产物
某些体系固相反应中可能形成的化合物
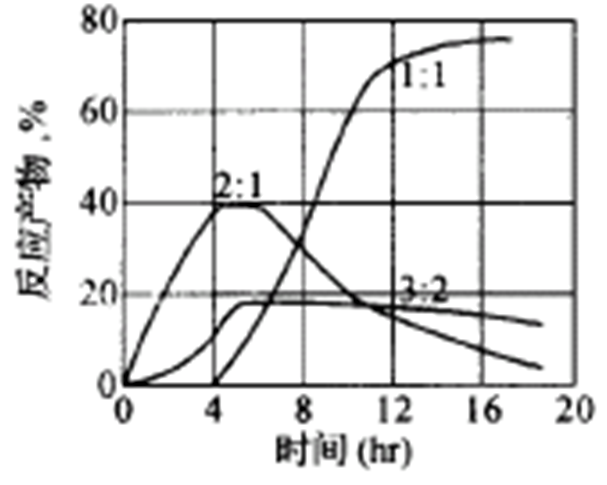
CaO与SiO2按1:1比例混合进行反应的各反应产物量与反应时间的关系图
二 固相反应的分类
固相反应的反应物体系涉及两个或两个以上的物相种类,其反应类型包括化学合成、分解、融化、升华、结晶等,反应过程又包括化学反应、扩散传质等过程。根据分类依据的不同,固相反应可以有如下不同的分类:
第一、按照参与固相反应的原始反应物的物相状态,可以将固相反应大致分成固—固反应、固—液反应、固—气反应等三大类型。
第二、按照固相反应涉及的化学反应类型不同,可以将固相反应分成合成反应、分解反应、置换反应、氧化还原反应等类型。
第三、按照固相反应的产物空间分布尺度,可以将固相反应分为(界面)成层反应、(体相)
非成层反应等两大类型。
第四、按照固相反应的反应控制速度步骤,可以将固相反应分成化学反应控制的固相反
应、扩散控制的固相反应、过渡范围控制的固相反应等类型。
1.固—液反应
固相—液相体系的反应,指至少一种固相物质和液相物质组成的体系发生化学反应的固相反应。其中的液相物质从广义上可分为以下两个大类:
(i)液相为溶液或溶剂物质。固体物质在其中进行的转化、溶解、析出(析晶)等的反应。液相包括水、无机和有机溶剂等。
(ii)液相为高温加热条件下的熔融液相。固相物质在其中发生转化、溶解、析出(析晶)等反应。一般熔融液相包括熔融的金属、非金属以及化合物等。
实际的材料制备过程中,常用的液相物质包括(a)水溶液、(b)部分非水溶剂和(c)熔融液相等三大类。其中,固体一水溶液体系的反应是工业上最常用的反应。而采用高温与加压条件下的水热(溶液)反应则是目前新材料研究中较有特色的一种反应途径。在常温条件下受到固相溶解度,反应速度等的限制,有些反应不易进行。因此,采用高温的水溶液,并施加一定的压力条件的高温水热反应,因其具有特殊的物理化学性质和反应活性,受到了重视。
水热反应进行的温度可以在较宽范围内调节,相应地,化学反应速度变化较大,对整个反应过程的影响也不同。因此按反应速度的控制因素可将水热反应分为两种情况:(a)化学反应支配反应速度的反应情况。此时,固一液相之间的化学反应速度较慢,是整个反应进行的控制步骤,反应速度可通过调节反应体系的温度,压力和气氛等进行控制。(b)扩散过程支配反应速度的反应情况。支配反应速度的扩散过程可以是反应初期的液相内溶质成分的扩散,也可以是在固相表面的液相膜内的扩散,或者是在后期的固相—液相接触表面处反应生成物层内的扩散过程。对应的控制调节条件也不相同。
2.固—气反应
固相—气相反应的原始反应物要求至少有一种固相物质和气相物质,由它们组成的体系发生的化学反应称为固—气反应。按照气相物质在反应过程是否进行化学传输过程,可将固—气反应分为无化学传输的蒸发反应和涉及化学传输过程的气相生长反应两大类。
(1)蒸发反应
蒸发反应的起因是固相物质的饱和蒸汽压,当饱和蒸汽压大于固相表面处的平衡蒸汽压
时,固相物质就不断地离开固相表面。相反的过程就是表面处的蒸汽原子落回到表面处,产生凝聚过程。利用这种蒸发—凝聚过程,控制其热力学、动力学条件,就可以制备出各种新型的薄膜类材料。
(2)气相生长反应
气相生长反应是一种非常有效的制备具有高纯、高分散性和高均匀性要求的材料的方法,可用来制备特种薄膜、单晶材料、高纯物质等。
3.固—固反应
固相—固相反应只涉及两个或以上的固相物质之间的化学反应以及物质的扩散等过程。按照反应进行的形式,固相反应又包括相变反应、固溶反应、离溶反应、析晶反应、化合与分解反应等种类。其中,相变反应是最基本的反应类型,在第五章中已经有详尽介绍,在此只作一些补充。
一般地,固体材料在一定的温度、压力范围内具有一种热力学稳定的晶体结构,随着温度、压力条件的变化,其晶体结构会发生变化,并伴随着材料的力学、电学、磁学性能等的变化。不同的固体结构之间的关联规律可以通过相图进行分析和判读。一般地,这种化学组成不变、晶型发生转变的固相—固相转变反应称为固态相变反应。
从热力学角度分析,按照相变发生点(临界压力、临界温度、临界组分等)的自由能及其导数变化特征,可将相变分为一级相变(自由能的一阶导数不连续)和二级相变(自由能的二阶导数不连续)。
动力学理论上,固—固相变反应过程可按成核与生长理论分析其变化速率,其成核速率与生长速度的处理方法类似液—固相变,两者的表达方式相似。一般地,固态相变时的成核步骤的速率决定了整体相变速率。
另外,从动力学过程来分析固态相变的结构变化特征时,可将固态相变分为位移式相变和重建式相变两大类。位移式相变的特点是在不破坏化学键的前提下,通过原子的协调移动而实现。这类协调移动包括晶格畸变和原子重新堆积等方式,因此相变的位垒低、速度快。常见的位移式相变有金属中的马氏体相变,ZrO2的四方—单斜相变,BaTi03陶瓷在120℃左右的立方—四方相变等。而重建式相变是在破坏化学键的基础上,重新建立新的晶体结构,因此相变位垒高、速度较为缓慢。


